Clear Sky Science · pt
Arquitetura interna projetada de nanopartículas lipídicas núcleo-casca promove liberação eficiente de mRNA do endossoma
Por que essa nova estratégia de entrega importa
Muitos dos medicamentos mais promissores, desde vacinas contra a COVID-19 até tratamentos experimentais contra o câncer, são feitos a partir de RNA mensageiro, ou mRNA. Mas há um problema persistente: assim que essas cadeias frágeis entram em nossas células, a maior parte fica presa e é destruída em pequenos compartimentos internos chamados endossomos. Este estudo apresenta um redesenho inteligente das minúsculas bolsas de gordura, conhecidas como nanopartículas lipídicas, que transportam o mRNA. Ao reorganizar sua estrutura interna em torno de um núcleo de ouro sólido, os pesquisadores melhoram dramaticamente quanto mRNA escapa para o espaço de trabalho da célula, onde ele pode realmente produzir proteínas úteis.
Dando aos minúsculos mensageiros um plano corporal melhor
As vacinas e terapias de mRNA atuais dependem em sua maioria de partículas moles e amorfas feitas de uma mistura de lipídios que envolvem o mRNA. Em teoria, lipídios “ionizáveis” nessas partículas deveriam ficar positivamente carregados no interior ácido dos endossomos e romper a membrana endossomal, liberando o mRNA. Na prática, a carga negativa do mRNA cancela grande parte desse efeito, de modo que apenas cerca de 2% do mRNA entregue chega à maquinaria de produção de proteínas da célula. Os autores fizeram uma pergunta simples, porém poderosa: em vez de apenas mudar a química dos lipídios, e se reengenheirassem a arquitetura interna da partícula para controlar onde o mRNA e os lipídios ficam em relação uns aos outros?
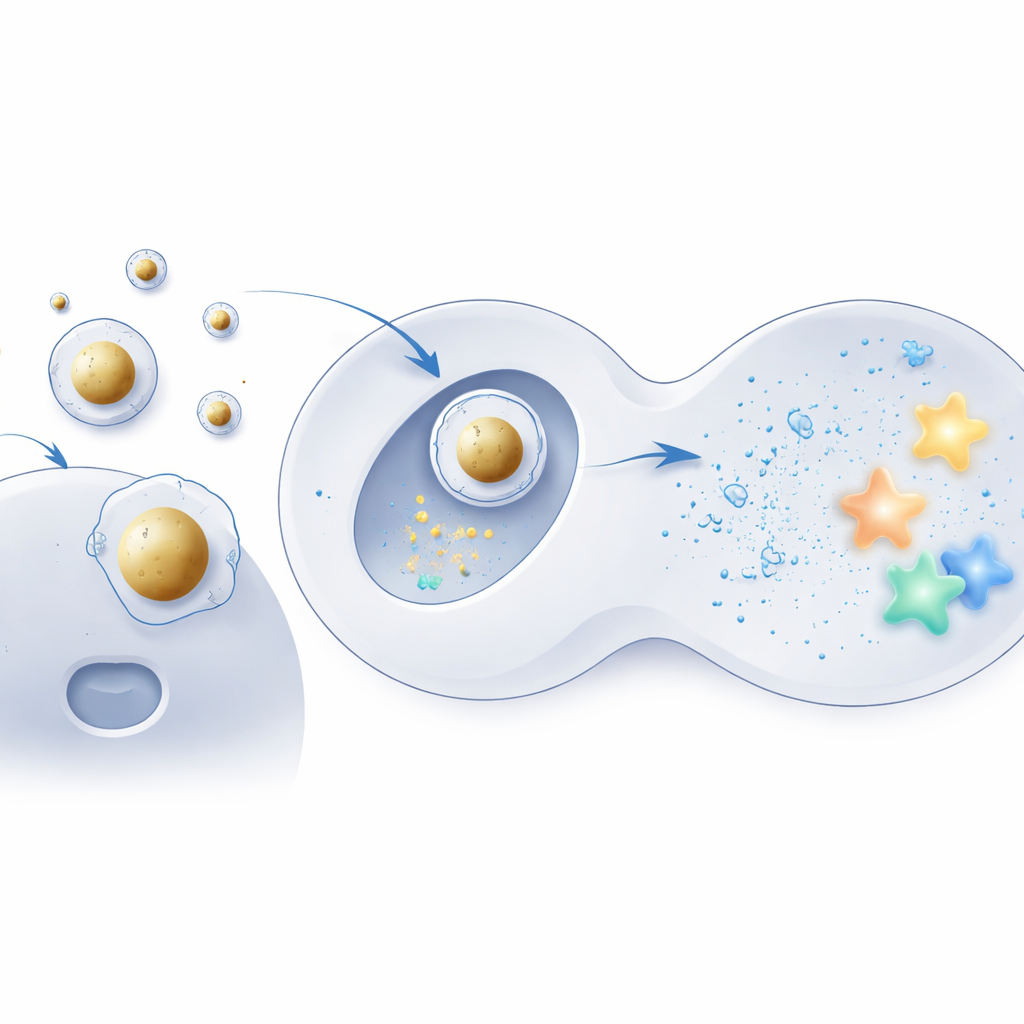
Construindo uma casca de entrega centrada em ouro
Para testar essa ideia, a equipe usou pequenas esferas de ouro como núcleos rígidos e as revestiu com os mesmos lipídios ionizáveis usados em formulações convencionais. O mRNA, carregado negativamente, foi primeiro condensado sobre esses núcleos e só então o conjunto foi envolvido em uma mistura familiar de lipídios auxiliares e moléculas estabilizadoras, criando uma estrutura ordenada núcleo–casca. Microscopia eletrônica e simulações computacionais mostraram que essas “Au‑LNPs” eram altamente uniformes, termodinamicamente estáveis e mantinham bem sua forma em condições aquosas semelhantes às do corpo. Importante: a composição lipídica geral permaneceu a mesma das partículas padrão, isolando a estrutura interna — e não os ingredientes — como a mudança-chave.
Como um interior reorganizado aumenta o escape
No ambiente endossomal levemente ácido, o núcleo à base de ouro fica fortemente positivo, atraindo o mRNA carregado negativamente para o interior enquanto empurra os lipídios ionizáveis carregados positivamente para fora, em direção à membrana circundante. Essa segregação impulsionada por carga concentra os lipídios que perturbam a membrana exatamente onde são necessários. Em testes com membranas modelo e em eritrócitos, as novas partículas foram mais eficazes em perfurar membranas em pH baixo, mantendo-se inertes em pH neutro — uma característica de segurança desejável. Em células vivas, imagens de mRNA fluorescente revelaram cerca de um aumento de duas vezes no escape endossomal e um aumento impressionante de ~100 vezes em quanto o mRNA se espalhou pelo citoplasma em comparação com partículas convencionais.
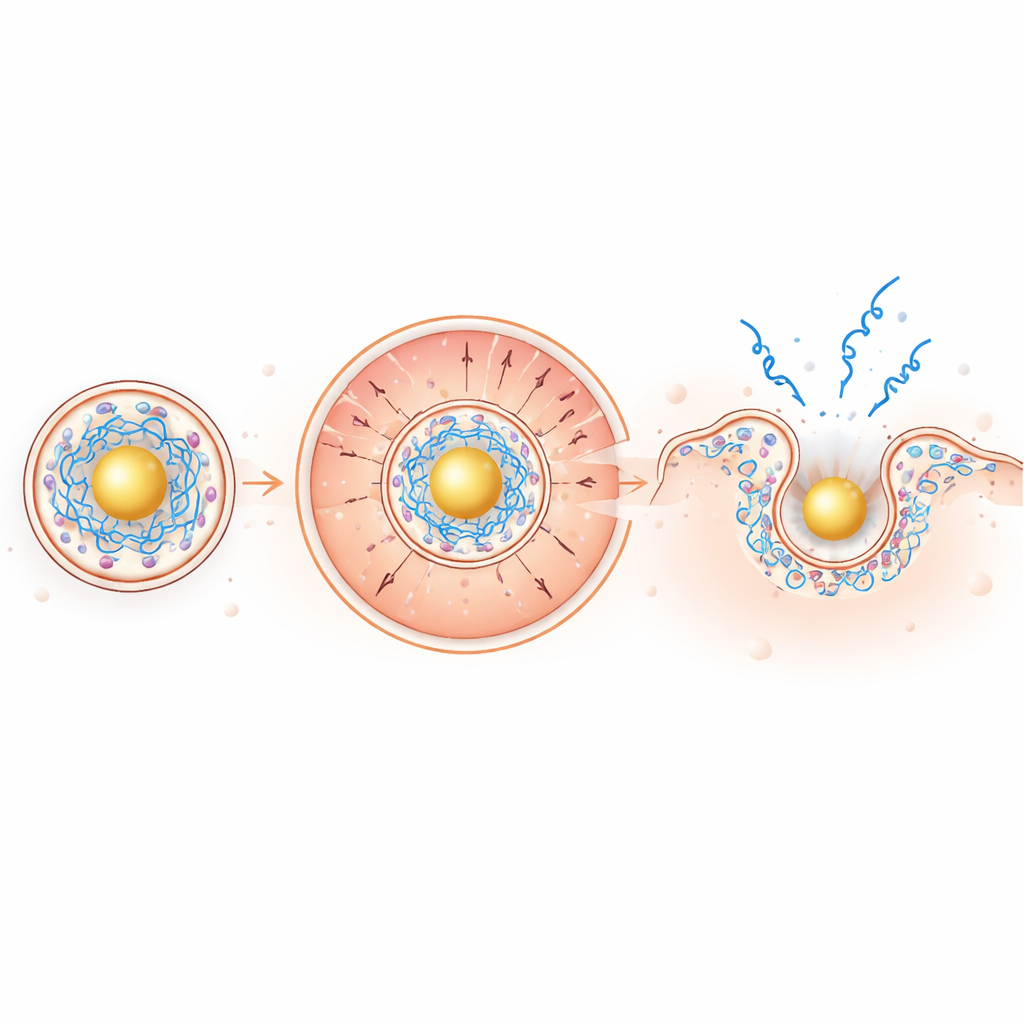
De placas a camundongos: sinais mais fortes e proteção ampliada
Essas vantagens físicas se traduziram em ganhos biológicos reais. Em diversos tipos celulares, as partículas com núcleo de ouro promoveram produção de proteínas-repórter muito maior do que as formulações padrão, especialmente em doses baixas. Em camundongos, elas aumentaram a produção de proteínas dirigidas por mRNA em até cinco a sete vezes após injeções intramusculares ou intravenosas, sem alterar onde no corpo as partículas tendiam a se acumular. Ao serem usadas para entregar um mRNA da proteína spike do SARS‑CoV‑2, as partículas redesenhadas aproximadamente dobraram os níveis de anticorpos após a primeira dose e os aumentaram ainda mais após um reforço, além de gerar anticorpos neutralizantes do vírus mais potentes. Em um modelo desafiador de câncer de mama triplo-negativo, vacinas de mRNA carregadas pelas novas partículas reduziram tumores de forma mais eficaz, diminuíram sinais de atividade tumoral e, notavelmente, prolongaram a sobrevida.
Segurança e um caminho para medicamentos futuros
Apesar de usarem ouro em seu núcleo, as partículas pareceram bem toleradas em camundongos. Pesos corporais, marcadores inflamatórios e exames de tecidos não mostraram toxicidade importante, e os níveis de ouro nos órgãos retornaram próximos ao basal em dois dias. Os autores ressaltam que o ouro serve principalmente como um arcabouço prova-de-conceito: o mesmo princípio de design interno poderia ser aplicado a outros materiais seguros ou biodegradáveis. A mensagem central para não-especialistas é que como embalamos o mRNA dentro de seu minúsculo transportador pode importar tanto quanto com o que o embalamos. Ao conferir às nanopartículas lipídicas um layout interno mais disciplinado, este trabalho oferece uma nova forma de superar um gargalo antigo na entrega de mRNA — desbloqueando vacinas e terapias mais eficazes contra doenças infecciosas, câncer e além.
Citação: Li, T., Zhang, J., Guo, J. et al. Engineered internal architecture of core-shell lipid nanoparticles promotes efficient mRNA endosomal release. Nat Commun 17, 2187 (2026). https://doi.org/10.1038/s41467-026-69017-8
Palavras-chave: entrega de mRNA, nanopartículas lipídicas, escape endossomal, nanomedicina, vacinas de RNA