Clear Sky Science · pt
FGF13 funciona como regulador do eixo ERK/glicólise aeróbica no estado inflamatório durante lesão pulmonar séptica
Por que este estudo importa para pacientes com infecções graves
A sepse é uma complicação com risco de vida de infecções que pode levar à falência pulmonar em poucas horas, deixando os pacientes dependentes de ventilação mecânica e com alto risco de morte. Este estudo explora uma proteína pouco conhecida dentro das nossas células, chamada FGF13, e revela como ela contribui para impulsionar a inflamação descontrolada e o consumo excessivo de energia que danificam gravemente os pulmões durante a sepse. Ao traçar esse circuito de controle oculto, o trabalho aponta novos alvos farmacológicos que podem acalmar a tempestade nos pulmões sem suprimir todo o sistema imune do corpo.
Um jogador oculto no dano pulmonar durante a sepse
Os pesquisadores começaram comparando tecido pulmonar de camundongos sépticos e de pacientes humanos com tecido de controles não sépticos. Eles examinaram uma família de moléculas conhecidas como fatores de crescimento de fibroblastos, que ajudam a manter a saúde pulmonar. Entre elas, FGF13 destacou-se: seus níveis estavam marcadamente mais baixos nos pulmões de pacientes e animais sépticos. Ao mapear onde o FGF13 estava localizado, encontraram-no principalmente dentro de dois tipos celulares chave: células endoteliais, que formam o revestimento interno dos vasos sanguíneos, e macrófagos, células imunes que detectam e ampliam a inflamação. Em pulmões sépticos, células endoteliais e macrófagos positivos para FGF13 estavam fortemente reduzidos, sugerindo que alterações nessa molécula podem estar ligadas à lesão pulmonar grave.
Como o FGF13 transforma defensores pulmonares em agentes de dano
Para testar o que o FGF13 realmente faz, a equipe usou ferramentas genéticas em camundongos para removê-lo de células específicas ou forçar essas células a produzi-lo em excesso. Quando o FGF13 foi deletado apenas nas células endoteliais, camundongos sépticos apresentaram pulmões menos permeáveis e edemaciados, menos células imunes invasoras e melhor sobrevida. O oposto ocorreu quando as células endoteliais foram programadas para superproduzir FGF13: edema pulmonar, sangramento e acúmulo de células inflamatórias pioraram. Um quadro semelhante emergiu nos macrófagos. Camundongos sem FGF13 nesses fagócitos mostraram respostas inflamatórias mais fracas e menor lesão pulmonar, enquanto macrófagos forçados a produzir mais FGF13 liberaram mais moléculas inflamatórias e agravaram o dano. Em cultura celular, reduzir o FGF13 tornou as células dos vasos sanguíneos e os macrófagos menos aderentes, menos inflamadas e menos tóxicas para as células vizinhas.
Células inflamadas mudam para um modo voraz por açúcar
Células inflamadas, como células cancerosas, frequentemente mudam sua estratégia energética: em vez de oxidar o combustível lentamente com oxigênio, elas degradam rapidamente a glicose num processo chamado glicólise aeróbica, gerando ácido lático. Os autores descobriram que o FGF13 incentiva fortemente essa mudança. Em camundongos sépticos sem FGF13 em células endoteliais ou macrófagos, os níveis sanguíneos de lactato foram mais baixos. Em placas de cultura, células com FGF13 reduzido captaram menos glicose e produziram menos lactato após estimulação inflamatória, enquanto células com excesso de FGF13 mostraram glicólise aumentada. Quando os pesquisadores bloquearam a glicólise com um fármaco, o efeito pró-inflamatório do excesso de FGF13 foi em grande parte atenuado, ligando o papel prejudicial da molécula diretamente a esse programa consumidor de açúcar.
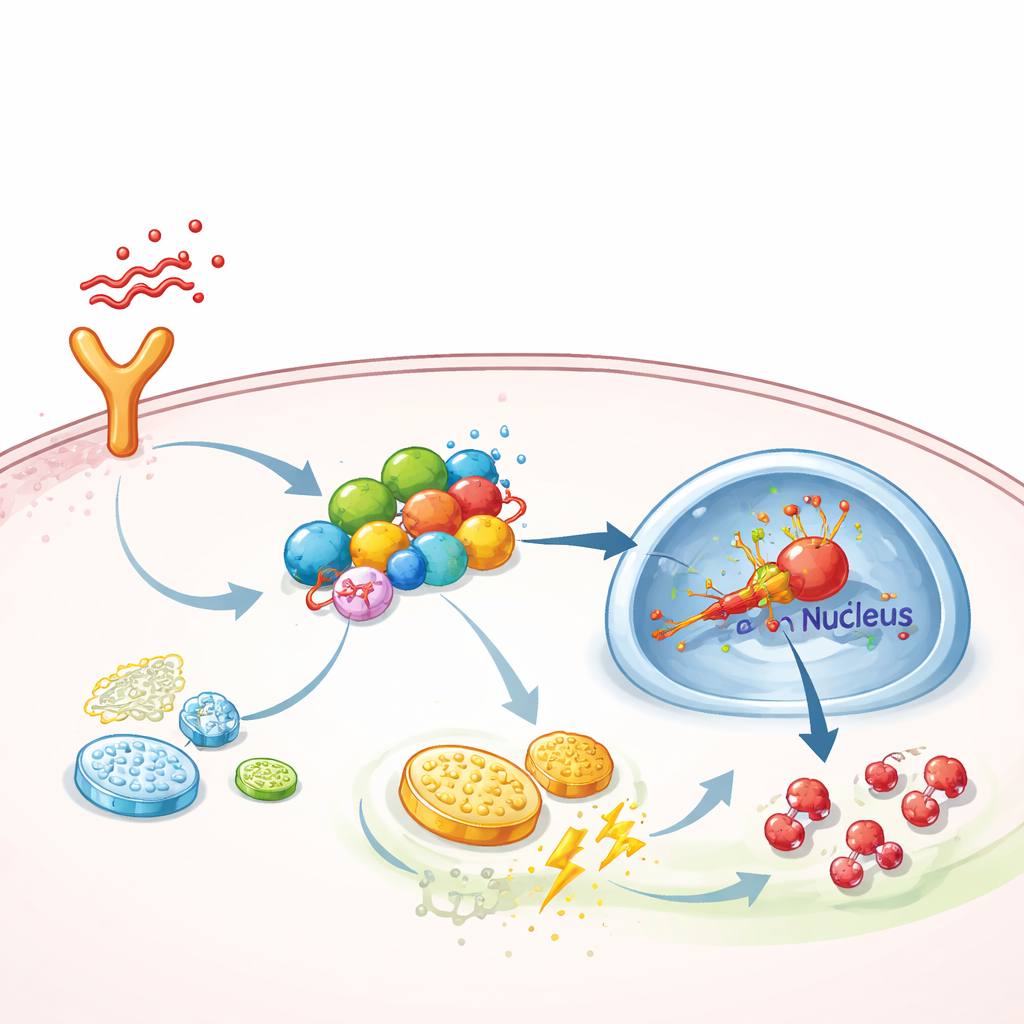
Um andaime molecular que amplifica a sinalização inflamatória
Aprofundando-se, a equipe investigou como o FGF13 empurra as células para esse metabolismo acelerado. Descobriram que o FGF13 se liga fisicamente a várias proteínas de sinalização que formam uma cadeia desde receptores de superfície até o núcleo celular — especificamente a via TAK1–MEK–ERK, conhecida por ativar um regulador mestre de respostas ao baixo oxigênio chamado HIF-1α. O FGF13 atua como um andaime, mantendo esses componentes próximos para que os sinais circulem com mais eficiência. Quando o FGF13 foi reduzido, a ativação de ERK e HIF-1α caiu, e a glicólise diminuiu; quando o FGF13 aumentou, a via tornou-se hiperativa. Superexpressar HIF-1α em camundongos anulou o benefício protetor da remoção do FGF13, enquanto um inibidor seletivo de ERK, SCH772984, neutralizou o dano causado pela superprodução de FGF13 e melhorou as condições pulmonares em animais sépticos.
O que isso significa para futuras terapias contra a sepse
Para um leitor leigo, a mensagem chave é que a lesão pulmonar séptica não é apenas destruição aleatória de tecido; ela é alimentada por um circuito molecular específico dentro das células endoteliais e dos macrófagos. O FGF13 ocupa o centro desse circuito, ajudando a montar um hub de sinalização que força as células para um estado altamente inflamatório e consumidor de glicose. Embora os níveis de FGF13 caiam durante a sepse — provavelmente como parte de uma resposta global ao estresse — este estudo mostra que a proteína remanescente ainda é um potente motor de dano. Ao bloquear os parceiros de sinalização do FGF13 ou a mudança glicolítica que ele promove, pode ser possível reduzir o inchaço, a permeabilidade e a inflamação pulmonar sem paralisar a capacidade do corpo de combater a infecção. Este trabalho, portanto, destaca o FGF13 e o eixo ERK–HIF‑1α–glicólise como pistas promissoras para desenvolver tratamentos mais precisos e seguros para a falência pulmonar associada à sepse.
Citação: Zhu, J., Wang, J., Jiang, C. et al. FGF 13 functions as a regulator of the ERK/aerobic glycolysis axis in the inflammatory state during septic lung injury. Nat Commun 17, 2383 (2026). https://doi.org/10.1038/s41467-026-69014-x
Palavras-chave: lesão pulmonar séptica, FGF13, inflamação endotelial, glicólise aeróbica, sinalização ERK