Clear Sky Science · pt
AACRNL evoluiu de fator de virulência para parasita epigenético que impulsiona a expansão do genoma em eucariotos de vida livre
Quando velhos venenos aprendem novos truques
Nossos genomas não são manuais de instruções silenciosos. São arenas lotadas onde genes, vírus e DNA móvel disputam constantemente espaço e controle. Este estudo revela um ator surpreendente nessa luta: uma proteína que começou sua existência como uma toxina usada por micróbios para atacar hospedeiros, mas que desde então foi reaproveitada dentro de animais de vida livre como uma espécie de "parasita epigenético" que ajuda a expandir sua própria presença no genoma.
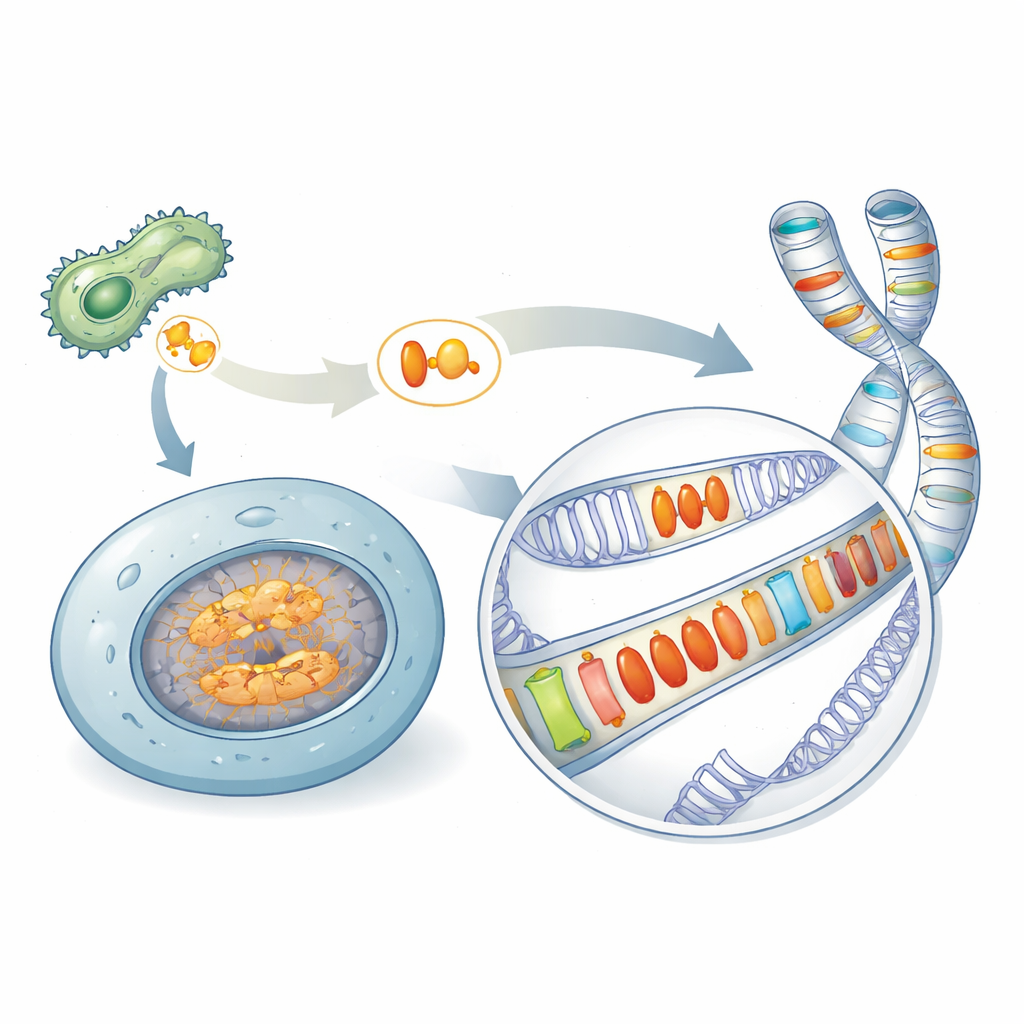
Um legado oculto de armas microbianas
Muitos micróbios causadores de doenças dependem de proteínas especiais, chamadas efetores, para sabotar as defesas dos organismos que infectam. Uma família famosa, conhecida como Crinklers, era tida como restrita a patógenos. Ao vasculhar uma grande variedade de espécies, os autores descobriram proteínas relacionadas — aqui agrupadas sob o nome AACRNL — em lugares inesperados, incluindo esponjas, corais, ouriços-do-mar e peixes ósseos que não são patógenos clássicos. Essas proteínas AACRNL mantêm o núcleo tipo-toxina capaz de modificar quimicamente outras proteínas, mas sua porção frontal de "entrega", que os patógenos usam para invadir células hospedeiras, em grande parte se desfez. Essa mudança estrutural sugere uma transição de atacar outros organismos para agir dentro das próprias células do hospedeiro.
Uma mudança egoísta no genoma
Em peixes ósseos, genes AACRNL ocorrem em várias cópias espalhadas por diferentes cromossomos. Ao comparar trechos vizinhos de DNA, os pesquisadores mostraram que algumas linhagens de AACRNL cessaram de se copiar, enquanto outras se multiplicaram com a ajuda de segmentos de DNA saltadores próximos chamados transposons. Esses transposons atuam como ônibus genômicos: quando se movem ou duplicam, podem arrastar o AACRNL junto. O resultado é um mosaico de cópias repetidas de AACRNL embutidas entre sequências de transposons, uma marca de um gene que se espalha para seu próprio benefício mais do que para o do hospedeiro.
Quebrando o botão mudo do genoma
Normalmente, as células mantêm esse DNA móvel sob rígido controle. Uma salvaguarda chave é uma marca química nas proteínas que empacotam o DNA, conhecida como H3K27me3, que ajuda a manter regiões perigosas ou ruidosas desligadas. Os autores descobriram que uma versão ativa do AACRNL em peixes, chamada AACRNLβ, pode modificar quimicamente a EZH2, a enzima que coloca essa marca repressiva. Quando AACRNLβ altera a EZH2, a quantidade de H3K27me3 em seu próprio endereço genético e nos transposons próximos diminui, o DNA local se abre, e tanto AACRNLβ quanto seus vizinhos transposonais passam a ser mais fortemente expressos. De fato, a proteína pressiona seu próprio botão de "ligar" e levanta os freios sobre os elementos móveis que podem transportá‑la para novos pontos no genoma.
Evadindo os cães de guarda imunológicos
Desencadear transposons e atividade genética incomum arrisca atrair a atenção do sistema imunológico. O estudo mostra que AACRNLβ resolve esse problema também. Ela adiciona uma pequena marca química à TRAF6, uma proteína central que ajuda a ativar sinais antivirais e inflamatórios. Marcada dessa forma, a TRAF6 torna‑se menos estável e é cada vez mais sinalizada para descarte pela maquinaria de limpeza da célula. Com esse hub de sinalização enfraquecido, vias de defesa chave disparam com menos intensidade, criando um ambiente mais tolerante no qual AACRNLβ e seus transposons associados podem persistir e se copiar com menos risco de serem detectados.
Uma corrida armamentista delicada dentro da célula
A história não termina com AACRNLβ correndo sem freios. A mesma proteína TRAF6 que é alvo de AACRNLβ pode, por sua vez, adicionar suas próprias marcas a AACRNLβ, sinalizando a proteína tipo-parasita para destruição. Esse vai‑e‑vem se assemelha a uma corrida armamentista molecular: AACRNLβ usa química derivada de toxinas para moldar a cromatina e a imunidade a seu favor, enquanto proteínas do hospedeiro revidam degradando‑a e mantendo sua atividade esporádica e arriscada. Os autores argumentam que esse cabo de guerra permitiu que uma antiga arma microbiana sobrevivesse como um residente egoísta em genomas de vida livre, ampliando o conteúdo de DNA e remodelando as regras do conflito genético de dentro para fora.
Por que isso importa para nossa visão dos genomas
Para um não‑especialista, a mensagem principal é que genomas não são apenas plantas otimizadas para a sobrevivência do hospedeiro. Eles também abrigam oportunistas. Este trabalho mostra que até toxinas clássicas podem ser domesticadas em elementos desse tipo, usando sua química destrutiva original para escapar de fechaduras epigenéticas e alarmes imunes, e para se espalhar pelo genoma ao longo do tempo evolutivo. Compreender esse tipo de conflito oculto ajuda a explicar por que os genomas são tão grandes, complexos e dinâmicos — e sugere que outras toxinas “aposentadas” podem estar silenciosamente reescrevendo o DNA em muitas espécies, talvez inclusive na nossa.
Citação: Xu, T., Geng, S., Lv, X. et al. AACRNL evolved from virulence factor to epigenetic parasite driving genome expansion in free-living eukaryotes. Nat Commun 17, 2130 (2026). https://doi.org/10.1038/s41467-026-69012-z
Palavras-chave: elementos genéticos egoístas, evolução do genoma, regulação epigenética, transposons, imunidade inata