Clear Sky Science · pt
Imobilização sinérgica multicomponente via estratégias dinâmicas e in situ para construção de biofarmacêuticos hierárquicos
Por que é importante construir medicamentos mais inteligentes
Muitos dos medicamentos mais potentes de hoje são grandes e frágeis moléculas biológicas, como proteínas e enzimas. Elas podem combater o câncer, matar bactérias nocivas e acelerar a cicatrização, mas são facilmente danificadas e difíceis de entregar ao local certo do corpo. Este artigo descreve uma nova maneira de “embalar” vários desses componentes delicados juntos dentro de um material protetor e esponjoso, para que possam atuar em sequência com mais eficácia e menos efeitos colaterais.
Transformando um cristal em um edifício molecular de apartamentos
Os pesquisadores começam com um material poroso especial feito de íons metálicos e pequenos blocos orgânicos. Ele se comporta um pouco como um minúsculo edifício flexível cheio de quartos e corredores. Eles mostram que essa estrutura, chamada estrutura pirimidínica zeolítica, pode ser cultivada em torno de proteínas de modo que as proteínas fiquem protegidas dentro do cristal. Esse aprisionamento “in situ” não esmaga nem desativa as proteínas, e imagens cuidadosas confirmam que elas estão distribuídas de maneira uniforme por todo o interior, muito parecido com inquilinos morando em todos os andares de um prédio.
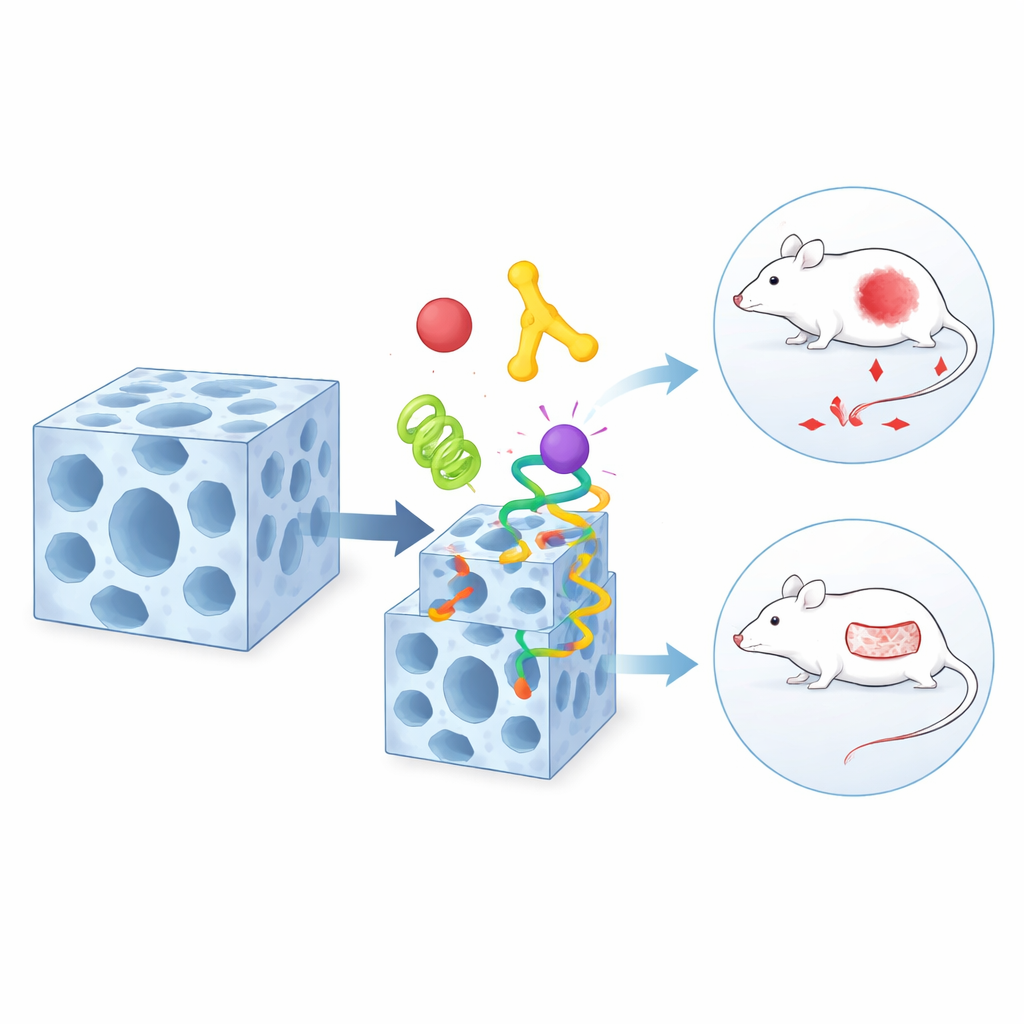
Um hospedeiro que muda de forma para decoração de superfície
O mesmo material tem um segundo truque surpreendente: ele pode mudar reversivelmente sua estrutura interna quando exposto a certos solventes ou à água. Durante essa transformação suave, algumas conexões químicas na estrutura afrouxam e depois se reformam. A equipe descobriu que grupos químicos específicos na superfície das proteínas — como os encontrados em certos aminoácidos — podem tirar vantagem desse momento de fragilidade. Eles competem temporariamente com os blocos de construção originais da estrutura e se inserem em “defeitos” recém-formados próximos à superfície. Como resultado, uma camada de proteínas fica ancorada principalmente na parte externa do cristal, enquanto as internas permanecem em seu lugar. Esse processo de troca dinâmica permite aos cientistas decidir quais componentes vivem no interior profundo e quais decoram a camada externa.
Projetando linhas de montagem enzimáticas
Com o controle tanto do espaço interno quanto do externo, os autores constroem minúsculas “linhas de montagem” enzimáticas. Em um exemplo, uma enzima que converte açúcar em um subproduto agressivo é aprisionada dentro da estrutura, enquanto uma segunda enzima que degrada com segurança esse subproduto fica fixada perto da superfície. Esse arranjo interno–externo faz a reação correr mais rápido e de forma mais eficiente do que designs tradicionais de núcleo–casca ou misturas aleatórias de enzimas. Como as enzimas externas são mais acessíveis às moléculas e o intermediário prejudicial é rapidamente removido, o sistema permanece ativo por muitos ciclos e tolera melhor calor, condições agressivas e uso repetido.
Pacotes inteligentes anti-câncer e anti-bacterianos
O verdadeiro poder dessa abordagem aparece quando ela é aplicada à medicina. A equipe combina uma proteína que direciona tumores, uma enzima que consome glicose e um fármaco quimioterápico padrão em uma única partícula em camadas. O componente de direcionamento na superfície guia a partícula até as células cancerígenas, a enzima esgota seu suprimento de energia ao consumir o açúcar local, e o fármaco de pequena molécula aplica um golpe letal adicional. Em camundongos com implantes de tumores humanos, esse pacote triplo reduz tumores muito mais eficazmente do que qualquer um dos componentes isolados ou misturas mais simples. Em um projeto separado, os autores adaptam a estrutura para feridas cutâneas infectadas colocando um peptídeo antibacteriano e uma enzima remodeladora de tecido em regiões diferentes do mesmo transportador. Em modelos de rato, essas partículas reduzem fortemente a infecção e aceleram o fechamento de feridas difíceis em comparação com tratamentos convencionais.

Como este trabalho avança a medicina
Para um não especialista, a mensagem principal é que este estudo transforma um único cristal poroso em uma casa programável para muitos tipos de moléculas terapêuticas. Ao decidir quem vive no interior, quem reside na superfície e em que proporção, os pesquisadores podem orquestrar tratamentos em etapas — primeiro direcionamento, depois ataque, depois reparo — dentro de um único objeto minúsculo. Essa estratégia não apenas protege fármacos biológicos frágeis, mas também permite que eles se auxiliem, levando a terapias anti-câncer e anti-bacterianas mais fortes e precisas. Os mesmos princípios de design poderiam ser adaptados para muitos futuros “medicamentos inteligentes” que precisam de múltiplos componentes trabalhando juntos no lugar certo e no momento certo.
Citação: Yang, M., Meng, X., Shi, R. et al. Multicomponent synergistic immobilization via in-situ and dynamic exchange strategies for constructing hierarchical biopharmaceuticals. Nat Commun 17, 2208 (2026). https://doi.org/10.1038/s41467-026-69009-8
Palavras-chave: estruturas metal-orgânicas, imobilização de enzimas, nanomedicina contra o câncer, cicatrização de feridas, liberação de biofarmacêuticos