Clear Sky Science · pt
Escherichia coli promove a metástase do câncer colorretal mantendo laços entre potenciadores e promotores por meio da liberação de armadilhas extracelulares de neutrófilos
Microbiota intestinal e a via secreta do câncer
O câncer colorretal frequentemente mata não por causa do tumor original no intestino, mas porque células tumorais migram para o fígado e aí se instalam. Este estudo revela um cúmplice inesperado nessa jornada: uma bactéria intestinal comum, Escherichia coli. Ao rastrear a cadeia de eventos desde bactérias no intestino até tumores agressivos no fígado, os pesquisadores mostram como micróbios, células imunes e a arquitetura do DNA dentro das células cancerosas podem atuar em conjunto para alimentar a metástase — e sugerem novas formas de interromper essa cadeia.
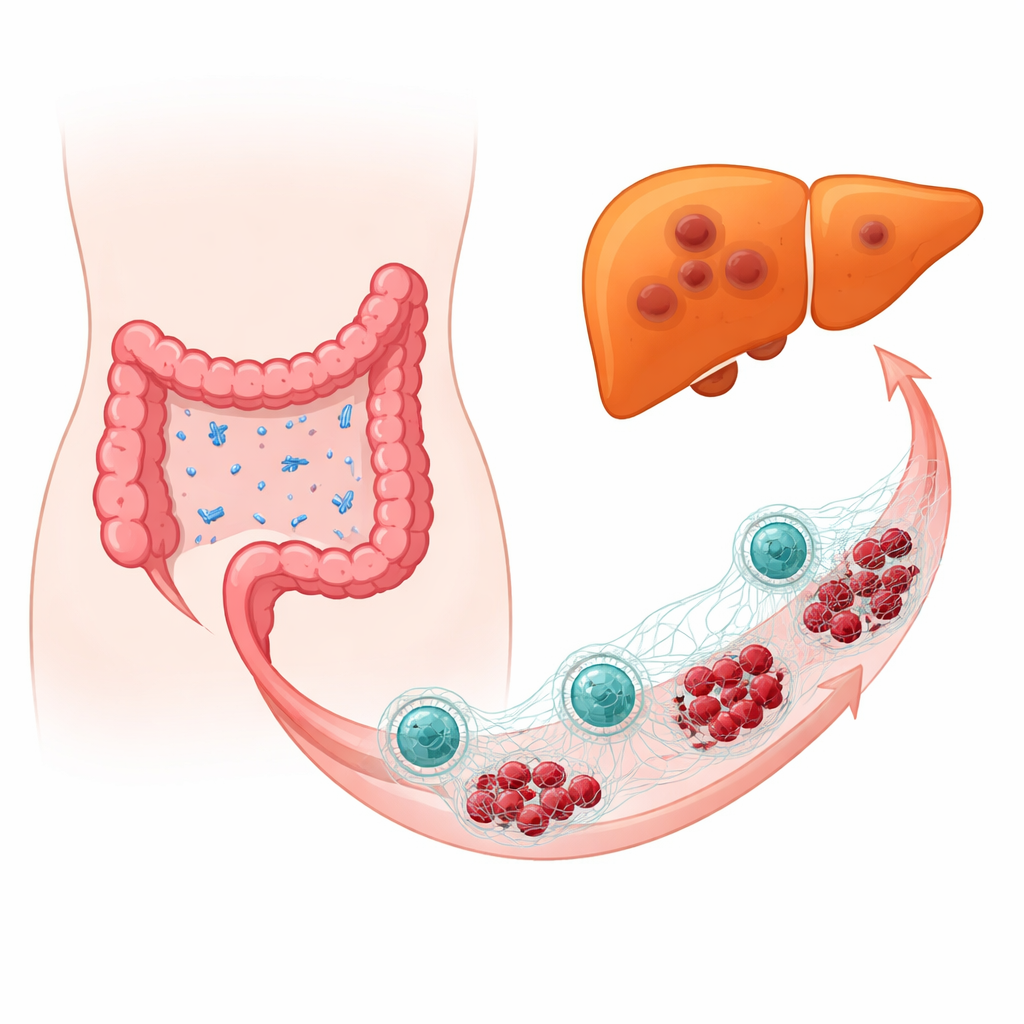
Quando bactérias amistosas se tornam hostis
A equipe examinou amostras de tumor de pessoas com câncer colorretal, comparando aquelas cujo câncer havia se espalhado para o fígado com as que não haviam metastizado. Usando perfis microbianos baseados em DNA de alta resolução, encontraram E. coli muito mais abundante em tumores que já haviam semeado o fígado. Em modelos murinos e em camundongos com sistemas imunes humanizados, a adição deliberada de E. coli próxima a tumores colorretais tornou as metástases hepáticas maiores e mais frequentes e empurrou as células tumorais para um estado mais móvel e invasivo. Mesmo quando a maior parte da flora intestinal normal foi eliminada com antibióticos e apenas E. coli foi reintroduzida, a bactéria ainda aumentou o crescimento e a disseminação do tumor, implicando a própria E. coli em vez de uma perturbação geral do microbioma.
Redes imunes que ajudam o câncer a escapar
Neutrófilos — células imunes de primeira linha que normalmente prendem e matam micróbios — emergiram como intermediários cruciais. Em resposta à E. coli, neutrófilos liberaram estruturas em forma de rede chamadas armadilhas extracelulares, compostas de DNA e proteínas tóxicas. Essas redes destinam-se a capturar bactérias, mas nesse contexto acabaram protegendo e fortalecendo inadvertidamente as células cancerosas. Quando os pesquisadores degradaram essas redes com enzimas ou bloquearam enzimas-chave necessárias para formá‑las, as metástases hepáticas encolheram e os tumores ficaram menos agressivos. A depleção de neutrófilos teve efeito protetor semelhante, apontando para um paradoxo: a própria resposta imune que combate infecções estava sendo sequestrada para ajudar o câncer a se espalhar.
De sinais elétricos a interruptores genéticos
Como redes pegajosas de DNA fora da célula tumoral poderiam alterar o que acontece no interior de seu núcleo? A resposta esteve no cálcio, um íon simples que atua como sinal elétrico nas células. O estudo mostrou que as armadilhas de neutrófilos aumentaram o nível de uma proteína canal, TRPC1, nas células do câncer colorretal. TRPC1 permitiu que mais cálcio entrasse na célula, o que por sua vez ativou um regulador sensível ao cálcio chamado NFATC3 e criou um circuito auto‑reforçador que manteve os níveis de TRPC1 elevados. Esse surto de cálcio incentivou duas pequenas proteínas, S100A8 e S100A9, a se unirem e então se ligarem a uma proteína de controle de crescimento importante, STAT3. O trio migrou para o núcleo, onde fez algo especialmente marcante: ajudou a dobrar e formar laços no DNA para que regiões regulatórias distantes e locais de início de genes se tocassem, estabilizando fisicamente “laços potenciador–promotor” que aumentam a expressão de certos genes.
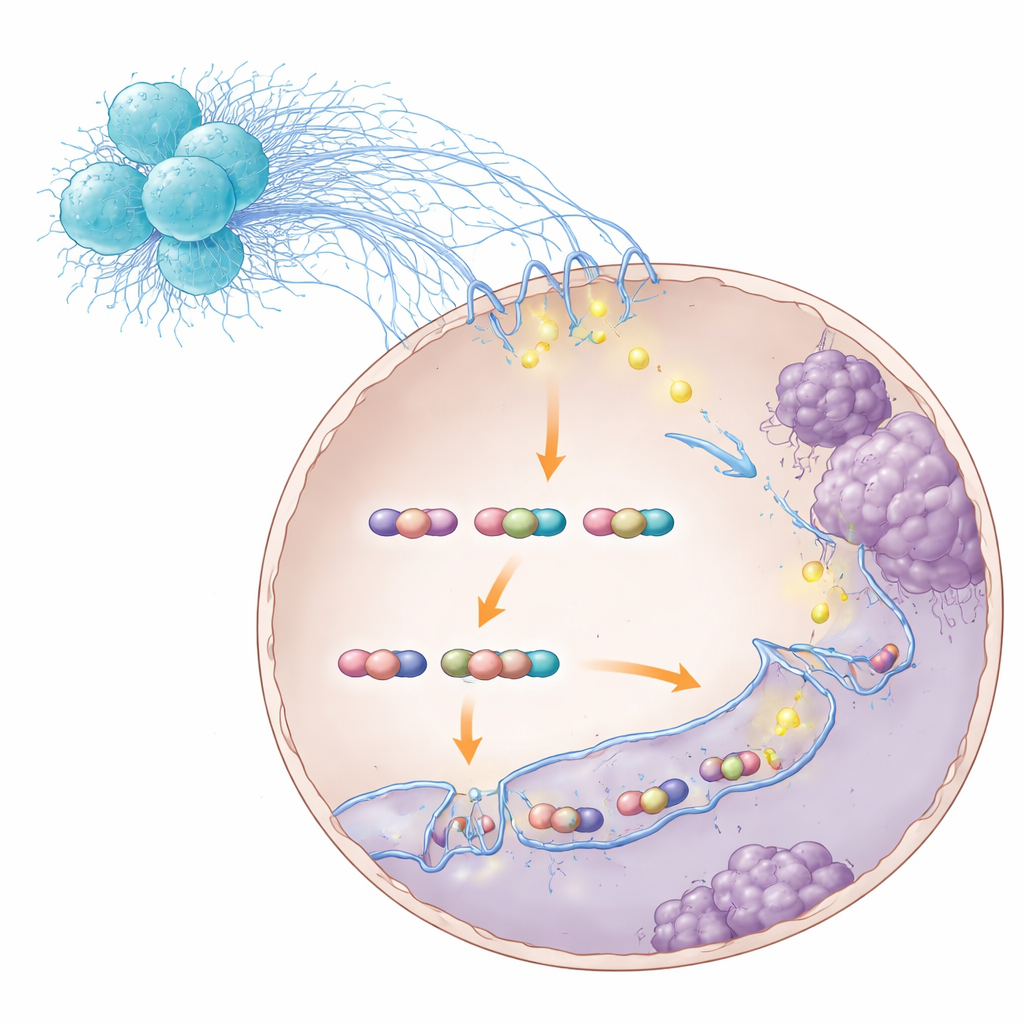
Reprogramando células cancerosas para a metástase
Ao mapear os contatos tridimensionais ao longo do genoma, os pesquisadores descobriram que o complexo STAT3–S100A8/9 promovia laços que favoreciam genes envolvidos em movimento e invasão celular. Um gene de destaque foi TNS1, que impulsiona as células a afrouxarem suas aderências e migrarem com mais facilidade. Quando o complexo STAT3–S100A8/9 foi perturbado, muitos desses laços enfraqueceram ou desapareceram, os níveis de TNS1 caíram e as células cancerosas perderam parte de sua capacidade de invadir e semear o fígado. Importante, essa perturbação não impediu que STAT3 tocasse o DNA por completo — ela desestabilizou especificamente a arquitetura de laços que superativava programas metastáticos. Em modelos animais, bloquear diferentes etapas dessa cadeia — desde a molécula sinalizadora bacteriana RIPK2 nos neutrófilos, passando por S100A8/9, até o próprio STAT3 — reduziu a metástase hepática e melhorou a sobrevida.
Quebrando a cadeia entre micróbios e tumores
Para não especialistas, a mensagem-chave é que uma bactéria intestinal comum pode ajudar o câncer colorretal a se espalhar ao provocar primeiro as células imunes a lançar redes de DNA e depois usar essas redes para acionar um circuito movido a cálcio que reconfigura como genes do câncer são ativados. Em vez de depender de antibióticos de amplo espectro, que podem prejudicar micróbios benéficos e diminuir a eficácia da imunoterapia do câncer, o trabalho aponta para alvos farmacológicos mais precisos: sensores bacterianos como RIPK2, a cascata TRPC1–cálcio–S100A8/9 e os laços de DNA dirigidos por STAT3 que travam genes relacionados à metástase em alta atividade. Interromper essa cadeia em um ou mais pontos pode oferecer uma nova estratégia para evitar que o câncer colorretal transforme um problema local no intestino em uma doença letal no fígado.
Citação: Pan, B., Yao, Y., Zhang, Z. et al. Escherichia coli promotes colorectal cancer metastasis by maintaining enhancer-promoter loops through releasing neutrophil extracellular traps. Nat Commun 17, 2290 (2026). https://doi.org/10.1038/s41467-026-69005-y
Palavras-chave: metástase do câncer colorretal, microbioma intestinal, armadilhas extracelulares de neutrófilos, sinalização STAT3, regulação epigenética de genes