Clear Sky Science · pt
O desenho de inibidores covalentes confere atividade contra as formas ligadas a GDP e GTP de KRAS G12C
Por que isso importa para tratamentos futuros contra o câncer
Os cânceres impulsionados por mutações no gene chamado KRAS há muito são considerados entre os mais difíceis de tratar. Recentemente, novos medicamentos que desligam uma forma mutante comum, KRAS G12C, chegaram aos pacientes e começaram a mudar esse cenário. Este artigo explora uma ideia ainda mais ambiciosa: podemos projetar fármacos que bloqueiem KRAS G12C em seus dois principais modos de atuação dentro da célula, e isso tornaria o tratamento do câncer mais rápido, mais eficaz ou mais duradouro?
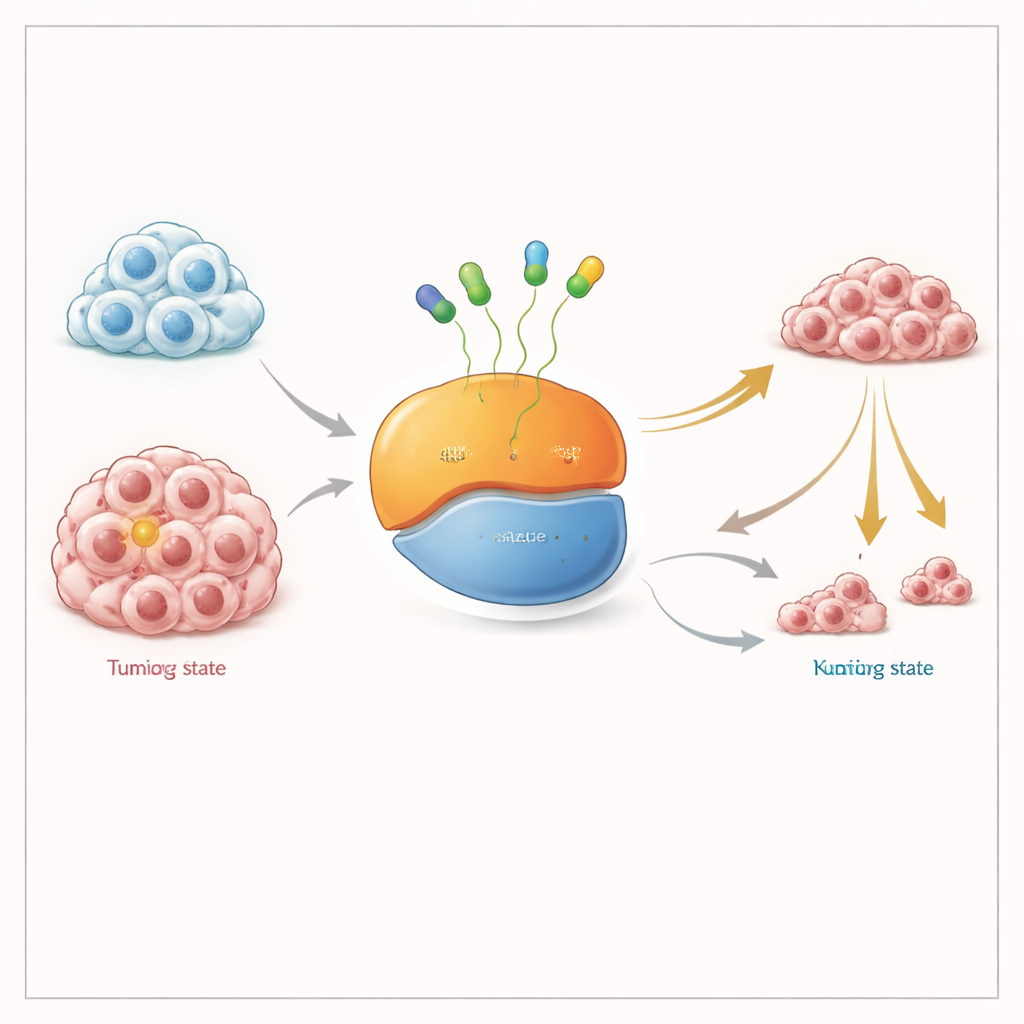
Desligando um interruptor molecular em duas posições
KRAS age como um pequeno interruptor liga–desliga dos sinais de crescimento celular. Ele alterna entre um estado “desligado”, no qual está ligado a uma molécula transportadora de energia (GDP), e um estado “ligado”, no qual carrega outra (GTP). A mutação KRAS G12C mantém esse interruptor parcialmente ligado e alimenta o crescimento tumoral. Medicamentos existentes aprovados pela FDA prendem-se à forma “desligada” e a travam; com o tempo, à medida que mais KRAS passa por essa forma, o total da proteína mutante fica desativado. Muitos cientistas defendem que um fármaco capaz de agarrar KRAS tanto em sua forma ligada quanto desligada deveria funcionar melhor, especialmente em tumores que se adaptam mantendo mais KRAS no estado ativo.
Projetando um novo tipo de gancho molecular
Os autores partiram para construir esses fármacos de duplo propósito. Eles focaram em um pequeno sulco próximo a uma região flexível do KRAS chamada Switch II, onde os medicamentos atuais já se ligam. Em vez de alterar o quão bem suas moléculas se encaixavam nesse sulco, reengenheiraram a porção “warhead” que forma uma ligação química permanente com a cisteína mutante na posição 12. Por meio de modelagem computacional e síntese de dezenas de variantes, descobriram um warhead especial em três partes que se aproxima da cisteína por um ângulo ligeiramente diferente. Esse deslocamento sutil cria espaço suficiente para a molécula maior de GTP, permitindo que os novos compostos se liguem ao KRAS tanto quando ele carrega GDP quanto GTP. Testes bioquímicos confirmaram que compostos líderes podiam interromper a interação do KRAS com um parceiro de sinalização chave, o RAF, em ambos os estados.
Observando como a proteína se remodela
Para entender por que essas moléculas funcionavam, a equipe determinou estruturas cristalográficas de alta resolução do fármaco ligado ao KRAS. Essas imagens mostraram que o novo warhead reage em um sítio incomum no esqueleto químico, desprendendo um átomo de flúor e formando uma ligação covalente em um carbono diferente do observado em fármacos típicos contra cisteínas. Essa química alterada ajuda o medicamento a se encaixar no bolso do Switch II mesmo quando GTP está presente. As estruturas também revelaram que, ao se ligar, o inibidor desloca uma pequena molécula de água e rearranja sutilmente outro laço, o Switch I, que normalmente contacta proteínas de sinalização a jusante. Esse remodelamento alostérico aproxima dois aminoácidos para formar uma ponte salina firme, distorcendo a superfície de modo que o RAF não consegue mais se acoplar e transmitir os sinais de crescimento.
Desligamento rápido, mas sem efeito de longo prazo mais forte
Munidos dessas percepções estruturais, os pesquisadores refinaram dois compostos líderes que se ligam de forma eficiente e seletiva ao KRAS G12C, poupando em grande parte outras proteínas contendo cisteínas. Em linhagens celulares tumorais, esses inibidores de duplo estado bloquearam rapidamente um importante circuito de sinalização conhecido como via MAPK, medido pela perda de uma marca química na proteína ERK e pela forte supressão do crescimento celular. Eles inativaram o KRAS nas células mais rapidamente do que um medicamento de referência que só mira o estado inativo. Em modelos murinos de tumor, um composto líder mostrou boa disponibilidade oral, formou rapidamente ligações covalentes com o alvo e encolheu tumores ou retardou seu crescimento. Ainda assim, quando a equipe comparou inibidores de duplo estado e de estado inativo por períodos mais longos, ambas as classes acabaram alcançando níveis similares de inativação do KRAS, inibição da via e controle tumoral.
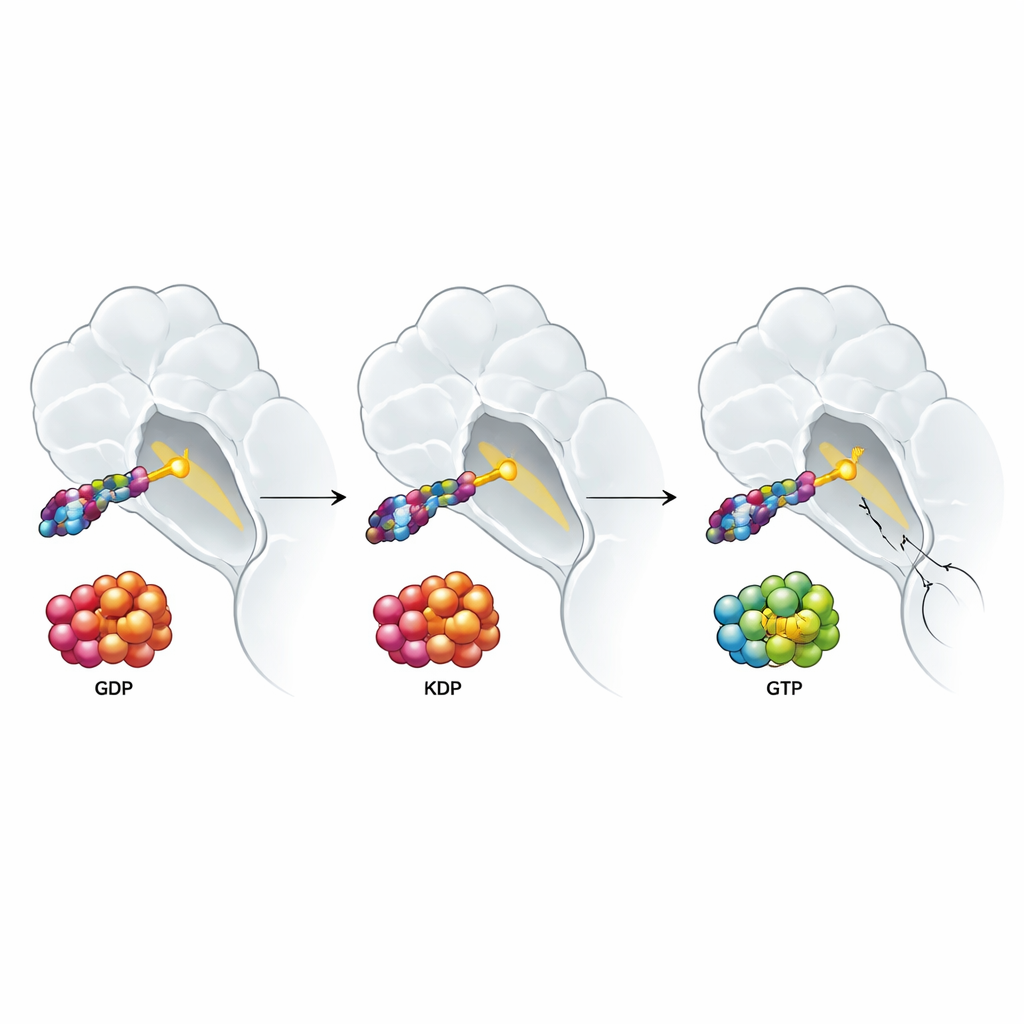
Por que os sinais de crescimento do entorno tumoral ainda prevalecem
O estudo também investigou como sinais do ambiente tumoral afetam esses fármacos. Fatores de crescimento como EGF e HGF, abundantes ao redor de muitos tumores, empurram as proteínas RAS para a forma ativa carregada por GTP e são conhecidos por atenuar respostas a terapias direcionadas. Poder-se-ia esperar que um fármaco que se liga à forma ativa do KRAS G12C evitasse esse problema. Em vez disso, os autores descobriram que tanto os inibidores de duplo estado quanto os de estado inativo perdiam potência quando esses fatores de crescimento estavam presentes. Experimentos detalhados apontaram um culpado surpreendente: a ativação das formas normais, não mutadas, de RAS (H‑RAS e N‑RAS), que podem contornar o KRAS G12C e manter os sinais de crescimento fluindo. Quando os pesquisadores deletaram H‑RAS e N‑RAS em uma linhagem de câncer de pulmão, a resistência induzida por fatores de crescimento desapareceu em grande parte para todos os tipos de drogas direcionadas ao KRAS G12C, enquanto um fármaco que bloqueia um passo a jusante na via foi menos afetado desde o início.
O que isso significa para pacientes e desenvolvimento de medicamentos
No conjunto, o trabalho demonstra que é quimicamente e estruturalmente viável construir fármacos covalentes contra KRAS G12C que capturem a proteína em seus estados ativo e inativo, e que esses inibidores de duplo estado podem desligar a sinalização mais rapidamente do que medicamentos existentes. Contudo, o engajamento rápido não se traduziu em controle tumoral claramente melhor nem em solução para a resistência induzida por fatores de crescimento em modelos pré-clínicos. Para pacientes, isso sugere que simplesmente adicionar atividade contra a forma ativa do KRAS pode não ser suficiente; estratégias combinatórias que também enderecem outros membros da família RAS ou nós de sinalização a jusante podem ser necessárias. O novo warhead e o roteiro estrutural apresentados aqui, no entanto, ampliam o conjunto de ferramentas para targeting do KRAS e informarão gerações futuras de terapias de precisão contra o câncer.
Citação: Condakes, M.L., Zhang, Z., Danahy, D.B. et al. Covalent inhibitor design confers activity against both GDP- and GTP-bound forms of KRAS G12C. Nat Commun 17, 2233 (2026). https://doi.org/10.1038/s41467-026-69003-0
Palavras-chave: KRAS G12C, inibidor covalente, inibição de duplo estado, sinalização MAPK, resistência a medicamentos