Clear Sky Science · pt
Um circuito basalo‑pré‑frontal‑talâmico definido molecularmente regula dimensões sensoriais e afetivas da dor em camundongos machos
Por que esse circuito cerebral importa para a dor
Dor é mais do que uma fisgada aguda ou um incômodo surdo; também traz um impacto emocional e pode remodelar nosso humor e comportamento por anos. Muitos pacientes com dor crônica têm pouco alívio com os medicamentos atuais e frequentemente enfrentam efeitos colaterais sérios. Este estudo em camundongos machos revela um circuito cerebral precisamente definido que ajuda o cérebro a modular a dor, tanto em termos da intensidade sensorial quanto do sofrimento emocional. Ao mapear e controlar esse caminho, o trabalho aponta para novas formas mais direcionadas de aliviar a dor crônica sem depender exclusivamente dos analgésicos tradicionais.
Uma rodovia oculta do cérebro pensante ao centro da dor
Os pesquisadores concentraram‑se no córtex pré‑frontal medial, uma região frontal envolvida em tomada de decisão, emoção e controle da dor, e no tálamo, um centro profundo de retransmissão que molda tanto a intensidade quanto a desagradabilidade da dor. Eles descobriram que um grupo específico de células no córtex pré‑frontal medial, marcadas por um gene chamado Foxp2, forma uma via de saída principal para o tálamo. Essas células localizam‑se principalmente na camada cortical mais profunda e enviam longas fibras para núcleos talâmicos particulares, enquanto em grande parte ignoram outros alvos típicos do pré‑frontal. Usando métodos de rastreio e mapeamento de cérebro inteiro, a equipe mostrou que esses neurônios marcados por Foxp2 se conectam fortemente a três regiões talâmicas conhecidas por influenciar o processamento da dor: o núcleo parataenial, o tálamo mediodorsal e o tálamo ventromedial. 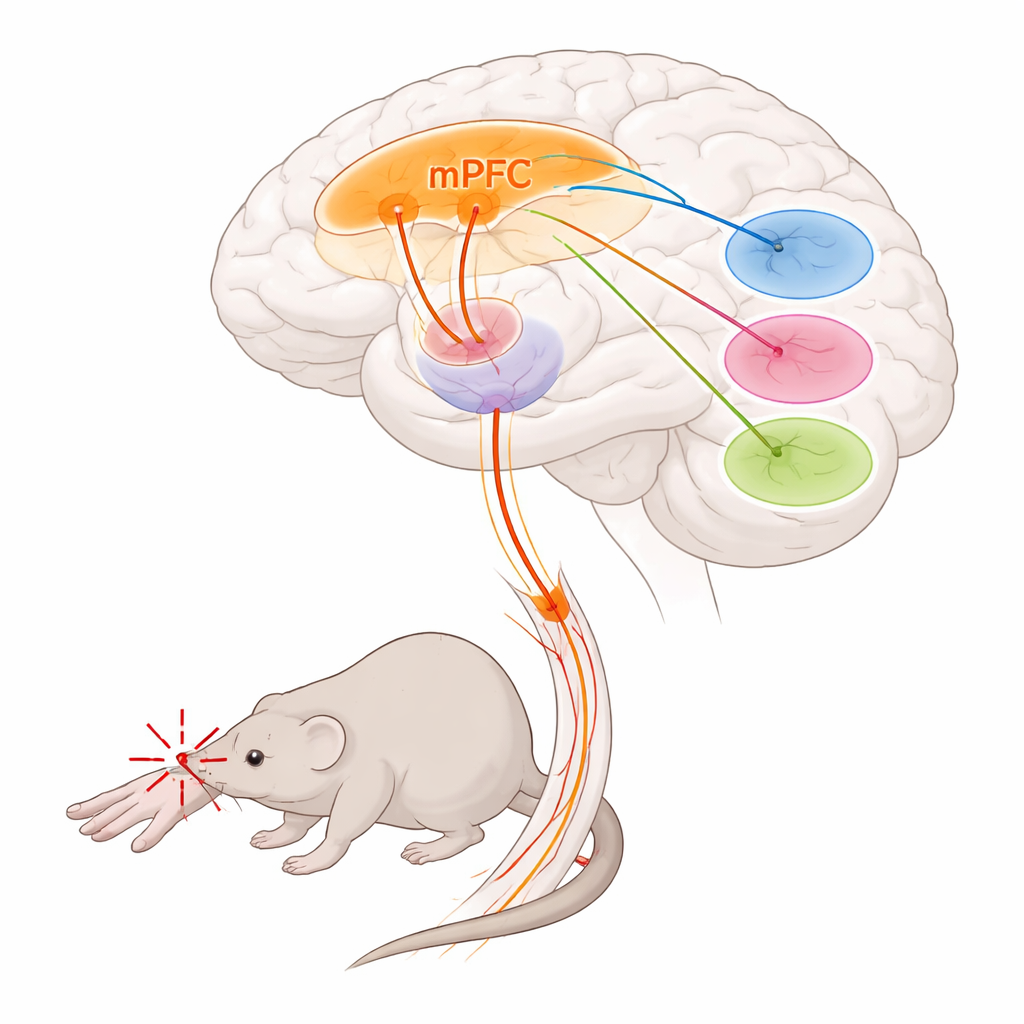
Quando a dor atinge, um centro chave de controle fica silencioso
Para ver como essa via se comporta durante a dor, os cientistas implantaram lentes minúsculas acima do córtex pré‑frontal medial e registraram a atividade de neurônios individuais marcados por Foxp2 em camundongos acordados. Durante pinçamentos mecânicos breves, dor química induzida por formalina e dor inflamatória de longa duração, essas células consistentemente silenciaram: a maioria mostrou menos explosões de atividade durante episódios dolorosos e nos dias seguintes à lesão inflamatória. Esse desligamento não foi sutil; em algumas condições mais de um terço a quase metade das células tornaram‑se marcadamente menos ativas. A descoberta sugere que estados de dor aguda e crônica podem, em parte, refletir o silenciamento de um sistema de freio pré‑frontal natural que, de outra forma, ajudaria a manter a dor sob controle.
Ligar e desligar o circuito remodela a dor
A equipe então perguntou se esse silenciamento era apenas um efeito colateral da dor ou um dirigidor dela. Usando ferramentas genéticas, eles bloquearam a saída dos neurônios marcados por Foxp2 a longo prazo ou aumentaram brevemente sua atividade. A inativação persistente tornou os camundongos mais sensíveis ao toque e ao calor, indicando que essa via normalmente restringe sinais de dor de entrada. Em contraste, a ativação de curto prazo elevou o limiar para estímulos dolorosos, reduziu a lambedura em fase tardia no teste de formalina (uma medida de dor inflamatória contínua) e fez os camundongos preferirem ambientes onde o circuito havia sido ativado, sinalizando alívio do peso emocional da dor. Ao iluminar ramos específicos do caminho, os pesquisadores mostraram que projeções para o tálamo parataenial reduzem tanto a sensibilidade física quanto as respostas de enfrentamento, enquanto projeções para os tálamos mediodorsal e ventromedial afinam principalmente as dimensões emocionais e comportamentais. Juntos, esses resultados revelam um esquema de fiação finamente dividido em que ramos diferentes da mesma população pré‑frontal controlam facetas distintas da experiência da dor.
Afinação química: um impulso colinérgico para alívio da dor
O que controla esses neurônios pré‑frontais de alívio da dor? Experimentos de rastreio descobriram forte entrada de uma região colinérgica no cérebro basal chamada banda diagonal horizontal. Muitas das células que enviam sinais dessa área para neurônios marcados por Foxp2 usam acetilcolina, um mensageiro envolvido em atenção e excitação. Ativar essa projeção colinérgica reduziu a sensibilidade mecânica e os comportamentos de enfrentamento e aliviou a hipersensibilidade inflamatória, embora não tenha alterado claramente o tom emocional negativo da dor. No lado receptor, os neurônios marcados por Foxp2 mostraram enriquecimento para um tipo particular de receptor de acetilcolina, conhecido como receptor nicotínico α4β2. Administrar diretamente um agonista seletivo α4β2 no córtex pré‑frontal medial tornou os camundongos menos sensíveis ao calor e ao toque dolorosos, mesmo em estados inflamatórios crônicos, e aumentou a atividade dos neurônios marcados por Foxp2. Bloquear esses neurônios eliminou o benefício do fármaco, mostrando que esse receptor alivia a dor especificamente ao excitar esse tipo celular. 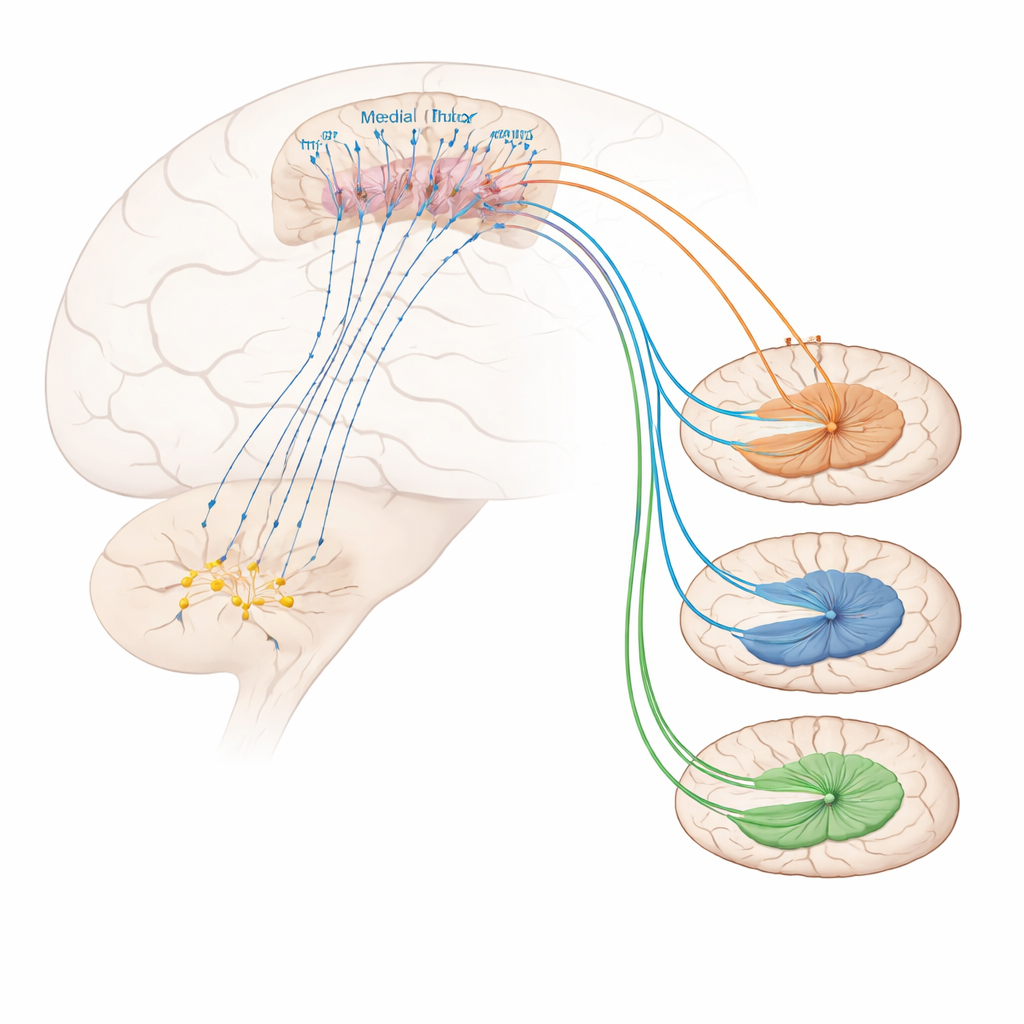
O que isso significa para tratamentos futuros da dor
Em termos práticos, o estudo identifica um caminho preciso em três etapas: uma região colinérgica “iniciadora” no cérebro basal, um conjunto especializado de células de controle no córtex pré‑frontal medial e hubs de retransmissão distintos no tálamo que governam separadamente quão intensa a dor é, quão ruim ela é emocionalmente e como reagimos a ela. A dor parece reduzir a atividade desse circuito; reativá‑lo, seja por estimulação direta ou por direcionamento de seus receptores de acetilcolina, diminui tanto a fisgada quanto o sofrimento da dor inflamatória em camundongos machos. Embora muito trabalho seja necessário para traduzir essas descobertas para humanos e para outras formas de dor crônica, os resultados destacam uma estratégia promissora: em vez de anestesiar toda a sensação, tratamentos futuros podem restaurar ou ajustar os próprios circuitos cerebrais de alívio da dor para uma terapia de longo prazo mais eficaz e possivelmente mais segura.
Citação: Xie, G., Liu, Y., Qi, X. et al. A molecularly defined basalo-prefrontal-thalamic circuit regulates sensory and affective dimensions of pain in male mice. Nat Commun 17, 2134 (2026). https://doi.org/10.1038/s41467-026-69001-2
Palavras-chave: dor crônica, córtex pré‑frontal medial, tálamo, sinalização colinérgica, receptores nicotínicos