Clear Sky Science · pt
Modificação covalente de um ácido glutâmico inspirada na tecnologia HaloTag
Transformando “âncoras” proteicas em alvos de fármaco
Muitos medicamentos modernos contra o câncer atuam prendendo‑se a proteínas dentro de nossas células. Mas algumas das proteínas mais importantes não têm “pegadores” fáceis para as drogas. Este estudo apresenta um truque químico engenhoso, inspirado numa ferramenta de laboratório popular chamada HaloTag, para se ligar a um ponto normalmente de difícil acesso numa proteína que ajuda a controlar sinais de crescimento relevantes para o câncer. O trabalho pode abrir novas vias para fármacos que inativem vias promotoras de tumor de forma mais duradoura.
Por que a maioria dos fármacos covalentes mira no mesmo ponto
Nos últimos anos, os chamados fármacos covalentes direcionados tornaram‑se uma classe promissora de medicamentos. Eles carregam um grupo químico levemente reativo que forma uma ligação permanente a um aminoácido específico de uma proteína, travando o fármaco no lugar. Quase todos esses fármacos miram na cisteína, um aminoácido relativamente raro mas altamente reativo. Em contraste, dois outros aminoácidos, o aspartato e o glutamato, são muito mais comuns e frequentemente cruciais para a forma e função da proteína, mas seus grupos ácidos “carboxilato” são muito menos reativos no ambiente aquoso da célula. Isso os torna difíceis de modificar de forma seletiva, e apenas alguns exemplos bem‑sucedidos de fármacos covalentes direcionados ao glutamato ou ao aspartato existiam antes deste trabalho.
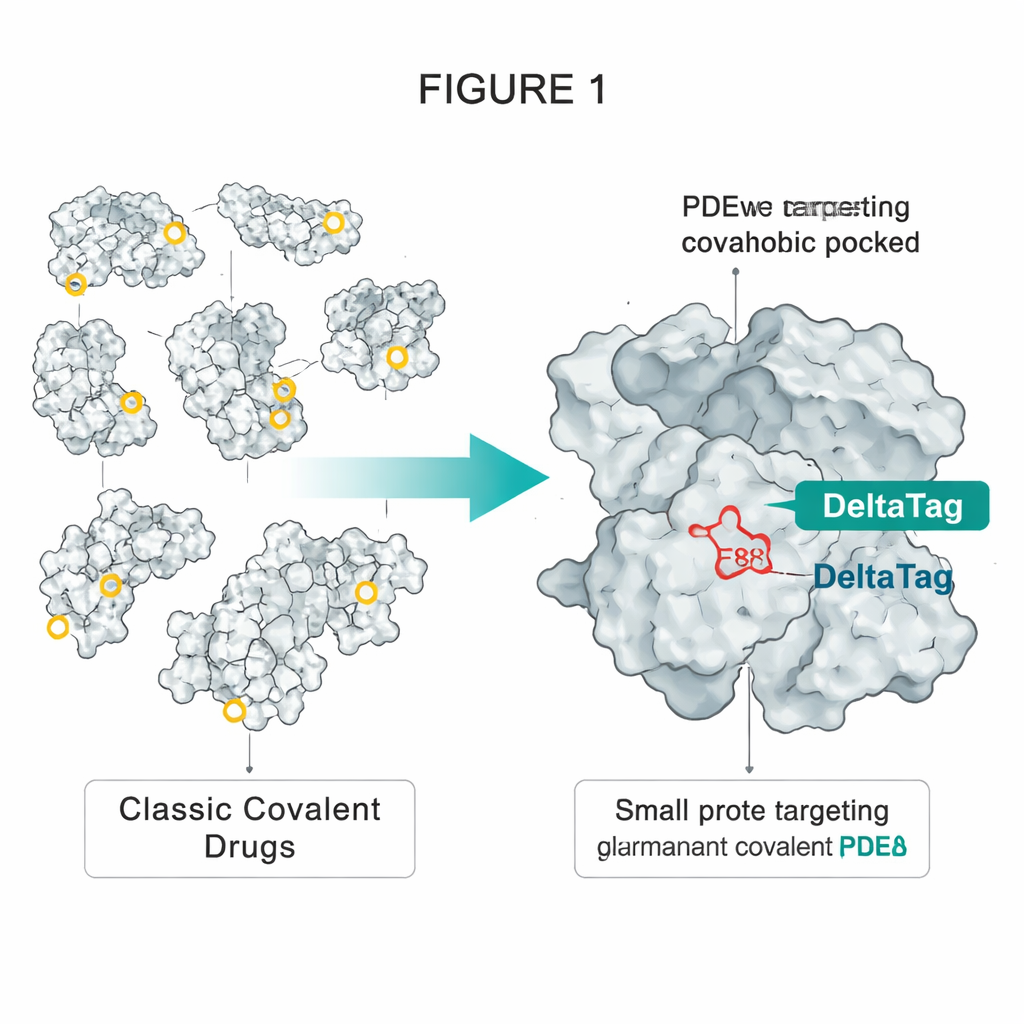
Tomando emprestado um truque da tecnologia HaloTag
Os autores se inspiraram na HaloTag, uma proteína de engenharia amplamente usada que pode ser marcada permanentemente com corantes fluorescentes. Na HaloTag, um aspartato especialmente posicionado no fundo de um bolso hidrofóbico reage com uma cadeia simples de cloroalcano do corante, formando uma ligação éster estável. A equipe observou que outra proteína, PDEδ, possui um bolso hidrofóbico semelhante que contém um único glutamato acessível, chamado E88. PDEδ transporta proteínas de sinalização modificadas por lipídios, como a pequena GTPase Rheb, por dentro da célula, ajudando‑as a alcançar membranas onde complexos promotores de crescimento como o mTORC1 são ativados. Inibidores não covalentes anteriores de PDEδ podiam bloquear esse transporte, mas seu efeito era limitado porque outra proteína, Arl2, pode desalojá‑los do bolso com o tempo.
Projetando o DeltaTag para se prender ao glutamato
Para superar esse problema de “expulsão”, os pesquisadores partiram de um bloqueador conhecido de alta afinidade para PDEδ e reengenheiraram uma de suas cadeias laterais para carregar um “warhead” haloalcano semelhante aos usados em ligantes da HaloTag. Através de várias rodadas de ajustes estruturais guiados por estruturas cristalográficas de proteínas, chegaram a um composto chamado DeltaTag. Sua característica chave é um grupo fenetil brometo posicionado de modo que, uma vez que a molécula se acomode no bolso lipídico de PDEδ, o brometo fique precisamente alinhado para reagir com E88. Medidas biofísicas e estruturas de raios‑X de alta resolução confirmaram que o DeltaTag forma uma ligação éster covalente especificamente com esse glutamato e que outros aminoácidos potencialmente mais reativos em PDEδ permanecem intocados. O composto é reativo o suficiente para marcar a proteína de forma eficiente, mas estável o bastante em água e na presença do principal antioxidante à base de enxofre da célula, o glutationa, para evitar danos indiscriminados em larga escala.
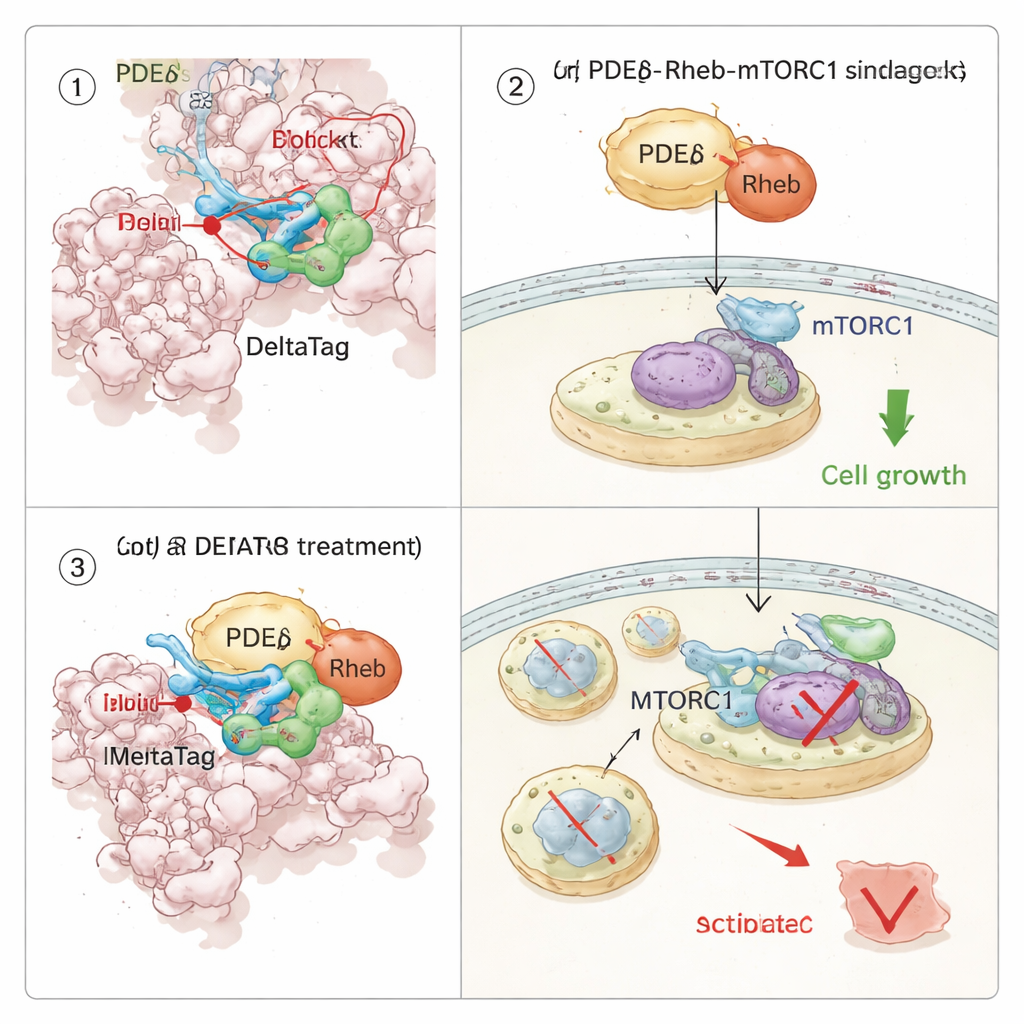
Reprogramando uma via de crescimento dentro de células cancerígenas
Como PDEδ auxilia Rheb, e Rheb por sua vez ativa a via de crescimento mTORC1, a equipe investigou como a inibição covalente de PDEδ reverberaria pela sinalização celular. Usando perfilamento de estabilidade térmica em milhares de proteínas, demonstraram que o DeltaTag se liga seletivamente a PDEδ em extratos celulares e perturba proteínas ligadas ao eixo Rheb–mTOR. Em experimentos de imageamento em células vivas, o DeltaTag fez com que Rheb se relocasse de um padrão difuso no interior celular para membranas internas mais agrupadas, consistente com a perturbação do seu transporte normal. Fosfoproteômica global e Western blots focados revelaram que a atividade do mTORC1, acompanhada pela fosforilação de uma proteína ribossomal chamada S6, diminuiu ao longo do tempo, enquanto sinais compensatórios em vias relacionadas aumentaram. Importante, em várias linhagens de células humanas de câncer dirigidas por KRAS mutante e dependentes de forte sinalização do mTOR, o DeltaTag retardou a proliferação celular de forma mais eficaz do que inibidores reversíveis estreitamente relacionados, e seu impacto foi menor em células sem PDEδ, apoiando que sua ação principal é on‑target.
Abrindo uma porta para novos tipos de alvos de fármacos
Este trabalho mostra que é possível construir pequenas moléculas que formam uma ligação permanente e altamente específica a um único glutamato enterrado num bolso hidrofóbico de uma proteína, usando uma química de haloalcano relativamente simples emprestada da HaloTag. No sistema modelo PDEδ, essa ligação covalente produz um bloqueio mais duradouro de uma via de crescimento relevante para o câncer do que fármacos reversíveis anteriores. Mais amplamente, a mesma lógica de design poderia ser aplicada a outras proteínas que têm cavidades hidrofóbicas mas carecem dos usuais aminoácidos “reativos”, desde que apresentem um glutamato ou aspartato estrategicamente posicionado. Com otimizações adicionais, inibidores covalentes direcionados ao glutamato como o DeltaTag podem se tornar ferramentas úteis para a biologia química e, em última instância, candidatos para novas terapias que enfrentem proteínas atualmente difíceis de medicar.
Citação: Zhang, R., Liu, J., Gasper, R. et al. Covalent modification of a glutamic acid inspired by HaloTag technology. Nat Commun 17, 1257 (2026). https://doi.org/10.1038/s41467-026-68999-9
Palavras-chave: inibidores covalentes, direcionamento de glutamato, PDEδ, sinalização mTOR, design de fármacos contra o câncer