Clear Sky Science · pt
Engenharia de células sintéticas com domínios intramembrana possuindo assimetrias bicamada distintas
Por que pequenas bolhas sintéticas importam
Cada célula viva é envolta por uma membrana que funciona como uma pele inteligente e flexível. Essa pele não é uniforme: o lado interno e o externo, e até diferentes manchas ao longo de sua superfície, podem ter composições e formas muito distintas. Essas diferenças ajudam as células a enviar sinais, atrair proteínas e até se dividir. Ainda assim, tem sido notoriamente difícil construir membranas modelo simples e controláveis que capturem essa complexidade. Este estudo apresenta uma forma prática de fabricar “células sintéticas” do tamanho celular cujas membranas são assimétricas em ambas as faces e lateralmente padronizadas em regiões distintas — abrindo caminho para imitadores de células mais realistas e para estudar como padrões de membrana impulsionam brotamento e divisão. 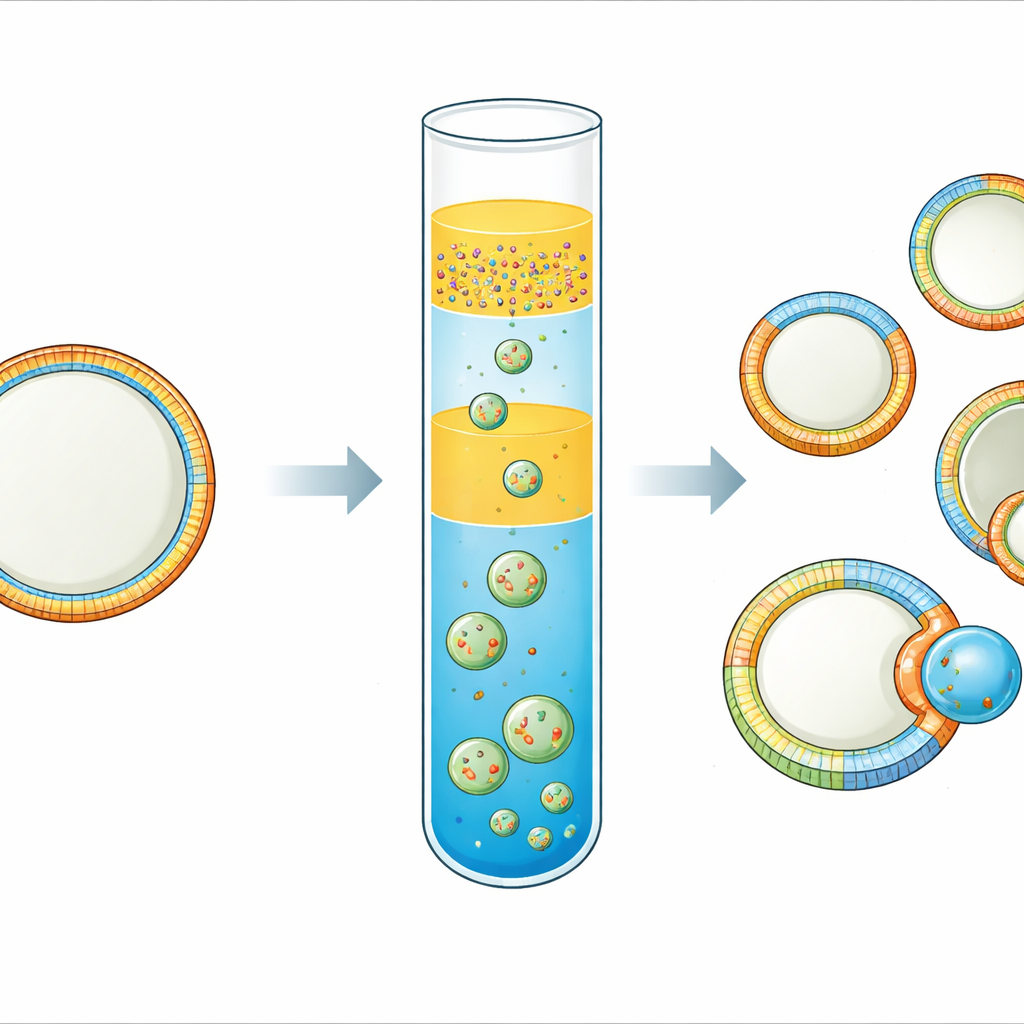
Construindo melhores imitadores de células
Membranas celulares reais são assimétricas: o lado interno é rico em lipídios carregados negativamente que recrutam proteínas de sinalização, enquanto o lado externo carrega lipídios diferentes que mediam o reconhecimento célula–célula. Muitos métodos de laboratório conseguem gerar vesículas gigantes — esferas ocos de moléculas semelhantes a gorduras — mas suas duas monocamadas geralmente acabam iguais, e o interior é difícil de acessar. Outras abordagens que criam assimetria frequentemente exigem dispositivos complexos, lipídios especiais ou deixam as vesículas presas a uma superfície. Os autores propuseram criar vesículas independentes e do tamanho celular que combinassem alto encapsulamento de biomoléculas com uma assimetria robusta e ajustável, mais parecida com a de uma célula viva.
Uma receita em três camadas para membranas assimétricas
A equipe refinou uma técnica de “emulsão invertida”, na qual minúsculas gotas de água cobertas por lipídios são forçadas através de uma interface óleo–água para formar vesículas. A inovação-chave é uma configuração com três camadas de óleo. Na camada inferior fica um óleo contendo os lipídios destinados à monocamada externa da membrana. Acima dele, colocam um óleo espaçador fino sem lipídios, e por cima disso uma emulsão de gotas de água rodeadas por um segundo óleo que carrega os lipídios para a monocamada interna. Durante uma breve etapa de centrifugação, as gotas atravessam o espaçador e a camada inferior, adquirindo uma segunda cobertura lipídica e fechando-se em vesículas. Escolher dois óleos de densidades diferentes e incluir o espaçador limita fortemente a mistura entre os reservatórios de lipídios, de modo que as monocamadas interna e externa mantêm composições distintas.
Testando se os dois lados permanecem diferentes
Para verificar que as monocamadas eram realmente distintas, os pesquisadores usaram leituras químicas e baseadas em proteínas. Em um conjunto de testes, eles adicionaram um lipídio fluorescente a apenas uma monocamada e então expuseram as vesículas a um químico na solução externa que apaga a fluorescência, mas não atravessa a membrana. Quando o lipídio fluorescente estava no lado externo, o sinal caiu quase completamente; quando estava no lado interno, praticamente não mudou, mostrando que a maioria dos lipídios marcados ficou onde era esperado. Em um segundo conjunto de experimentos, colocaram lipídios que se ligam a proteínas específicas — como lipídios marcados com biotina para estreptavidina ou grupos de cabeça especiais para proteína fluorescente verde com etiqueta His — em apenas uma monocamada. Proteínas adicionadas ao compartimento oposto (dentro ou fora) ligaram-se apenas quando o lipídio correspondente estava no mesmo lado da membrana, confirmando tanto a forte assimetria quanto a preservação da função protéica.
Criando “rafts” e observando o brotamento das membranas
Membranas celulares reais também contêm “rafts”: pequenas manchas enriquecidas em certos lipídios como colesterol e esfingomielina, que podem agrupar proteínas e influenciar a forma. Conseguir essa separação de fases com o método de emulsão invertida havia sido difícil porque o colesterol tendia a permanecer dissolvido no óleo em vez de entrar na membrana. Ao usar esqualeno na camada de óleo inferior, que retém o colesterol menos fortemente do que o óleo mineral padrão, os autores puderam formar de maneira reprodutível vesículas cujas membranas se dividiam em regiões líquidas-ordenadas e líquidas-desordenadas coexistentes, muito parecidas com os rafts. Em seguida combinaram esse padrão lateral com a assimetria de monocamadas: um domínio levava um ligante na monocamada interna que ligava estreptavidina no interior, enquanto outro domínio carregava glicolipídios que ligavam toxina da cólera no exterior. 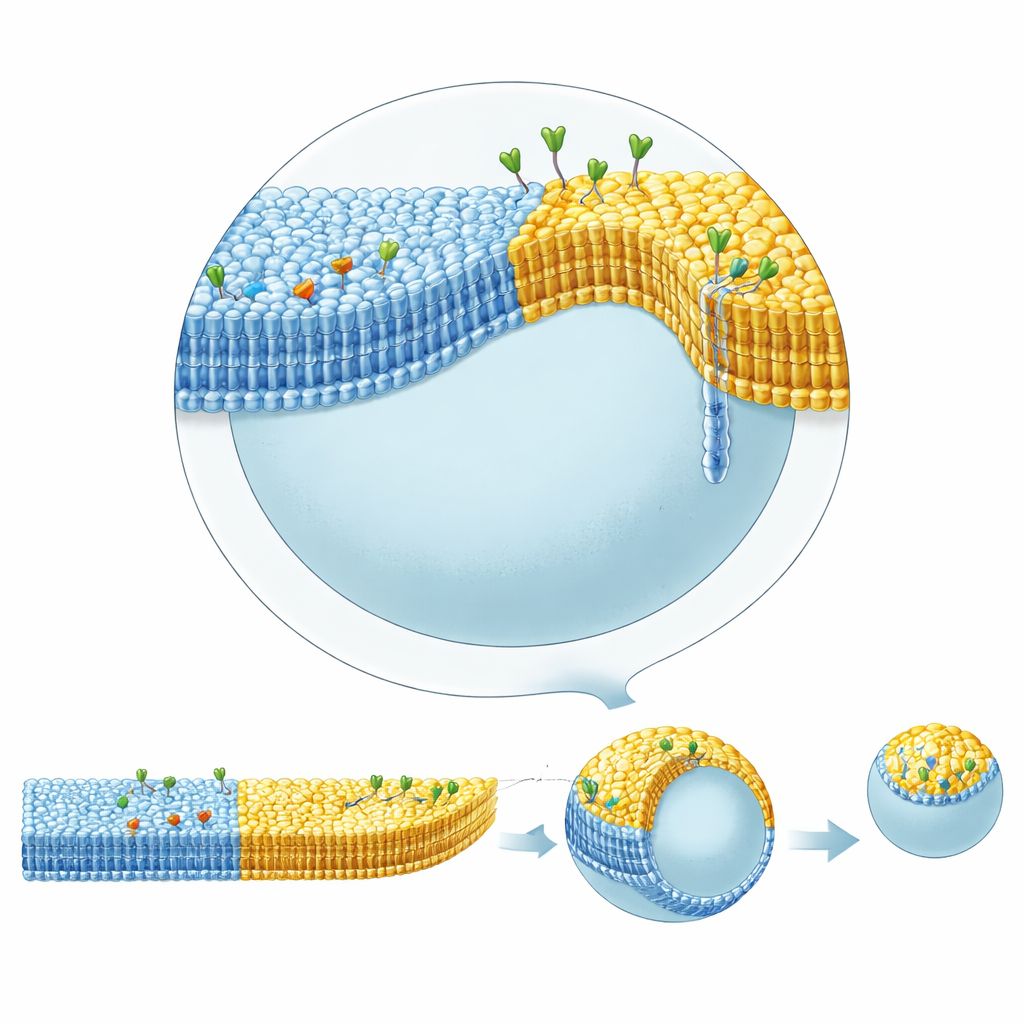
Como proteínas e padrões dirigem mudanças de forma
Essas vesículas complexas exibiram dinâmicas de forma impressionantes. Quando a toxina da cólera se ligou aos glicolipídios no domínio ordenado do lado externo, esse domínio protuberou para fora formando um broto curvo conectado por um pescoço estreito e, sob leve desinflação osmótica, pôde se destacar completamente como uma vesícula filha. Esse brotamento não exigiu moléculas portadoras de energia como ATP nem maquinarias especializadas de divisão; surgiu puramente da interação entre composição lipídica, limites de domínio e ligação proteica assimétrica. Ao aumentar a quantidade de estreptavidina ligada no lado interno do domínio desordenado, a equipe pôde neutralizar a curvatura externa do domínio ordenado e gradualmente restaurar uma forma mais esférica. Análises geométricas detalhadas dos contornos das vesículas mostraram que a curvatura da membrana salta na fronteira entre domínios, e que os pescoços estreitos que se fecham durante o brotamento devem suportar forças de pelo menos dezenas de piconewtons — quantificando como a estrutura de domínios e o aglomeramento de proteínas podem esculpir mecanicamente as membranas.
O que isso significa para futuras células sintéticas
Em termos práticos, os autores desenvolveram uma receita para fabricar bolhas moles do tamanho celular cujas peles são padronizadas e com duas faces, de forma muito semelhante às membranas celulares reais. Porque o método é relativamente simples, funciona com muitos lipídios diferentes e permite que proteínas e outras grandes moléculas sejam aprisionadas no interior, abre caminho para construir células artificiais mais parecidas com as reais a partir do zero. Essas células sintéticas podem ajudar cientistas a dissecar como padrões de membrana controlam sinalização, tráfego e divisão, e podem eventualmente ser aproveitadas como transportadores inteligentes de fármacos que mudam de forma ou se dividem sob comando dentro do corpo.
Citação: Yandrapalli, N., Seemann, T., Lipowsky, R. et al. Engineering synthetic cells with intramembrane domains possessing distinct bilayer asymmetries. Nat Commun 17, 2620 (2026). https://doi.org/10.1038/s41467-026-68997-x
Palavras-chave: células sintéticas, membranas lipídicas, assimetria de membrana, separação de fases, brotamento de membrana