Clear Sky Science · pt
Plataforma de nanodisco com glicoproteína viral para análise de vacinas
Transformando proteínas virais em alvos mensuráveis
Vacinas modernas dependem cada vez mais de versões precisamente projetadas das proteínas que recobrem a superfície dos vírus. Essas proteínas são os principais alvos de anticorpos protetores, mas são notoriamente difíceis de estudar em sua forma natural, ligada à membrana. Este artigo descreve uma nova plataforma laboratorial que insere proteínas de superfície virais em comprimento completo em pequenas partículas lipídicas planas chamadas nanodiscos. Essa configuração permite aos cientistas medir o quanto candidatos a vacina imitam vírus reais, como os anticorpos se ligam a eles e como redesenhar essas vacinas para obter melhor proteção.
Por que recriar a superfície viral importa
Muitas das proteínas virais mais importantes ficam ancoradas em uma membrana lipídica, exatamente como em um vírus verdadeiro. Abordagens laboratoriais tradicionais costumam remover a porção de membrana para facilitar a produção e purificação dessas proteínas em solução. Mas esse atalho elimina regiões próximas à membrana que abrigam alvos de anticorpos especialmente valiosos, incluindo um segmento do HIV conhecido como região externa proximal à membrana (MPER). Essas regiões próximas à membrana podem ter aparência e comportamento diferentes quando não estão inseridas em um ambiente lipídico realista, o que significa que fragmentos solúveis da proteína podem fornecer uma imagem incompleta ou enganosa de como uma vacina se comportará no organismo.
Construindo uma plataforma de nanodisco versátil
Os pesquisadores criaram um fluxo de trabalho enxuto de cinco dias para colher proteínas de superfície virais em comprimento completo de células humanas, manter seus segmentos transmembranares naturais intactos e reinseri-los em um disco lipídico controlado. Primeiro eles expressaram glicoproteínas de HIV e Ebola, engenheiradas, na superfície celular, depois as extrairam suavemente com detergente e as capturaram em uma matriz de purificação. Enquanto as proteínas ainda estavam ligadas, misturaram lipídios definidos e uma proteína andaime em forma de cinturão que se auto-assembla em uma pequena membrana em formato de disco. À medida que o detergente foi removido, as proteínas virais acomodaram-se nesses nanodiscos. As preparações resultantes foram altamente puras, estáveis por meses na geladeira e apresentaram revestimentos glicanos (açúcares) muito semelhantes aos encontrados nos espigões virais nativos. 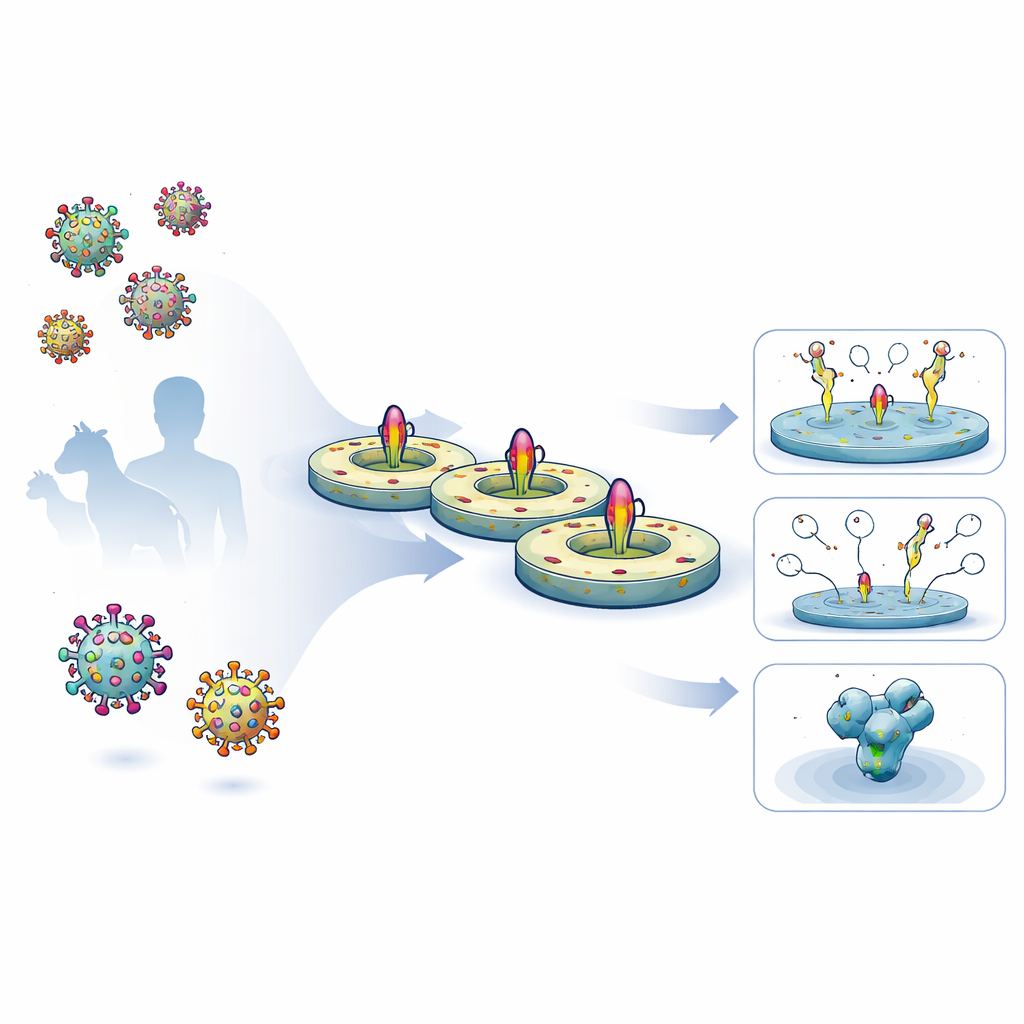
Lendo a ligação de anticorpos e respostas imunes
Com proteínas incorporadas em nanodiscos em mãos, a equipe testou quão bem diferentes anticorpos podiam se ligar usando vários arranjos de ressonância plasmônica de superfície (SPR), uma técnica que acompanha a ligação em tempo real. Usando nanodiscos de HIV projetados para expor a região MPER, mostraram que um anticorpo amplamente neutralizante e potente chamado 10E8 se ligou cerca de 70 vezes mais fortemente ao constructo projetado do que a um desenho anterior, principalmente porque a dissociação foi muito mais lenta. Mutações de controle que desestruturaram a região MPER eliminaram completamente a ligação do 10E8, confirmando que a plataforma pode relatar com sensibilidade como mudanças de projeto afetam epítopos chave. Os mesmos nanodiscos funcionaram como sondas em citometria de fluxo, onde ajudaram a isolar células B de camundongos e macacos imunizados que reconheciam a forma transmembrana completa da proteína do HIV, incluindo partes ausentes em sondas solúveis padrão. 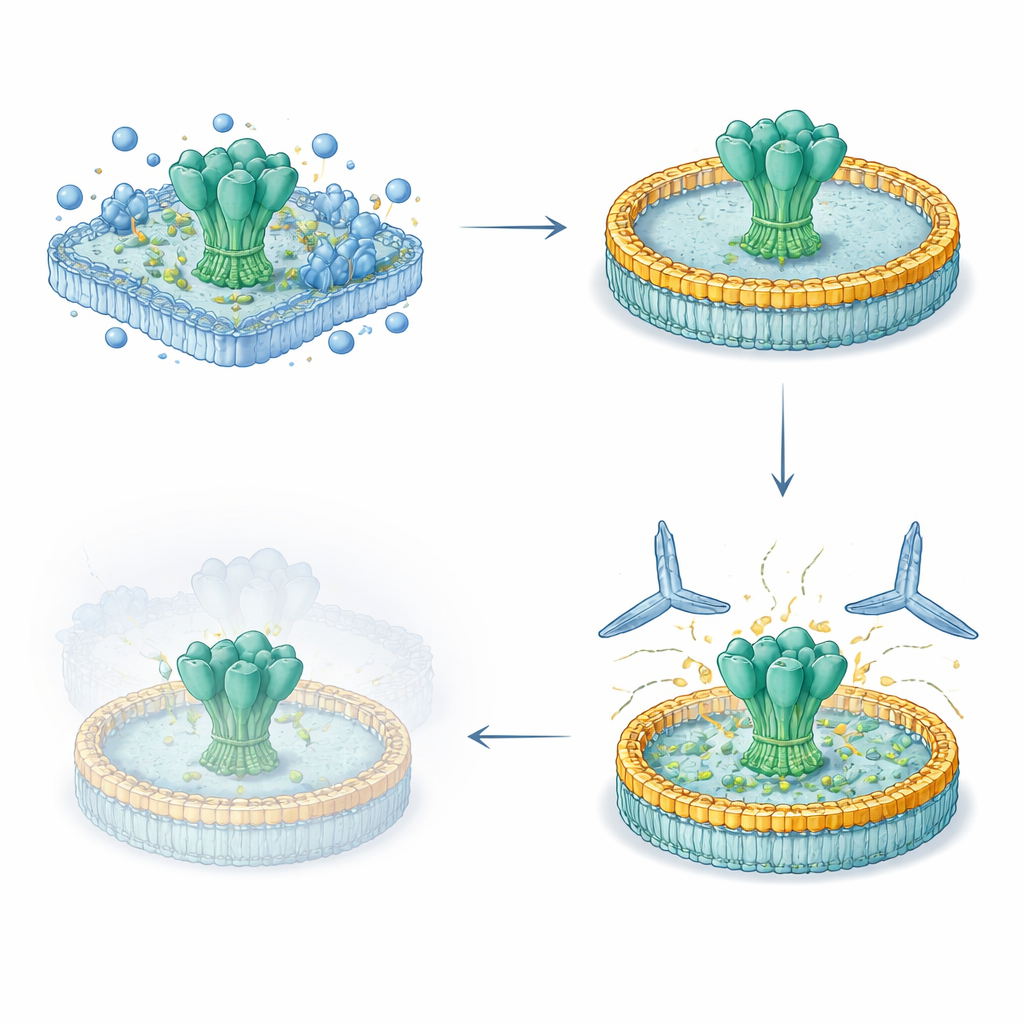
Vendo o alvo completo em detalhe atômico
Para entender exatamente como os anticorpos reconhecem a MPER em seu contexto nativo, os autores usaram microscopia eletrônica criogênica para imagem dos nanodiscos de HIV ligados a três anticorpos amplamente neutralizantes diferentes. Eles obtiveram uma estrutura a 3,5 angstrons de um anticorpo, 10E8, engajando o segmento MPER enquanto o restante do espigão do HIV permanecia ancorado no disco lipídico. Isso revelou uma rede contínua de contatos entre 10E8 e tanto a MPER quanto porções adjacentes da proteína externa, incluindo um bolso profundo na junção entre duas subunidades. Ao comparar essa estrutura com imagens anteriores do 10E8 ligado apenas a um peptídeo curto, a equipe mostrou que o ambiente de membrana e o espigão em comprimento completo permitem contatos extras e movimentos dinâmicos que eram invisíveis em modelos mais simples, e que aminoácidos específicos no vírus influenciam fortemente quão facilmente o 10E8 pode neutralizá-lo.
Usos amplos para vacinas mais inteligentes
Na prática, essa plataforma de nanodisco dá aos projetistas de vacinas uma forma de avaliar candidatos transmembranares com as mesmas poderosas ferramentas analíticas antes reservadas a fragmentos proteicos solúveis. Ela funciona em diferentes vírus, suporta medições detalhadas de ligação, permite a triagem e o sequenciamento precisos de células B induzidas pela vacina e fornece estruturas de alta resolução que capturam epítopos realistas próximos à membrana. Para um leitor leigo, a conclusão é que os cientistas agora dispõem de um campo de testes mais realista para proteínas de superfície viral, capaz de mostrar quais desenhos de vacina realmente se parecem e se comportam como o vírus real e como ajustá-los para respostas de anticorpos mais fortes e amplas. Isso deve acelerar o desenvolvimento de vacinas de próxima geração não apenas para o HIV, mas para muitos outros vírus envelopados.
Citação: Rantalainen, K., Liguori, A., Ozorowski, G. et al. Virus glycoprotein nanodisc platform for vaccine analytics. Nat Commun 17, 2561 (2026). https://doi.org/10.1038/s41467-026-68985-1
Palavras-chave: nanodiscos, vacinas contra HIV, glicoproteínas virais, anticorpos amplamente neutralizantes, crio-ME