Clear Sky Science · pt
Mapeamento por radicais em sangue total de mamíferos
Vendo proteínas em ação no sangue real
As proteínas em nosso sangue mudam de forma constantemente enquanto desempenham funções vitais, como combater infecções, transportar ferro e responder a doenças. Até agora, a maioria das ferramentas para examinar essas pequenas alterações de forma funcionava apenas em amostras laboratoriais simplificadas ou em células isoladas. Este estudo mostra, pela primeira vez, que é possível ler as formas das proteínas diretamente em sangue mamífero intacto, abrindo caminho para observar processos patológicos como realmente ocorrem no organismo.
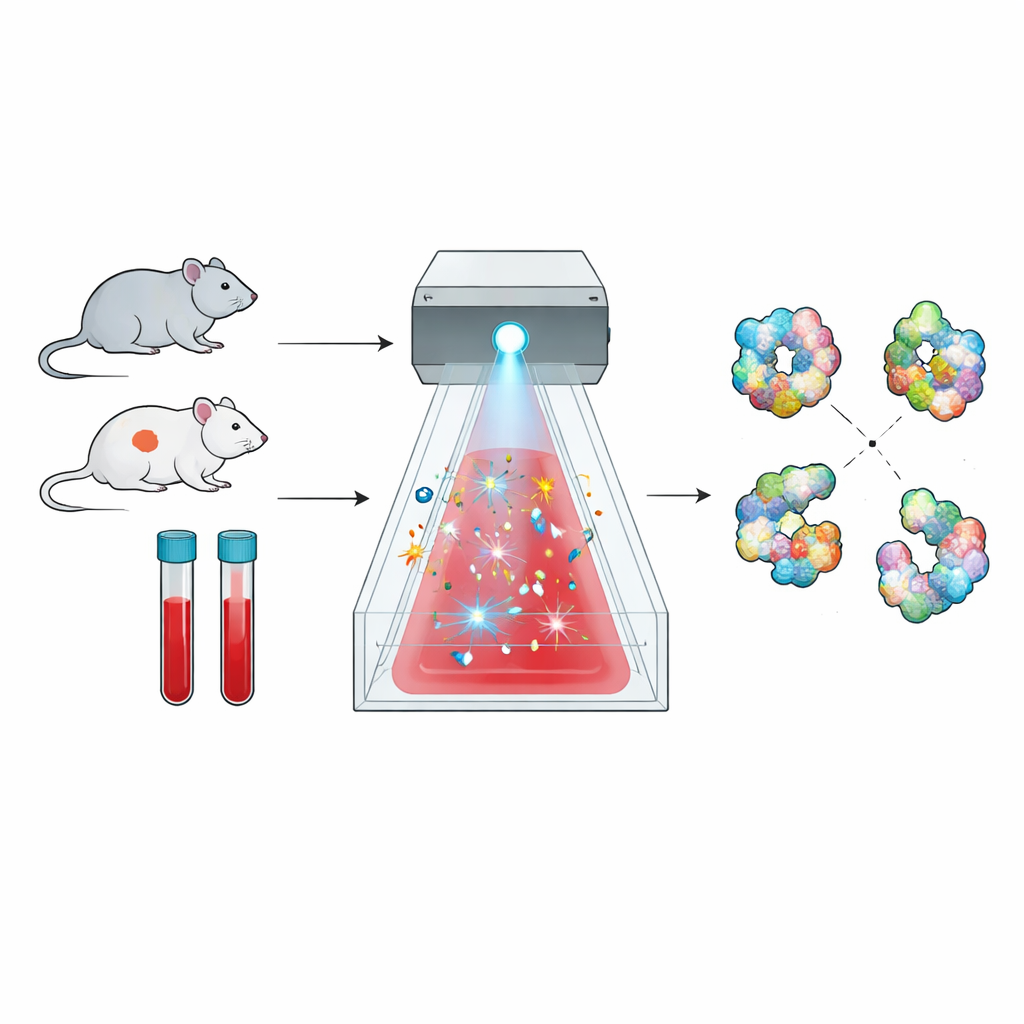
Uma nova maneira de mapear formas de proteínas
Proteínas não são peças rígidas; elas se dobram em formas tridimensionais complexas, e essas formas determinam o que podem fazer. O método explorado aqui, chamado footprinting por radicais, tira proveito desse fato. Rajadas breves de moléculas altamente reativas funcionam como um “flash” químico, atingindo apenas as partes da proteína expostas ao líquido ao redor. Depois, espectrometria de massa é usada para contar onde esses ataques químicos ocorreram, produzindo uma espécie de mapa de superfície, ou impressão digital, da forma de cada proteína. Mudanças nessa impressão entre estados saudáveis e doentes revelam deslocamentos sutis na dobra da proteína ou em suas interações com parceiros.
Fazendo a técnica funcionar em sangue total
Aplicar essa abordagem diretamente ao sangue foi um desafio de longa data. O sangue absorve fortemente luz ultravioleta e está repleto de enzimas, como catalase, que destroem rapidamente os químicos geradores de radicais usuais antes que possam marcar as proteínas. Os pesquisadores solucionaram isso trocando para persulfato de sódio, que pode ser dividido por um flash brilhante de luz de banda larga em potentes radicais sulfato. Usando um sistema comercial chamado FOX, demonstraram que o persulfato pode ser ativado de forma confiável e que uma leitura de dosimetria incorporada pode acompanhar quantos radicais são produzidos, permitindo controle preciso da “exposição” que cada amostra recebe.
Protegendo as células enquanto capturam detalhes
Como o método se destina a estudar proteínas em algo próximo ao seu estado natural, era crucial que as próprias células sanguíneas não fossem destruídas. Testes em sangue de camundongo mostraram que a adição de persulfato concentrado causou apenas alterações menores e reversíveis na forma dos glóbulos vermelhos e menos de dois por cento de ruptura celular, semelhante a soluções salinas simples. A equipe também desenvolveu uma mistura de “quenche” aprimorada que absorve rapidamente as espécies reativas residuais, prevenindo danos espúrios de reações secundárias mais lentas após o flash. Em conjunto, esses aprimoramentos permitiram rotular proteínas em sangue de camundongo intacto preservando a estrutura celular e mantendo o ruído de fundo muito baixo.
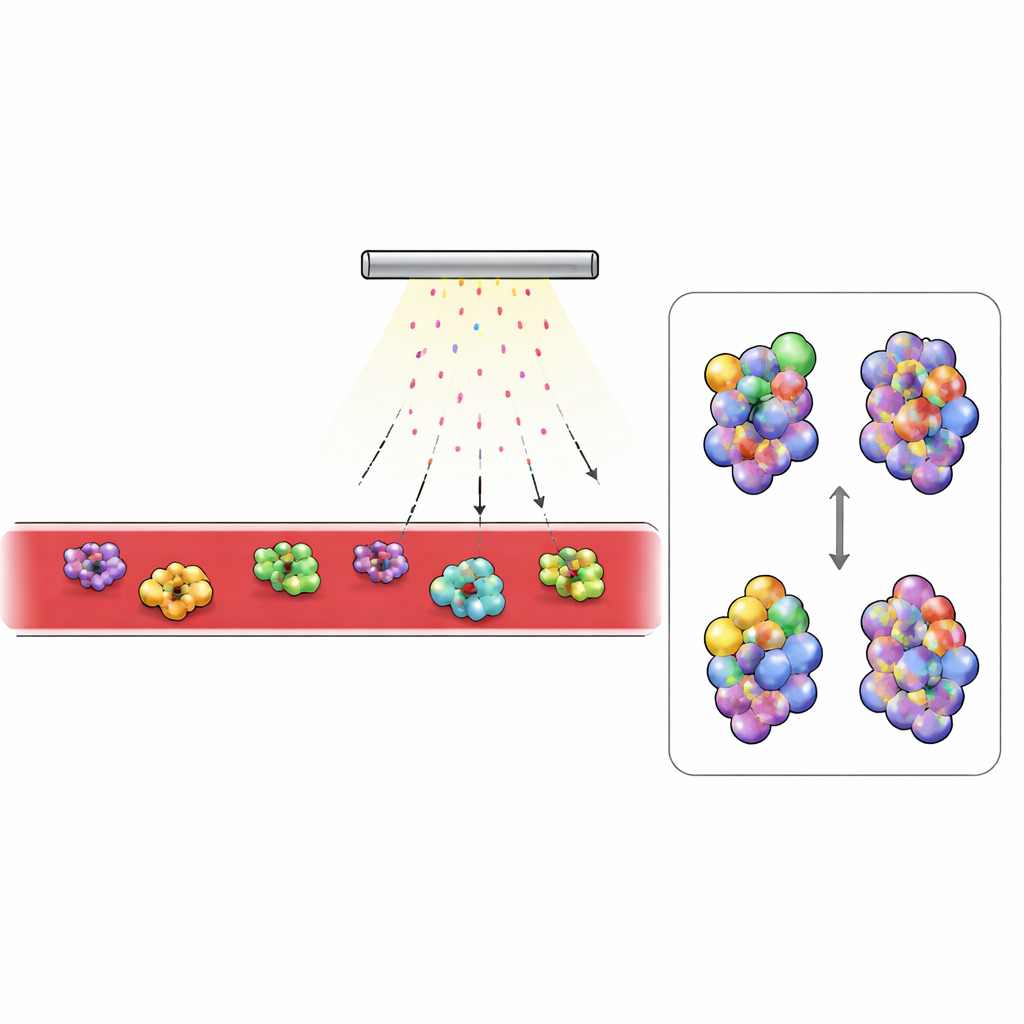
O que muda no sangue diabético
Com essa plataforma em mãos, os pesquisadores compararam sangue de camundongos saudáveis e de um modelo comum de diabetes tipo 2. Eles se concentraram nas proteínas mais abundantes detectadas, especialmente aquelas que circulam fora das células. Proteínas extracelulares mostraram marcação muito mais intensa do que as intracelulares, refletindo a penetração limitada do persulfato para o interior celular. Duas proteínas sanguíneas se destacaram: o complemento C3, um componente-chave do sistema imune, e a transferrina, que transporta ferro. Em camundongos diabéticos, regiões de C3 que ficam enterradas quando a proteína muda para sua forma ativa foram menos marcadas, enquanto regiões normalmente escondidas ficaram mais expostas. Esse padrão corresponde à mudança estrutural conhecida quando C3 é convertido em seu fragmento ativo, C3b, e testes sanguíneos confirmaram que os animais diabéticos tinham muito mais C3 ativado. Na transferrina, áreas próximas ao sítio de ligação do ferro estavam mais protegidas no sangue diabético, consistente com a proteína carregando mais ferro. Medições independentes mostraram maior ferro sérico e uma fração maior de transferrina saturada com ferro em camundongos diabéticos.
Por que isso importa para saúde e medicina
Para um não especialista, a mensagem essencial é que os autores criaram uma maneira de “sentir” as formas de muitas proteínas de uma só vez diretamente no sangue real, e então usar esses padrões de forma para inferir como a doença está alterando a química do corpo. Nesse modelo de camundongo de diabetes tipo 2, o método revela sinalização do complemento hiperativa e maior carregamento de ferro na transferrina — mudanças que testes clássicos podem não detectar ou ver apenas indiretamente. Como a abordagem funciona com pequenas amostras de sangue e usa uma fonte de luz padronizada, ela pode eventualmente ajudar a identificar sinais estruturais precoces de doença, acompanhar como medicamentos biológicos se comportam na corrente sanguínea e orientar o desenho de tratamentos mais eficazes.
Citação: Zhao, M., Tobin, L., Misra, S.K. et al. Radical footprinting in mammalian whole blood. Nat Commun 17, 2470 (2026). https://doi.org/10.1038/s41467-026-68982-4
Palavras-chave: proteômica estrutural, proteínas do sangue, diabetes tipo 2, sistema complemento, metabolismo do ferro