Clear Sky Science · pt
Variações no terminal C das proteínas afetam a proteostase
Como a extremidade das proteínas molda a saúde
Cada proteína em nossas células termina com uma pequena “cauda” de apenas alguns blocos construtores. Essas caudas podem parecer um detalhe, mas este estudo revela que elas silenciosamente decidem quais proteínas persistem e quais são rapidamente removidas. Como os níveis de proteínas estão na raiz do câncer, de distúrbios genéticos e da resposta celular ao estresse, compreender essas caudas oferece novas maneiras de avaliar o risco de doenças e até projetar tratamentos futuros.
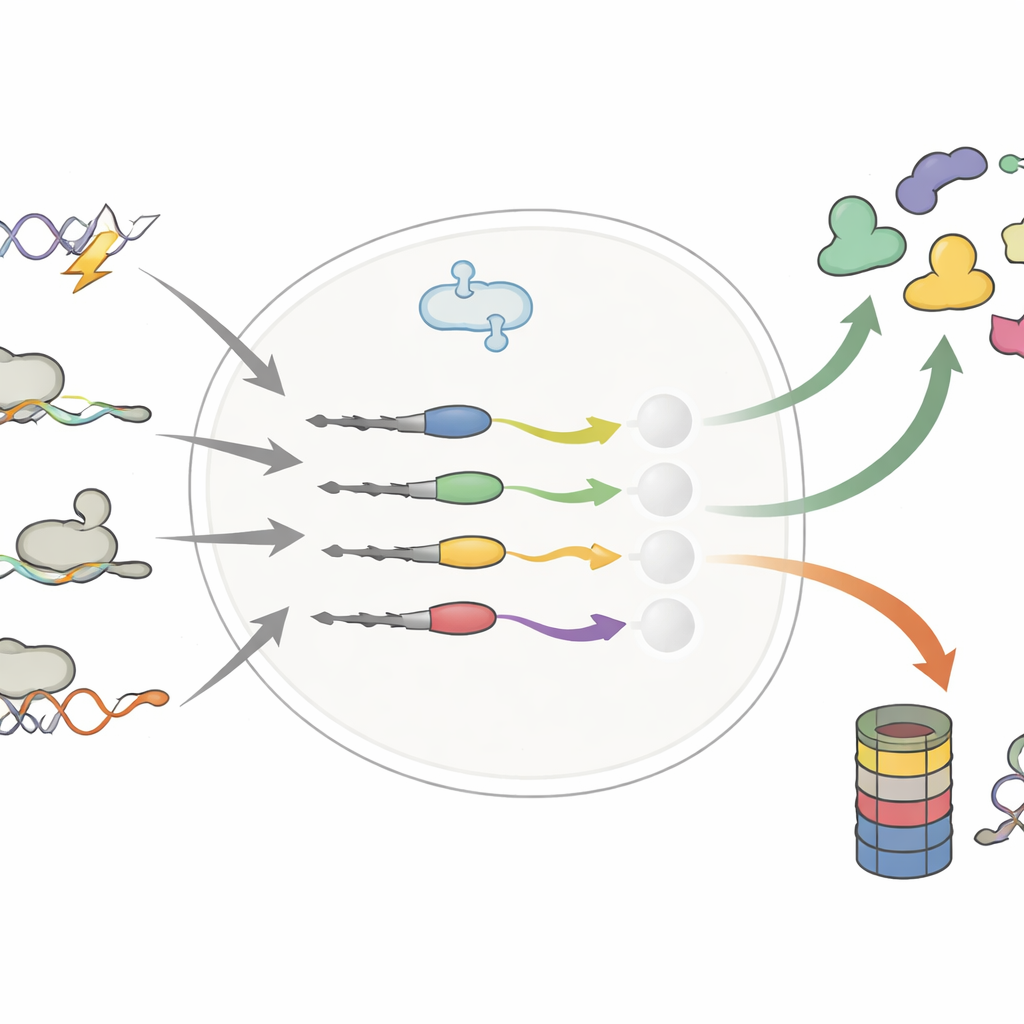
Pequenas mudanças na cauda da proteína, grandes mudanças na vida útil
Os autores concentraram-se na extremidade das proteínas — o terminal C — onde até alguns blocos extras ou trocados podem aparecer por mutações no DNA, splicing alternativo do RNA ou ribossomos lendo além do sinal normal de parada. Trabalhos anteriores sugeriam que tais caudas “errôneas” atuam principalmente como marcas de descarte, enviando proteínas defeituosas para o triturador da célula. Ao comparar sistematicamente milhares de caudas normais e alteradas, este estudo derruba essa visão simplista. A equipe mostra que caudas alteradas podem tanto encurtar quanto prolongar a vida de uma proteína, às vezes estabilizando dirigidores de câncer ou desestabilizando bloqueadores de tumor.
Quando erros genéticos ajudam ou prejudicam proteínas
Uma fonte importante de alterações nas caudas são as mutações nonstop, que apagam um sinal de parada normal para que o ribossomo continue por um trecho de RNA que normalmente fica silencioso. Os pesquisadores testaram mais de 3.000 variantes nonstop ligadas a doenças usando um repórter de dupla cor que mede o quanto cada cauda protege ou enfraquece uma proteína-modelo. Em média, as caudas mutantes ainda tornaram as proteínas menos estáveis que suas contrapartes normais, mas uma fração substancial fez o oposto: aproximadamente uma em cada dez mutações nonstop estabilizou proteínas, enquanto quase um terço as desestabilizou. Essas variações afetaram oncoproteínas e supressores de tumor bem conhecidos, o que implica que mutações que pareciam sutis podem, de fato, inclinar o equilíbrio entre crescimento e morte celular.
Variedade embutida por splicing e readthrough
Nem todas as diferenças de cauda são acidentes. Nossos genes rotineiramente produzem múltiplas versões proteicas por splicing alternativo e por readthrough programado de códon de parada. Ao explorar catálogos de genes humanos, os autores descobriram que quase dois terços dos genes produzem proteínas com mais de um desenho de cauda, e muitas diferem apenas nos últimos poucos blocos construtores. Testar exemplos selecionados mostrou que essas versões quase idênticas frequentemente têm meias-vidas claramente diferentes. Algumas caudas geradas por readthrough tornaram proteínas mais estáveis, outras menos. Isso sugere que as células usam deliberadamente a variação de cauda como um botão de ajuste fino, regulando quanto tempo formas proteicas específicas persistem em diferentes tecidos ou condições.
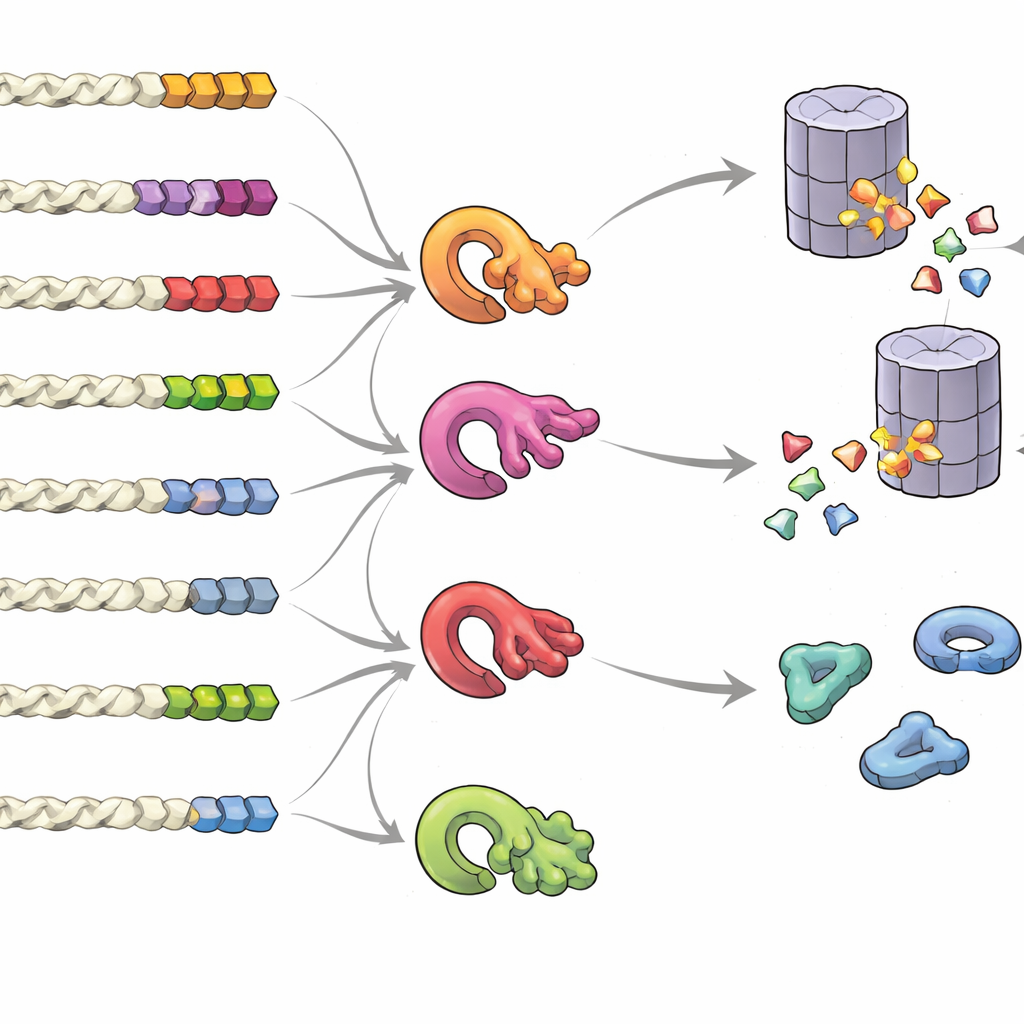
O que faz uma cauda ser sinal de “mantenha-me” ou “jogue-me fora”
Para entender quais características de uma cauda influenciam o destino da proteína, a equipe criou bibliotecas de caudas aleatórias e mediu seu impacto em larga escala. Eles descobriram que não existe apenas um “motivo” fixo, mas sim a composição geral, a posição e o agrupamento de certos blocos construtores que importam. Caudas ricas em componentes pequenos ou apolares, ou nos mais raros cisteína e triptofano, tenderam a atrair degradação, especialmente quando esses resíduos se agrupavam. Em contraste, caudas enriquecidas em componentes ácidos favoreceram a estabilidade. Ao olhar entre muitas espécies, as caudas proteicas normais mostraram sinais claros de pressão evolutiva para evitar padrões arriscados, enquanto caudas geradas por readthrough ou mudanças de quadro, propensas a erros, eram tendenciosas para composições desestabilizadoras. O grupo também descobriu que múltiplas enzimas de controle de qualidade — diferentes ligases de ubiquitina — se especializam em reconhecer distintos padrões hidrofóbicos nas caudas, formando uma rede intrincada que decide quais proteínas são destruídas.
Por que isso importa para a medicina e a biotecnologia
O trabalho redefine as caudas proteicas de pontos finais passivos para reguladores ativos da abundância proteica. Para um leitor leigo, isso significa que muitas doenças podem surgir não apenas de proteínas quebradas, mas também de mudanças sutis em quanto tempo as proteínas permanecem, conduzidas por pequenas diferenças em suas extremidades. Também serve de alerta de que terapias que promovem deliberadamente o readthrough de sinais de parada, usadas para tratar certos distúrbios genéticos, podem alterar inadvertidamente as meias-vidas de muitas proteínas normais. Ao mesmo tempo, os achados sugerem estratégias novas e poderosas: ao projetar sequências de cauda ou induzir as células a favorecer formas de splicing ou eventos de readthrough específicos, cientistas podem um dia ajustar os níveis de proteínas para cima ou para baixo com notável precisão.
Citação: Chu, CY., Hsu, SY., Yeh, CW. et al. Protein C-terminal variations impact proteostasis. Nat Commun 17, 2288 (2026). https://doi.org/10.1038/s41467-026-68979-z
Palavras-chave: estabilidade da proteína, cauda terminal C, degradação de proteínas, mutações genéticas, proteostase