Clear Sky Science · pt
VSIG10L é um determinante importante da homeostase esofágica e da predisposição herdada ao esôfago de Barrett
Por que isso importa para pessoas com azia
Azia crônica é comum, mas apenas uma pequena parcela das pessoas desenvolve o esôfago de Barrett, uma condição que pode evoluir para câncer esofágico. Este estudo faz uma pergunta simples, porém importante: por que algumas famílias são muito mais propensas ao esôfago de Barrett do que outras? Ao traçar um único gene e observar como ele molda o revestimento do esôfago em humanos e camundongos, os pesquisadores revelam um elo perdido entre o risco herdado, o dano por refluxo e a capacidade do organismo de manter o esôfago saudável.
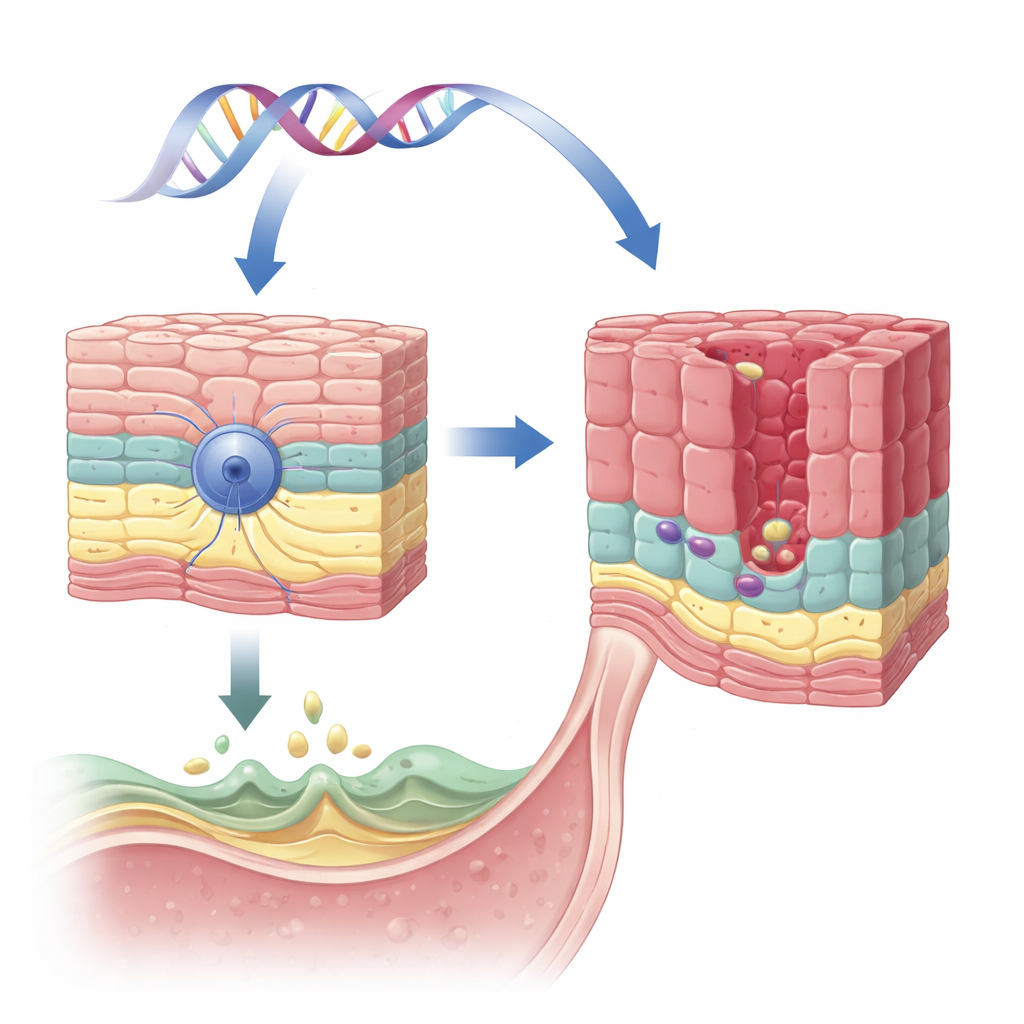
Um gene protetor no revestimento esofágico
A equipe concentrou-se em um gene chamado VSIG10L, previamente identificado em uma grande família com muitos membros afetados pelo esôfago de Barrett e cânceres relacionados. VSIG10L é ativo nas camadas superiores das células achatadas (escamosas) que revestem o esôfago, mas não nas células basais mais profundas, semelhantes a células-tronco. Usando um método sensível de detecção de RNA em tecidos humanos, de porco e de camundongo, bem como em culturas tridimensionais de células esofágicas humanas, os pesquisadores mostraram que VSIG10L é consistentemente ativado apenas em células “em maturação” logo acima da camada basal. Esse padrão sugere que VSIG10L ajuda as células escamosas a completar os passos finais de maturação e formar uma barreira estável.
Mutações herdadas que enfraquecem a barreira
Ao sequenciar o gene VSIG10L em 684 pessoas de 302 famílias com esôfago de Barrett e câncer esofágico, os investigadores descobriram várias variantes raras e potencialmente danosas. Para testar o efeito dessas variantes, eles criaram organoides esofágicos derivados de células-tronco humanas de um paciente portador de uma dessas mutações. Comparados com organoides de um doador saudável, os organoides mutantes não conseguiram construir a estrutura escamosa normal e em camadas. Em vez disso, frequentemente formaram aglomerados celulares anormais, em forma de glândula, que permaneceram travados em um estado basal imaturo, marcado pela proteína p63. Essa distorção da estratificação e da maturação normais espelha passos iniciais considerados precursores do esôfago de Barrett em pacientes.
Modelos murinos que reproduzem a doença humana
Para ir além das culturas celulares, a equipe criou camundongos portadores de uma cópia precisa da mutação familiar humana em VSIG10L ou de uma perda completa do gene. Em camundongos saudáveis, o gene correspondente Vsig10l é novamente ativo apenas nas células escamosas suprabasais. Ao microscópio eletrônico, os camundongos mutantes exibiram uma perda notável de desmossomos—os pequenos “rebites” que prendem as células vizinhas—nessas camadas. Mapas de atividade gênica do estômago escamoso, uma região do camundongo que se assemelha ao esôfago inferior, revelaram ampla interrupção dos programas estruturais e de diferenciação. Quando os camundongos receberam uma dieta contendo o ácido biliar desoxicolato, mimetizando refluxo crônico, 70–100% dos animais com mutação em Vsig10l desenvolveram extensas manchas ricas em mucina semelhantes ao Barrett na junção escamosa–colunar, enquanto camundongos do tipo selvagem desenvolveram apenas lesões pequenas e limitadas.
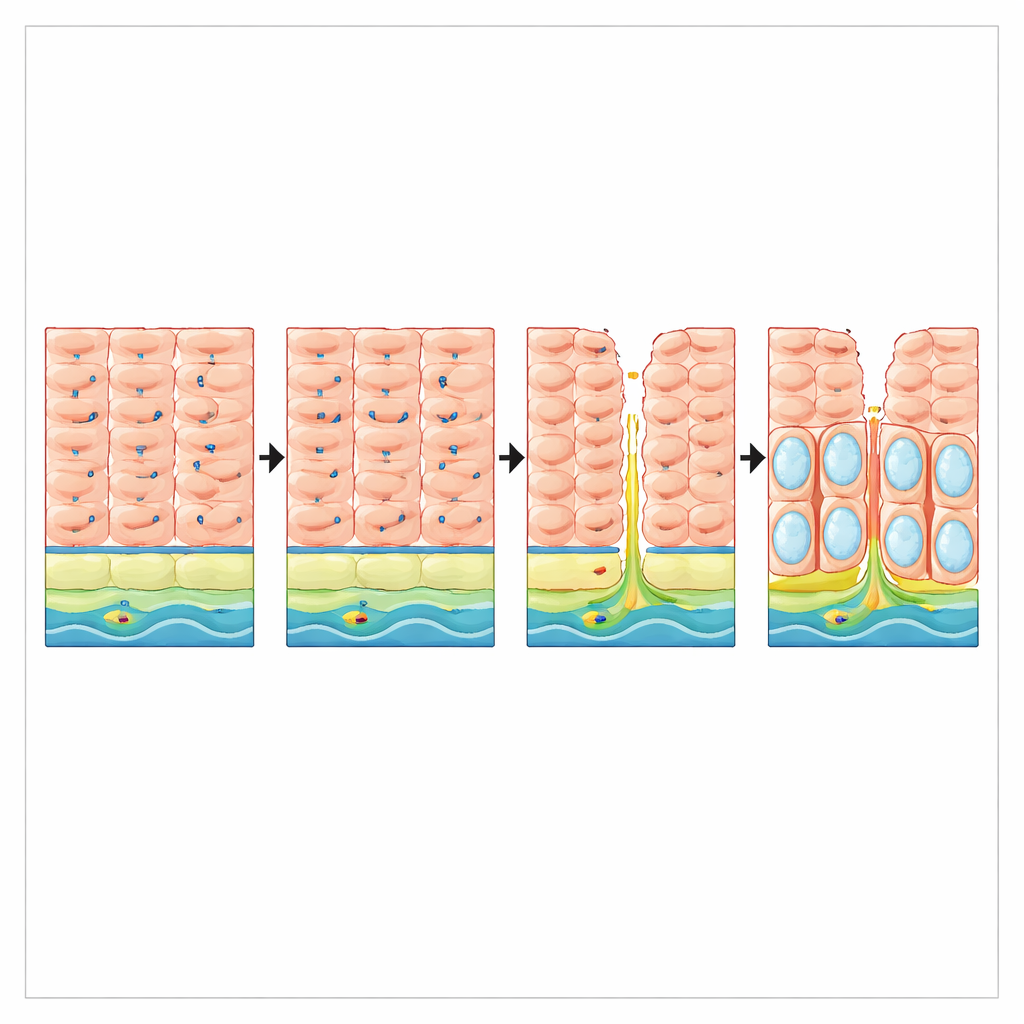
Dano por refluxo e perda de proteção em pacientes
Os pesquisadores então investigaram se o próprio refluxo poderia perturbar o VSIG10L em humanos. Em biópsias de pacientes com doença do refluxo gastroesofágico de longa duração, mas sem esôfago de Barrett, os níveis de RNA de VSIG10L foram cerca de três vezes menores do que em pessoas sem refluxo, embora o marcador básico de células escamosas TP63 permanecesse inalterado. Em cortes de tecido, o revestimento esofágico saudável mostrou uma faixa clara de células positivas para VSIG10L acima da camada basal. Em contraste, a mucosa danificada pelo refluxo exibiu uma expansão de células de tipo basal ricas em p63 e uma perda quase completa do gradiente de diferenciação positivo para VSIG10L. Essas descobertas sugerem que o refluxo crônico corrói não apenas a integridade física do revestimento, mas também o programa gênico que mantém sua renovação ordenada.
Unindo as peças
Em conjunto, o trabalho apoia um modelo simples: VSIG10L é um guardião chave da barreira escamosa esofágica. Defeitos herdados nesse gene, ou sua supressão adquirida pelo refluxo crônico, levam a uma maturação inadequada do revestimento, a menos âncoras entre células e a uma superfície mais permeável. Nesse estado vulnerável, a exposição repetida ao ácido e à bile promove uma cicatrização anômala em forma de glândula em vez da restauração do revestimento escamoso original, preparando o terreno para o esôfago de Barrett. Para pacientes e famílias, essa pesquisa aponta para futuros testes genéticos que possam identificar os mais expostos ao risco e para novas terapias destinadas a preservar ou restaurar a função de VSIG10L, com o objetivo de longo prazo de prevenir o esôfago de Barrett e sua progressão para câncer.
Citação: Ravillah, D., Singh, S., Katabathula, R.M. et al. VSIG10L is a major determinant of esophageal homeostasis and inherited predisposition to Barrett’s esophagus. Nat Commun 17, 2167 (2026). https://doi.org/10.1038/s41467-026-68975-3
Palavras-chave: esôfago de Barrett, refluxo gastroesofágico, predisposição genética, homeostase epitelial, risco de câncer esofágico