Clear Sky Science · pt
Explorando a alosteria da fucosiltransferase humana 8 com um inibidor covalente para suprimir a fucosilação central
Por que bloquear um açúcar minúsculo pode fazer diferença no câncer
Nossas células constantemente decoram proteínas com pequenas cadeias de açúcar que ajustam finamente como essas proteínas funcionam. Uma marca de açúcar em particular, chamada fucosilação central, ajuda tumores a crescer, se espalhar, escapar do sistema imune e até resistir a drogas modernas contra o câncer. Este artigo descreve como cientistas encontraram um ponto de controle oculto na enzima humana que adiciona esse açúcar e construíram uma nova molécula de baixa toxicidade que se prende a esse ponto de controle para desligar a enzima. O trabalho abre um novo caminho para medicamentos que reprogramam sutilmente os açúcares da superfície celular em vez de atacar diretamente o DNA ou as proteínas.
Como as células usam marcas de açúcar para moldar a doença
Proteínas que saem da “fábrica” interna da célula passam por uma linha de acabamento molecular onde cadeias de açúcar são anexadas e editadas. A fucosilação central é um desses passos finais, realizado por uma enzima chamada FUT8, que adiciona uma única unidade de fucose a uma posição-chave em muitos glicanos ligados a proteínas. Quando os níveis de FUT8 aumentam, essa marca de açúcar se torna mais comum em moléculas que controlam o crescimento celular, a movimentação e o reconhecimento imune. Estudos associaram alta atividade de FUT8 a melanomas agressivos, câncer de mama triple-negativo, câncer de pulmão e resistência a drogas direcionadas e a algumas terapias com anticorpos. Bloquear a FUT8 pode remover certas proteínas imunoinibitórias, como PD‑1, da superfície celular e tornar tumores mais visíveis ao sistema imune, tornando FUT8 um alvo atraente para imunoterapia do câncer e para melhorar fármacos biológicos.
A necessidade de bloqueadores mais inteligentes e seletivos
Projetar fármacos contra FUT8 tem sido difícil porque muitas enzimas relacionadas usam o mesmo combustível açúcar básico. Inibidores anteriores frequentemente mimetizavam esse substrato, levando a uma neutralização ampla e não seletiva de várias vias de fucosilação e a efeitos colaterais indesejados, incluindo problemas de coagulação que interromperam um ensaio clínico. Os autores raciocinaram que uma estratégia melhor seria evitar o sítio ativo principal, muito concorrido, e em vez disso buscar um sítio único “remoto” na FUT8 que pudesse atuar como um interruptor de controle. Usando um ensaio de triagem de alto rendimento que monitorava a atividade enzimática, eles vasculharam mais de seis mil compostos e identificaram algumas moléculas em forma de cadeia que retardavam a FUT8 enquanto também reduziam a invasão de células cancerosas em pratos de cultura.
Descobrindo um bolso de controle oculto
Usando cristalografia de raios X, a equipe resolveu as estruturas tridimensionais da FUT8 ligadas a dois desses inibidores. Para surpresa deles, nenhum dos compostos se acomodou no ponto habitual onde o doador e o aceitador do açúcar se ligam. Em vez disso, ambos encaixaram em um bolso longo, em forma de canal, entre dois lobos principais da enzima, próximo porém distinto do centro ativo. A ligação nesse sítio deslocou certos loops e aminoácidos-chave de suas posições, particularmente elementos que normalmente ajudam a prender o doador de açúcar. Simulações por computador mostraram que, quando o bolso estava ocupado, o movimento global e o paisagem energética da FUT8 mudavam, favorecendo formas com baixa capacidade catalítica. Em outras palavras, os inibidores funcionavam alostericamente: pressionavam um botão distante que fazia com que as partes atuantes da enzima ficassem desalinhadas.
Transformando uma molécula promissora em uma ferramenta covalente precisa
Munidos desse mapa estrutural, os pesquisadores procuraram moléculas que não apenas ocupassem o bolso, mas também pudessem formar uma ligação permanente a um resíduo de lisina próximo (K216) que naturalmente se movimenta em direção ao canal. Eles descobriram que um reagente chamado SSO, que carrega um éster N‑hidroxissuccinimida reativo, ligava‑se ao mesmo sulco e formava uma ligação covalente com K216, travando a enzima em um estado inativo. A partir das características compartilhadas do SSO e do composto inicial NH125, combinaram fragmentos de ambos para criar uma nova molécula chamada CAIF. Estruturas cristalográficas confirmaram que o CAIF se encaixa ao longo do canal, ajusta‑se entre resíduos hidrofóbicos e forma uma ligação covalente com K216. Esse projeto aumentou a inibição da FUT8 várias vezes em comparação com os compostos originais, preservando enzimas estreitamente relacionadas e destacando a forma única do bolso alostérico da FUT8.
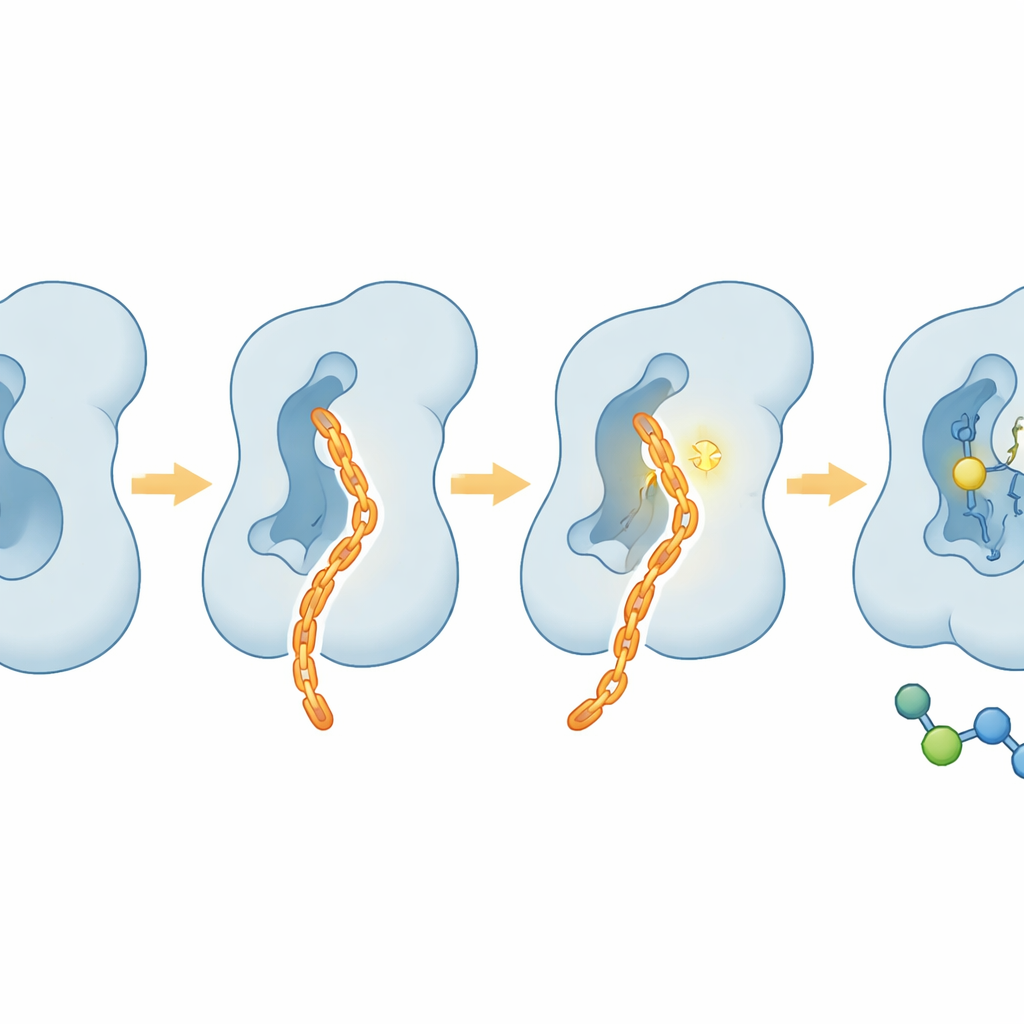
Suave para as células, duro no comportamento tumoral
Além de tubos de ensaio, a equipe examinou como o CAIF se comporta em células vivas. Em várias linhas celulares humanas, o CAIF mostrou toxicidade mínima mesmo em doses altas, indicando que não envenena amplamente a maquinaria celular. Ainda assim, reduziu marcadamente a fucosilação central na superfície celular, conforme revelado por corantes que se ligam a açúcares, e fez isso com muito mais seletividade para a FUT8 do que inibidores pan‑fucosilantes anteriores. Em ensaios de invasão de células cancerosas, o CAIF superou um bloqueador à base de açúcar comumente usado ao limitar a capacidade das células tumorais de migrar através de uma matriz, um marco da potencialidade metastática. Esses efeitos estão alinhados com o papel conhecido da FUT8 em aumentar invasão e evasão imune, em vez de impulsionar diretamente a divisão celular.
O que isso significa para tratamentos futuros contra o câncer
Este estudo não afirma que o CAIF em si esteja pronto para ser um fármaco. Em vez disso, demonstra que a FUT8 contém um bolso alostérico anteriormente desconhecido e susceptível a fármacos, que pode ser alvo de moléculas cuidadosamente modeladas que formam uma ligação durável a uma única lisina. Explorando esse sítio, os pesquisadores podem reduzir seletivamente a atividade de uma enzima que modifica açúcares e que se situa no cruzamento da progressão tumoral, evasão imune e resistência a medicamentos, ao mesmo tempo em que deixa enzimas relacionadas amplamente intactas. O trabalho oferece um roteiro para projetar inibidores de próxima geração que redefinam padrões de açúcar relevantes para a doença em proteínas e que podem, em última instância, ampliar o arsenal para imunoterapia do câncer e melhorar medicamentos baseados em anticorpos.
Citação: Jiang, J., He, D., Ke, M. et al. Exploiting human fucosyltransferase 8 allostery with a covalent inhibitor for core fucosylation suppression. Nat Commun 17, 2607 (2026). https://doi.org/10.1038/s41467-026-68971-7
Palavras-chave: Inibição de FUT8, fucosilação central, inibidores alostéricos covalentes, glicosilação no câncer, desenho de fármacos para glicosiltransferases