Clear Sky Science · pt
FANCD2 restringe a progressão das forquilhas e previne fragilidade em origens precoces durante a re-replicação
Quando as cópias de DNA saem um pouco do roteiro
Toda vez que uma célula se divide, precisa copiar sua biblioteca de DNA inteira exatamente uma vez. Se partes dessa biblioteca são copiadas duas vezes, ou copiadas de forma apressada e desleixada, o resultado pode ser cromossomos quebrados e mutações que alimentam o câncer. Este estudo examina o que acontece quando as salvaguardas da célula contra rodadas extras de cópia começam a falhar e revela como uma proteína de reparo chamada FANCD2 intervém para evitar que células com mau comportamento moderado deslizem para um caos genômico completo.
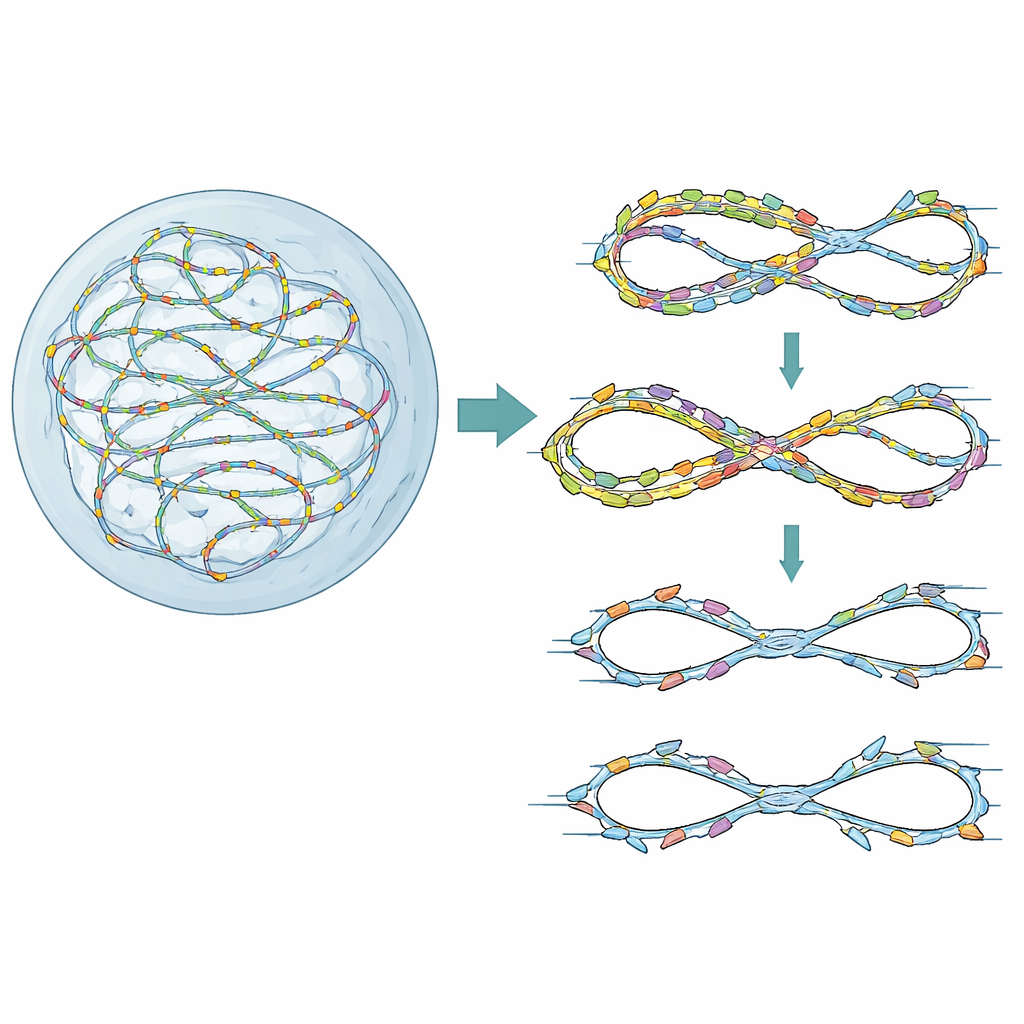
Guardiões para uma cópia limpa
Nossos cromossomos são duplicados a partir de milhares de pontos de partida, ou “origens”, que são licenciadas e depois ativadas em uma sequência cuidadosamente cronometrada. Uma pequena proteína chamada Geminin normalmente ajuda a garantir que cada origem seja ativada apenas uma vez por ciclo celular. Quando a Geminin é perdida ou enfraquecida, algumas origens podem disparar novamente sobre DNA já copiado, uma situação conhecida como re-replicação. Células cancerosas, que frequentemente superproduzem fatores de licenciamento, são especialmente suscetíveis a esse problema. Os autores usaram primeiro uma triagem genética de alto teor em células humanas preparadas para re-replicação em baixo nível pela depleção de Geminin. Eles perguntaram quais genes de reparo de DNA e pontos de checagem se tornam cruciais nesse estado estressado e descobriram que FANCD2, mais conhecido por reparar entrecruzamentos de DNA na anemia de Fanconi, emergiu como um protetor chave da sobrevivência celular e da integridade do genoma.
Um primeiro respondente nas máquinas de cópia sobrecarregadas
A equipe então rastreou onde e quando o FANCD2 aparece em células passando por re-replicação. Logo após a remoção da Geminin, o FANCD2 se acumula rapidamente na cromatina e forma focos nucleares brilhantes, bem antes de detecções amplas de quebras de DNA. Usando marcação do DNA recém-sintetizado juntamente com ensaios de proximidade, mostraram que o FANCD2 é recrutado diretamente às máquinas de replicação ativas, especialmente em células cujo DNA já está sendo copiado uma segunda vez. Em células sincronizadas liberadas para o próximo ciclo de divisão, surgiu uma população distinta com um padrão de DNA de sobre-replicação difuso. Essas células exibiram sinais fortes de FANCD2 e RPA, indicando estresse de replicação em curso, e foram mantidas na fronteira antes da mitose por um ponto de checagem ativo, sugerindo que o FANCD2 faz parte de uma resposta precoce que estabiliza forquilhas estressadas em vez de simplesmente reagir a DNA quebrado.
Segurando forquilhas descontroladas e lacunas ocultas
Para testar como o FANCD2 molda a cópia do DNA, os pesquisadores combinaram a perda de Geminin com a depleção de FANCD2. Surpreendentemente, remover FANCD2 não aumentou a fração de células com genomas obviamente re-replicados. Em vez disso, ensaios de fibras de DNA em molécula única revelaram que as forquilhas de replicação percorreram distâncias maiores e ficaram mais assimétricas, um sinal de progressão desigual e instável. Essas forquilhas mais rápidas deixaram para trás mais lacunas de fita simples no DNA recém-formado, vistas como focos intensos de RPA e BrdU nativo e confirmadas pela sensibilidade de trechos marcados a uma enzima que corta regiões de fita simples. Células sem Geminin e sem FANCD2 apresentaram um aumento em quebras cromossômicas, fragmentos, corpos nucleares e micronúcleos, todos sinais de severa instabilidade genômica. Bloquear a PARP, um fator que normalmente ajuda a manejar tais lacunas, imitou e agravou esses defeitos, ressaltando que a formação descontrolada de lacunas é central para o dano.
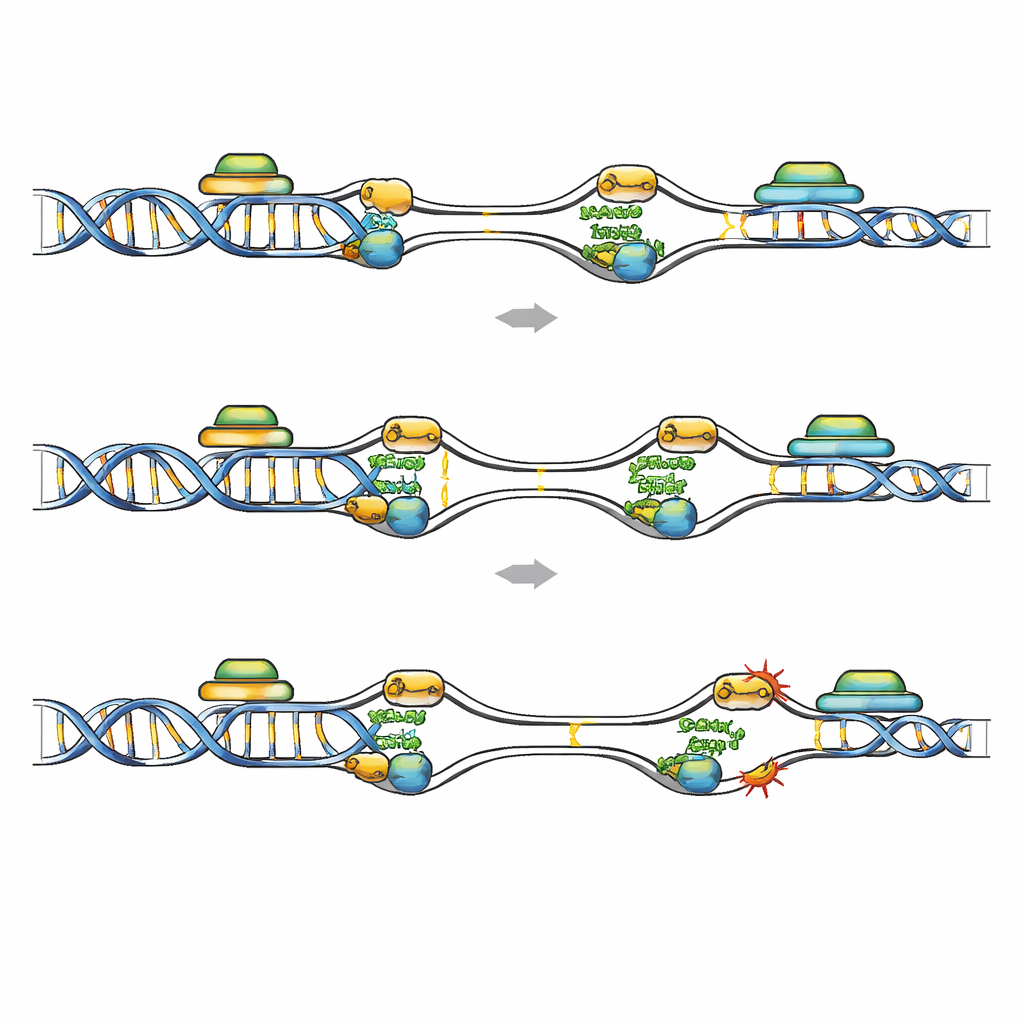
Pontos frágeis onde copiar e transcrever colidem
Mapeamentos genômicos da ligação de FANCD2 ofereceram uma visão de onde a re-replicação é mais perigosa. Em células leucêmicas depletadas de Geminin, o FANCD2 deslocou-se de sítios frágeis comuns clássicos para origens de replicação que disparam cedo e estão embutidas em genes curtos, ricos em GC e altamente transcritos. Essas regiões apresentam marcas de transcrição ativa e são propensas a R-loops, onde o RNA nascente se híbrida com o DNA molde, potencialmente bloqueando a replicação. Conjuntos públicos de dados mostraram mais dano ao DNA e sinais elevados de híbridos RNA–DNA em genes enriquecidos por FANCD2 após a perda de Geminin, e essas regiões se sobrepuseram com os chamados sítios frágeis de replicação precoce. Quando a transcrição foi amplamente reduzida com um fármaco, ou quando R-loops foram removidos especificamente pela superexpressão de RNase H1, o número de focos de FANCD2, RPA e dano ao DNA em células deficientes em Geminin caiu marcadamente. Isso indica que colisões entre origens reativadas e unidades de transcrição ativas, amplificadas por R-loops, criam pontos frágeis que o FANCD2 precisa proteger.
Ajustando a proteção por meio de marcas químicas
O FANCD2 é ativado em parte pela adição de uma pequena etiqueta semelhante à ubiquitina. Ao depletar FANCA, um componente central da maquinaria de marcação, e usando células que expressam uma versão mutante do FANCD2 resistente a essa modificação, os autores mostraram que a mono-ubiquitinação melhora a sobrevivência de células em re-replicação, mas não é absolutamente necessária. Mesmo o FANCD2 não marcado ofereceu proteção parcial, consistente com papéis distintos tanto na detecção quanto na estabilização de forquilhas estressadas. O panorama geral é que o FANCD2 ajuda a desacelerar e organizar a replicação em origens precoces vulneráveis e limita quantas e quão grandes as lacunas de fita simples se tornam.
Por que isso importa para o tratamento do câncer
Para não especialistas, a mensagem central é que nem todo erro de replicação é catastrófico desde o começo. Re-replicação leve, como ocorre em alguns tumores, pode ser tolerada se sistemas protetores como o FANCD2 mantiverem a cópia de DNA descontrolada sob controle e evitarem que lacunas frágeis se transformem em cromossomos quebrados. Quando essa salvaguarda é removida ou sobrecarregada, os mesmos erros de licenciamento em baixo nível rapidamente escalam para uma fragmentação do genoma. Como a perda de Geminin e defeitos no licenciamento da replicação são enriquecidos em células cancerosas, e muitos tumores já carregam fragilidades na rede Fanconi/BRCA, as vulnerabilidades aqui reveladas sugerem estratégias terapêuticas: combinar inibidores que empurrem células cancerosas em direção à re-replicação com fármacos que exacerbem o acúmulo de lacunas, como inibidores de PARP, poderia conduzir seletivamente células malignas além de seu limite de tolerância enquanto poupa células normais com proteção intacta.
Citação: Badra-Fajardo, N., Karydi, E., Bayona-Feliu, A. et al. FANCD2 restrains fork progression and prevents fragility at early origins upon re-replication. Nat Commun 17, 2478 (2026). https://doi.org/10.1038/s41467-026-68966-4
Palavras-chave: Estresse na replicação do DNA, FANCD2, Geminin, re-replicação, instabilidade genômica