Clear Sky Science · pt
O dobramento induzido por associação governa a montagem do componente da cadeia leve substituta e do receptor pré-B
Como nossos corpos testam novos anticorpos
Antes que uma célula B jovem na medula óssea seja autorizada a entrar no sistema imunológico, ela precisa passar por um teste rigoroso: consegue construir um núcleo de anticorpo funcional? Este artigo explora como uma versão “de ensaio” de parte do anticorpo, chamada cadeia leve substituta, ajuda a realizar esse teste. Ao observar como essas proteínas se dobram e se encaixam, os autores revelam um sistema oculto de controle de qualidade que decide quais anticorpos futuros são bons o bastante para serem mantidos — e quais são descartados.
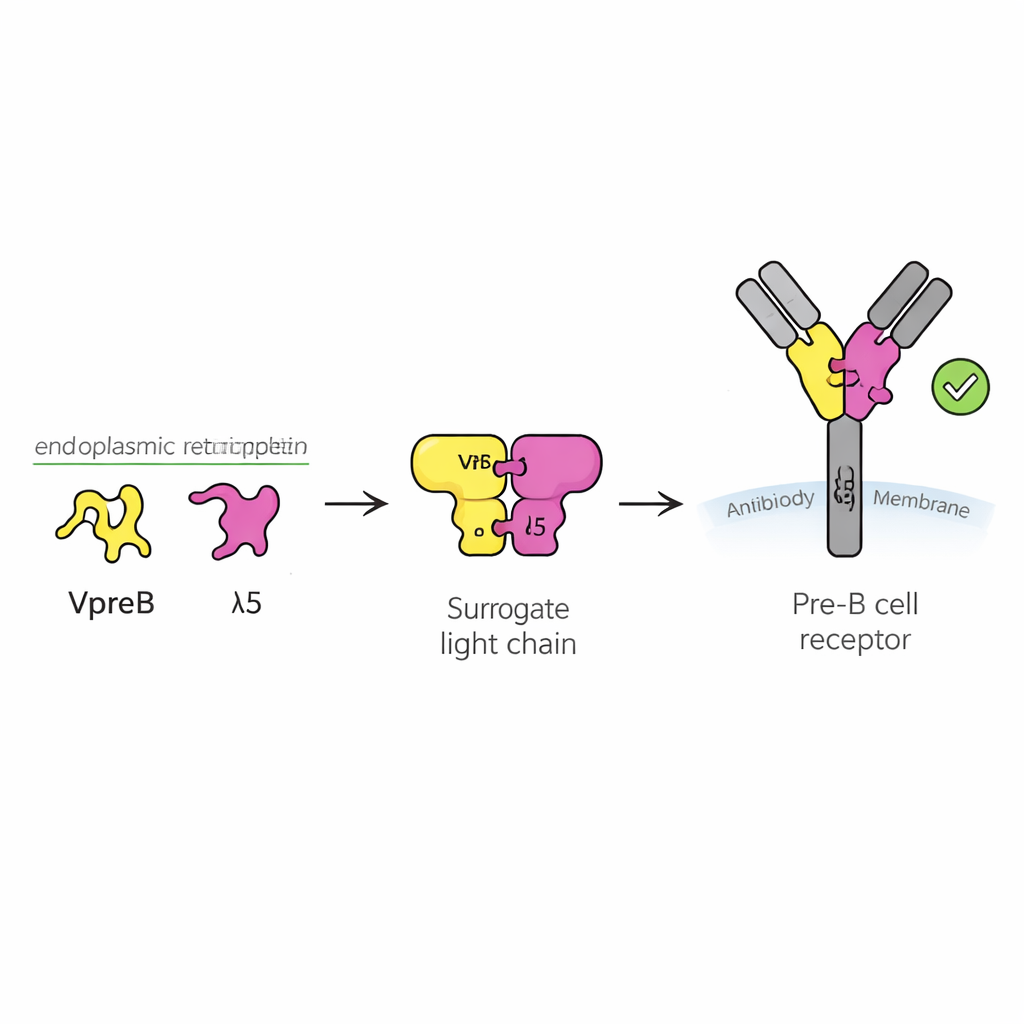
Um ponto de verificação de segurança para células imunes jovens
Anticorpos são proteínas em forma de Y que reconhecem invasores. Eles são constituídos por duas partes principais: cadeias pesadas e cadeias leves. Durante o desenvolvimento das células B, a cadeia pesada é produzida primeiro, e a célula precisa verificar se essa nova cadeia pesada é útil antes de investir energia para fabricar uma cadeia leve correspondente. Para isso, a célula usa um substituto temporário chamado cadeia leve substituta, formado por duas proteínas denominadas VpreB e λ5. Juntas com a cadeia pesada, elas formam o receptor pré-B, um sensor na superfície celular que envia um sinal de “siga” ou “pare”. Cerca de metade das cadeias pesadas recém-rearranjadas falham nesse teste, então entender como a cadeia leve substituta funciona é fundamental para compreender como um repertório saudável de anticorpos é construído.
Dobramento por associação: ajudando um parceiro instável
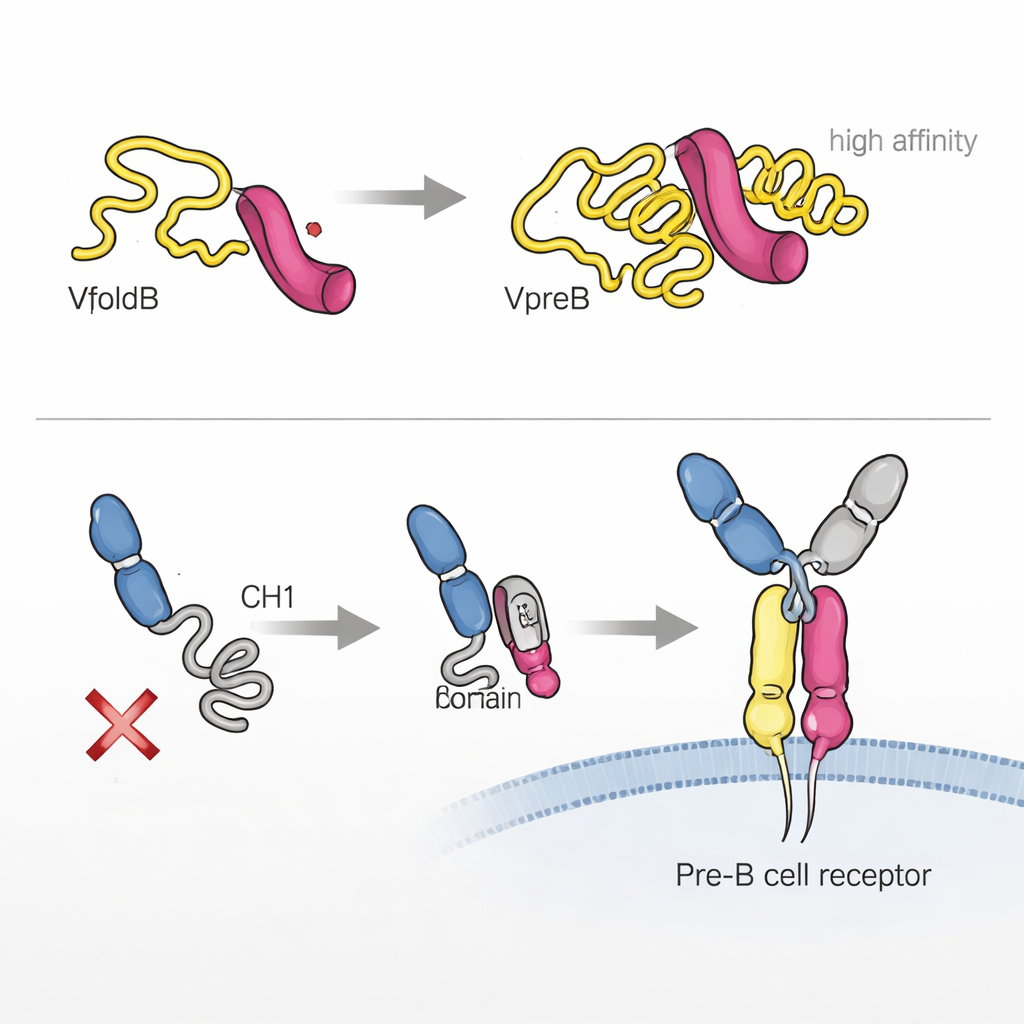
Os autores descobriram que um dos componentes, VpreB, está em grande parte não dobrado e é instável quando isolado. Usando técnicas biofísicas, mostraram que ele só adquire sua forma tridimensional correta quando se liga à λ5. Um trecho curto de λ5, em forma de folha beta, encaixa-se em VpreB e completa sua estrutura, como inserir um dente que falta em uma engrenagem. Esse “dobramento induzido por associação” não apenas estabiliza VpreB, como também cria uma parceria muito forte entre as duas proteínas, com afinidade na faixa de baixos nanomolares. Nas células, somente quando VpreB e λ5 se montam nessa cadeia leve substituta é que escapam da retenção no retículo endoplasmático e passam a ser secretadas ou encaminhadas adiante, destacando como dobramento e controle de qualidade estão fortemente acoplados.
Finalizando a cadeia pesada e aprovando a inspeção
A história não termina com VpreB e λ5. Uma região crucial da cadeia pesada, chamada CH1, é inicialmente não estruturada e mantida dentro da célula. Os pesquisadores mostraram que λ5, atuando de certo modo como uma chaperona, pode desencadear o dobramento de CH1 quando se ligam. Essa segunda etapa de dobramento induzido por associação é essencial para construir o receptor pré-B completo e permitir que ele saia do retículo endoplasmático e alcance a superfície celular. Curiosamente, ambas as partes da cadeia leve substituta — VpreB e λ5 — podem tocar a cadeia pesada, mas apenas λ5 é capaz de conduzir CH1 ao seu estado final, competente para dobramento. Quando isso não ocorre, o receptor parcial é retido e a célula rejeita efetivamente aquela cadeia pesada.
Caudas flexíveis que afinam a ligação e o sinal
Tanto VpreB quanto λ5 carregam segmentos flexíveis e não estruturados conhecidos como regiões únicas, que não se assemelham a nenhuma sequência proteica conhecida. Embora essas caudas não sejam estritamente necessárias para que as duas proteínas se montem em um tubo de ensaio, a equipe descobriu que elas influenciam fortemente a rapidez com que a cadeia leve substituta se forma, quão estável ela fica e quão bem se liga a segmentos da cadeia pesada. Nas células, remover essas regiões reduziu a eficiência de secreção dos complexos montados. A cauda de λ5, em particular, revelou-se multitarefas: ajuda a acelerar a montagem, é essencial para certos contatos com a região variável da cadeia pesada e contribui significativamente para a forma como o receptor pré-B interage com antígenos e outros ligantes. Em alguns casos, a força de ligação de uma combinação cadeia leve substituta–cadeia pesada chegou perto da de um fragmento de anticorpo normal.
Por que isso importa para a diversidade de anticorpos
Ao mapear esses eventos passo a passo de dobramento e montagem, os autores propõem que a cadeia leve substituta faz mais do que simplesmente manter a cadeia pesada no lugar. Ela atua como uma inspetora dinâmica, usando seu núcleo estruturado e suas caudas flexíveis para perceber se uma cadeia pesada pode dobrar corretamente e interagir produtivamente com alvos potenciais. Combinações bem-sucedidas são dobradas, estabilizadas e autorizadas a alcançar a superfície celular, onde enviam sinais que permitem à célula B continuar a maturação. Combinações defeituosas ficam presas e são eventualmente eliminadas. Para o leitor leigo, a conclusão é que seu sistema imunológico executa uma sofisticada “bancada de testes” para futuros anticorpos, construída a partir de proteínas que literalmente dobram umas às outras, garantindo que apenas núcleos de anticorpos bem comportados prossigam para defendê-lo.
Citação: König, J., Sarmiento Alam, N.C., He, R. et al. Association-induced folding governs surrogate light chain and pre-B cell receptor core assembly. Nat Commun 17, 1202 (2026). https://doi.org/10.1038/s41467-026-68965-5
Palavras-chave: desenvolvimento de células B, dobramento de anticorpos, cadeia leve substituta, controle de qualidade de proteínas, receptor pré-B