Clear Sky Science · pt
Destravando a deracemização enzimática de allenos estruturalmente diversos por fotoenzimas projetadas
Por que combinar e adequar moléculas importa
Muitos medicamentos funcionam apenas quando seus átomos estão organizados de uma maneira tridimensional muito específica, como uma mão esquerda que cabe em uma luva esquerda, mas não em uma direita. Quimistas frequentemente conseguem sintetizar essas moléculas “de uma só mão”, mas é difícil fazê‑lo de forma limpa quando os blocos de construção são complexos. Este artigo enfrenta esse desafio para uma classe difícil de estruturas torcidas chamadas allenos, usando enzimas movidas por luz projetadas sob medida. O trabalho demonstra como biologia e fotoquímica podem ser combinadas para separar a “mão” molecular desejada de uma mistura embaralhada, prometendo rotas mais rápidas e limpas para futuros medicamentos e materiais.
Blocos torcidos com grande retorno
Allenos são cadeias lineares de três átomos de carbono com duas ligações duplas adjacentes, mas esse arranjo simples torce o espaço de modo a conferir à molécula uma quiralidade axial. Essas torções aparecem em produtos naturais, agentes de proteção de culturas e catalisadores avançados. Infelizmente, métodos tradicionais para produzir allenos quirais tendem a ser altamente especializados: um catalisador que funciona muito bem para um alleno frequentemente falha para outro com pequenas mudanças na estrutura. Mesmo catalisadores químicos acionados por luz desenvolvidos recentemente enfrentam essa limitação. Como resultado, os químicos precisam redesenhar catalisadores repetidamente quando querem explorar novos allenos, retardando a descoberta e aumentando o desperdício.
Tomando emprestada a seletividade da natureza e adicionando luz
Enzimas em sistemas vivos são excelentes em reconhecer e transformar formas específicas com precisão notável, mas elas evoluíram para alvos naturais, não para allenos sintéticos. Os autores propuseram criar uma “fotoenzima” que combine seletividade do tipo enzimático com a capacidade de captar luz como fonte de energia. Eles partiram de um arcabouço proteico chamado CTB10 e o reprogramaram geneticamente para incorporar um aminoácido não natural que age como uma pequena antena de luz incorporada. Quando esse bloco especial absorve luz ultravioleta, ele pode transferir energia para um alleno próximo, excitando‑o temporariamente e permitindo que sua torção seja embaralhada. Ao repetir esse processo muitas vezes, a enzima pode remover seletivamente uma das mãos de uma mistura 50:50 e deixar para trás predominantemente a outra. 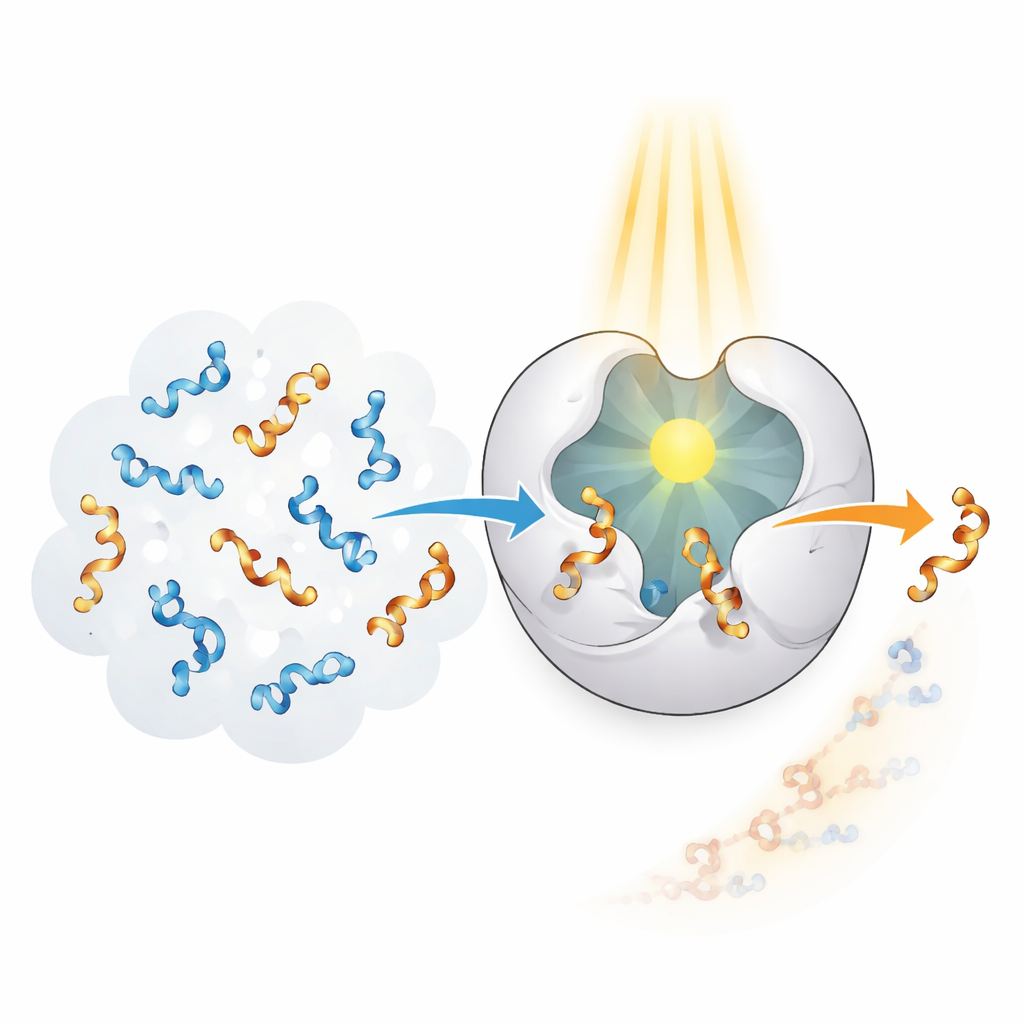
Esculpindo bolsos ajustados para muitos convidados diferentes
Projetar um sistema assim não é tão simples quanto iluminar uma proteína. A equipe usou modelagem por computador, mutações estratégicas e imagens por raios X para esculpir várias versões da fotoenzima, cada uma com um bolso interno ligeiramente diferente. Esses bolsos mantêm o alleno em uma pose definida ao lado da antena de luz e estabilizam partes-chave da molécula por meio de ligações de hidrogênio e interações sutis de empacotamento. Passo a passo, os pesquisadores melhoraram tanto a afinidade de ligação quanto o alinhamento entre enzima e alleno, fatores cruciais para uma transferência de energia eficiente. As variantes finais mostraram desempenho impressionante, convertendo ácidos carboxílicos de alleno, ésteres e amidas em produtos de mão única com pureza muito alta, frequentemente acima de 99% de uma das mãos, e fazendo isso em ar sem necessidade de condições delicadas.
Observando o mecanismo em resolução atômica
Para entender por que as novas fotoenzimas preferem uma mão em detrimento da outra, os autores cristalizaram pares enzima–substrato e os examinaram em resolução atômica. Eles descobriram que a mão do alleno favorecida fica mais próxima do grupo coletor de luz e pode adotar várias conformações ligeiramente diferentes, todas compatíveis com transferência de energia eficiente. A mão desfavorecida ou se liga fracamente ou fica mais afastada, tornando muito menos provável sua excitação. Experimentos adicionais com materiais de partida puramente dextrógiros e levógios confirmaram esse viés: a enzima converte rapidamente a mão preferida em um intermediário reativo, que então relaxa em solução para uma mistura onde a mão oposta se acumula. Em essência, a proteína se comporta como uma catraca molecular, excitando e consumindo repetidamente uma mão enquanto permite que a outra se acumule. 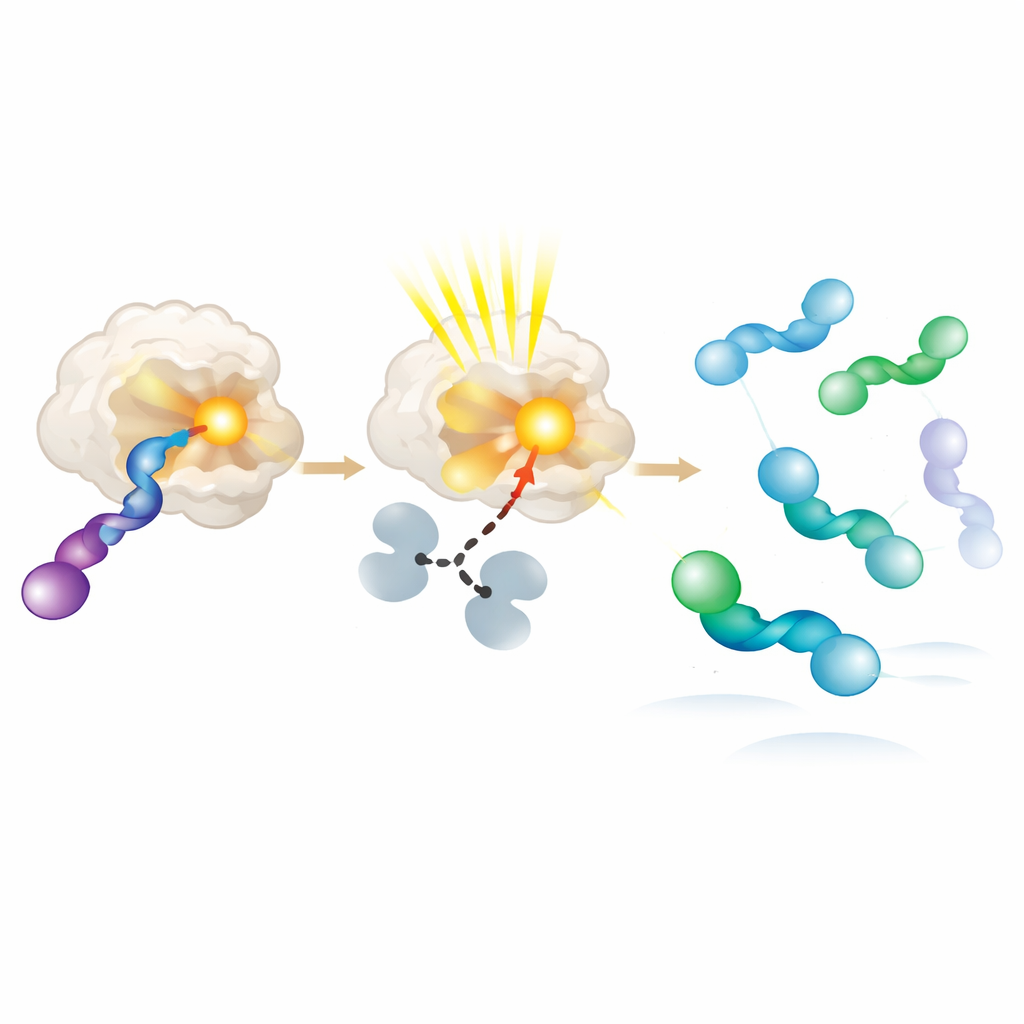
O que isso significa para a química futura
Para não especialistas, a mensagem principal é que a equipe criou uma máquina proteica programável que usa luz para classificar e aprimorar moléculas torcidas com versatilidade sem precedentes. Em vez de projetar um novo catalisador químico para cada alvo, os pesquisadores podem agora partir desta plataforma de fotoenzima e ajustar seu bolso interno para aceitar muitos allenos diferentes. Essa abordagem reduz a lacuna entre o controle refinado da natureza e a necessidade da indústria química por métodos amplos e robustos. A longo prazo, tais enzimas movidas a luz poderiam ajudar químicos a preparar blocos de construção complexos e de mão única para medicamentos e materiais de forma mais eficiente, com menos etapas e menos desperdício.
Citação: Fu, K., Li, M., Deng, Z. et al. Unlocking enzymatic deracemization of structurally diverse allenes by designed photoenzymes. Nat Commun 17, 2082 (2026). https://doi.org/10.1038/s41467-026-68964-6
Palavras-chave: fotoenzima, deracemização, alleno quiral, biocatálise, transferência de energia triplet