Clear Sky Science · pt
A infecção por HCMV prejudica funções de barreira e promove transição epitelial–mesenquimal em um modelo de organoide de colangiócito
Por que essa história do vírus no fígado importa
O citomegalovírus humano é um vírus muito comum que a maioria de nós carrega sem saber. No entanto, em recém-nascidos e pessoas com o sistema imunológico fragilizado, ele pode estar associado a problemas graves no fígado e nos ductos biliares, incluindo uma doença infantil rara, porém devastadora, chamada atresia biliar. Este estudo usa ductos biliares humanos em miniatura, cultivados em laboratório, para mostrar como o vírus pode danificar diretamente esses tubos delicados e desencadear alterações de fibrose que podem ajudar a explicar as ligações entre infecção e doença hepática crônica, discutidas há muito tempo.
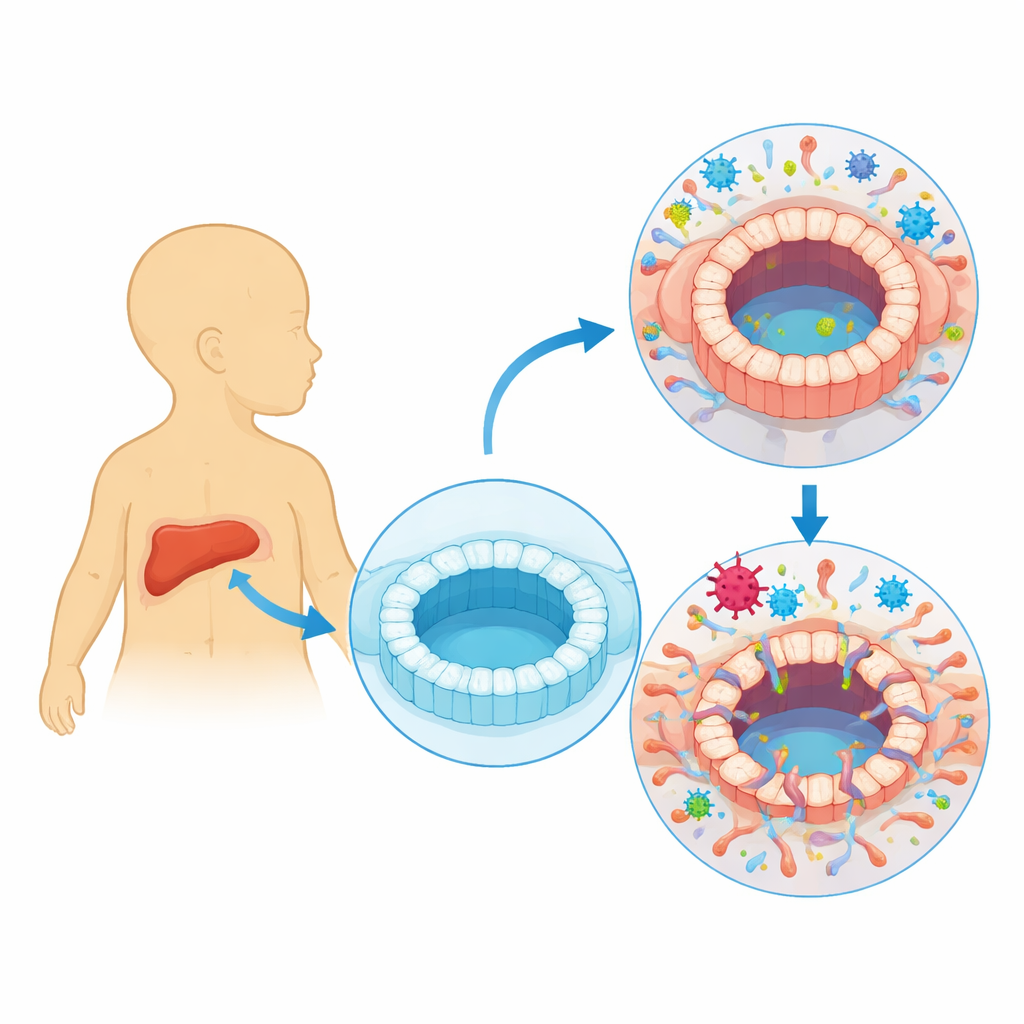
Uma olhada mais próxima em um vírus comum, mas silencioso
O citomegalovírus humano (HCMV) costuma permanecer silencioso em nossos corpos, alternando entre uma fase ativa, em que produz novas partículas virais, e uma fase latente, em que se esconde dentro de certos leucócitos. Clínicos há muito tempo notam que pessoas com infecção evidente por HCMV podem desenvolver lesão dos ductos biliares e colestase, condição em que a bile não flui corretamente. Muitos lactentes com atresia biliar, condição em que os ductos biliares se obstruem e se cicatrizam logo após o nascimento, também apresentam sinais de infecção recente por HCMV. No entanto, permanecia incerto se o vírus realmente infecta as células que revestem os ductos biliares ou se aparece apenas como espectador durante a doença.
Construindo pequenos ductos biliares em placa
Para responder a isso, os pesquisadores criaram organoides tridimensionais que imitam os ductos biliares humanos. Eles partiram de células-tronco pluripotentes induzidas, reprogramadas a partir do sangue humano, e as direcionaram para formar células do tipo colangiócito — o tipo que reveste os ductos biliares. Essas células se auto-organizaram em esferas ocas com uma cavidade central e conexões célula–célula apertadas, assemelhando-se a um ducto biliar em miniatura. A equipe então expôs esses organoides a uma linhagem de HCMV marcada com um marcador fluorescente que acende quando o vírus está se replicando ativamente. Isso lhes permitiu rastrear as células infectadas e medir como os organoides mudavam ao longo do tempo.
Como a infecção deforma a estrutura e enfraquece a barreira
Uma vez infectados, os organoides deixaram de crescer normalmente e ficaram deformados, com paredes engrossadas e irregulares. Algumas células brilhavam intensamente, mostrando atividade viral completa e produção de novas partículas virais; outras carregavam material genético viral em níveis mais baixos, sugerindo um estado mais dormente, semelhante à latência. Testes funcionais revelaram que os organoides infectados perderam capacidades chave dos ductos biliares. Eles não mais inchavam adequadamente em resposta a um estímulo que depende de canais de transporte iônico e apresentaram maior vazamento em um ensaio de resistência elétrica que mede a tensão da barreira. Proteínas que normalmente selam os espaços entre as células, como componentes de junções estreitas, foram reduzidas, e o transporte de um corante de teste para dentro e fora da cavidade interna tornou‑se anormal. Em conjunto, essas alterações mostram que o HCMV pode comprometer diretamente a parede do ducto biliar, tornando‑a permeável e disfuncional.
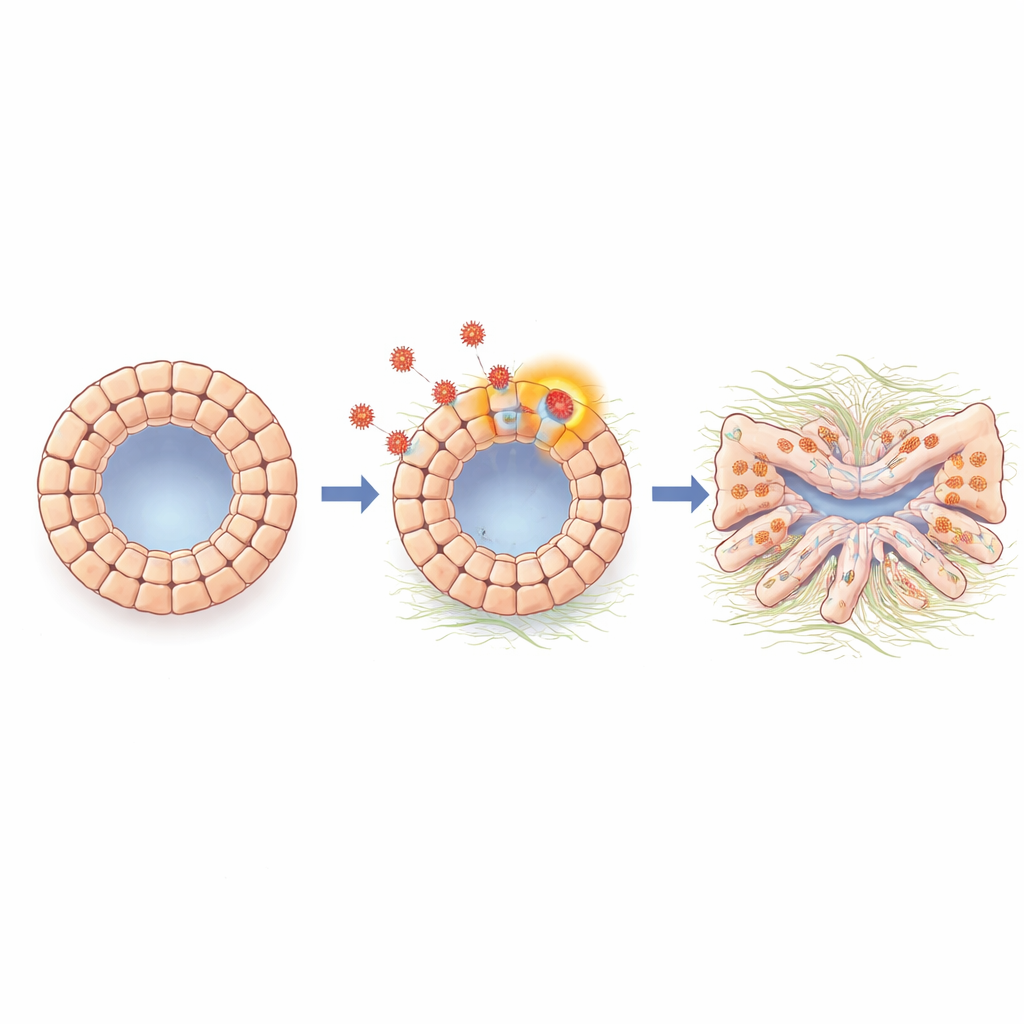
As células mudam de identidade em direção a um estado fibrótico
Indo mais fundo, os cientistas analisaram a atividade gênica nos organoides em nível de conjunto e em resolução de célula única. Eles identificaram uma forte ativação de um programa semelhante à transição epitelial–mesenquimal, processo no qual células superficiais fortemente conectadas afrouxam suas ligações, adotam uma característica mais móvel e fibrosa e passam a produzir moléculas associadas à cicatrização do tecido. Os organoides infectados mostraram níveis aumentados de N‑cadherina e outros marcadores ligados a essa mudança, bem como genes envolvidos em fibrose e produção de matriz. Uma molécula sinalizadora chamada TGF‑beta, bem conhecida por dirigir a fibrose em muitos órgãos, foi aumentada durante a infecção. Quando a equipe bloqueou a sinalização de TGF‑beta com um inibidor de pequena molécula ou um anticorpo, os organoides recuperaram uma forma mais normal, e muitos dos genes relacionados à cicatrização e à transição voltaram em direção ao nível basal, indicando que o TGF‑beta é um intermediário chave conectando a presença viral às alterações celulares prejudiciais.
Dos tubos cultivados em laboratório de volta às crianças doentes
Para verificar se essas observações de laboratório se relacionam com a doença real, os pesquisadores examinaram tecido hepático de crianças com atresia biliar e de outras condições hepáticas pediátricas. Usando sondas sensíveis, eles detectaram DNA de HCMV em colangiócitos — as células dos ductos biliares — em cerca de dois terços das amostras de atresia biliar, mas com muito menos frequência em fígados sem atresia biliar. Nas mesmas regiões onde o DNA viral foi encontrado, as células dos ductos biliares exibiram níveis mais altos de TGF‑beta e N‑cadherina, compatíveis com o padrão de transição e fibrose observado nos organoides. Isso sugere que, em pelo menos um subconjunto de crianças, o HCMV infecta diretamente os colangiócitos e os orienta para um estado fibrótico ao ativar vias mediadas por TGF‑beta.
O que isso significa para entender e tratar doenças dos ductos biliares
Em termos simples, este trabalho mostra que um vírus comum pode invadir as células que revestem os ductos biliares, afrouxar suas conexões apertadas e empurrá‑las rumo a uma identidade cicatricial e menos especializada por meio de um sinal baseado em TGF‑beta. Essas alterações enfraquecem as funções de barreira e transporte dos ductos e podem contribuir para os ductos biliares obstruídos e fibróticos observados em doenças como a atresia biliar. Embora nem todo caso de doença dos ductos biliares seja causado por HCMV, o estudo reforça a ideia de que, em lactentes vulneráveis, a infecção viral pode ser uma peça importante do quebra‑cabeça — e que direcionar vias relacionadas ao TGF‑beta pode, algum dia, ajudar a proteger ou restaurar ductos biliares frágeis.
Citação: Ye, Z., Hu, X., Rahaman, S.M. et al. HCMV infection disrupts barrier functions and promotes epithelial–mesenchymal transition in a cholangiocyte organoid model. Nat Commun 17, 2273 (2026). https://doi.org/10.1038/s41467-026-68962-8
Palavras-chave: citomegalovírus, atresia biliar, organoides do ducto biliar, transição epitelial mesenquimal, sinalização TGF-beta