Clear Sky Science · pt
Compreendendo a promoção por metais alcalinos na catálise de hidrogenação por meio da Interação Forte Metal–Base
Por que ajustar catalisadores importa para o cotidiano
Converter moléculas simples, como dióxido de carbono e hidrogênio, em combustíveis e produtos químicos úteis é fundamental para uma energia mais limpa e uma indústria mais sustentável. Muitos dos catalisadores metálicos que impulsionam essas reações já contêm pequenas quantidades de metais alcalinos, como sódio ou potássio, atuando como “promotores”, mas o papel real desses aditivos tem sido surpreendentemente obscuro. Este estudo revela um princípio unificador sobre como esses aditivos realmente funcionam, oferecendo um caminho para projetar catalisadores mais inteligentes que direcionem reações para produtos desejados e reduzam resíduos.
Um olhar mais atento em catalisadores reforçados
Catalisadores feitos de metais de transição, como ródio e níquel, apoiam‑se em suportes sólidos e ajudam a quebrar e refazer ligações químicas. Por décadas, a indústria tem adicionado metais alcalinos para tornar esses catalisadores mais ativos, seletivos ou duráveis. As explicações usuais focavam em efeitos geométricos simples (mudança na forma e tamanho das partículas) ou na doação direta de elétrons do metal alcalino para o metal ativo. No entanto, em condições operacionais reais esses promotores existem principalmente como óxidos, e não como átomos metálicos nus, o que torna a transferência direta de elétrons uma imagem incompleta.
Descobrindo uma parceria forte na superfície
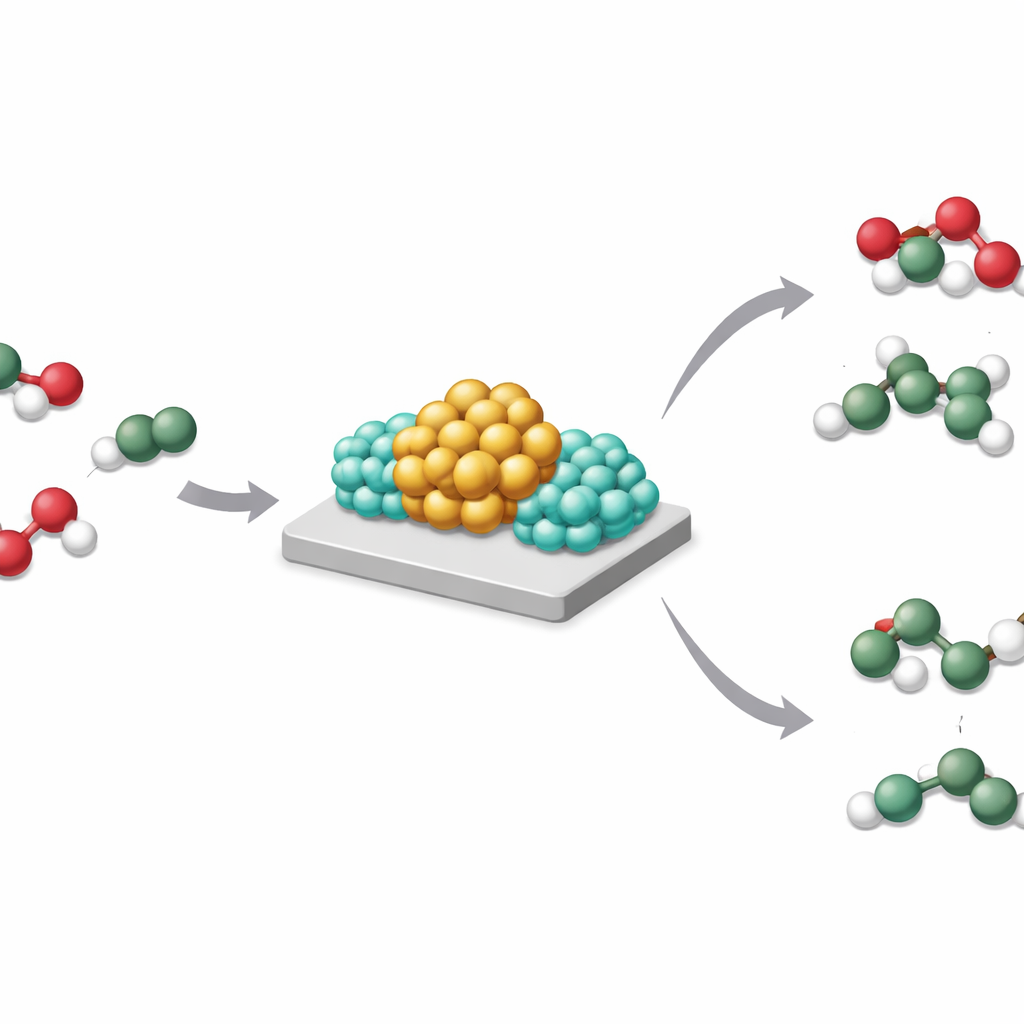
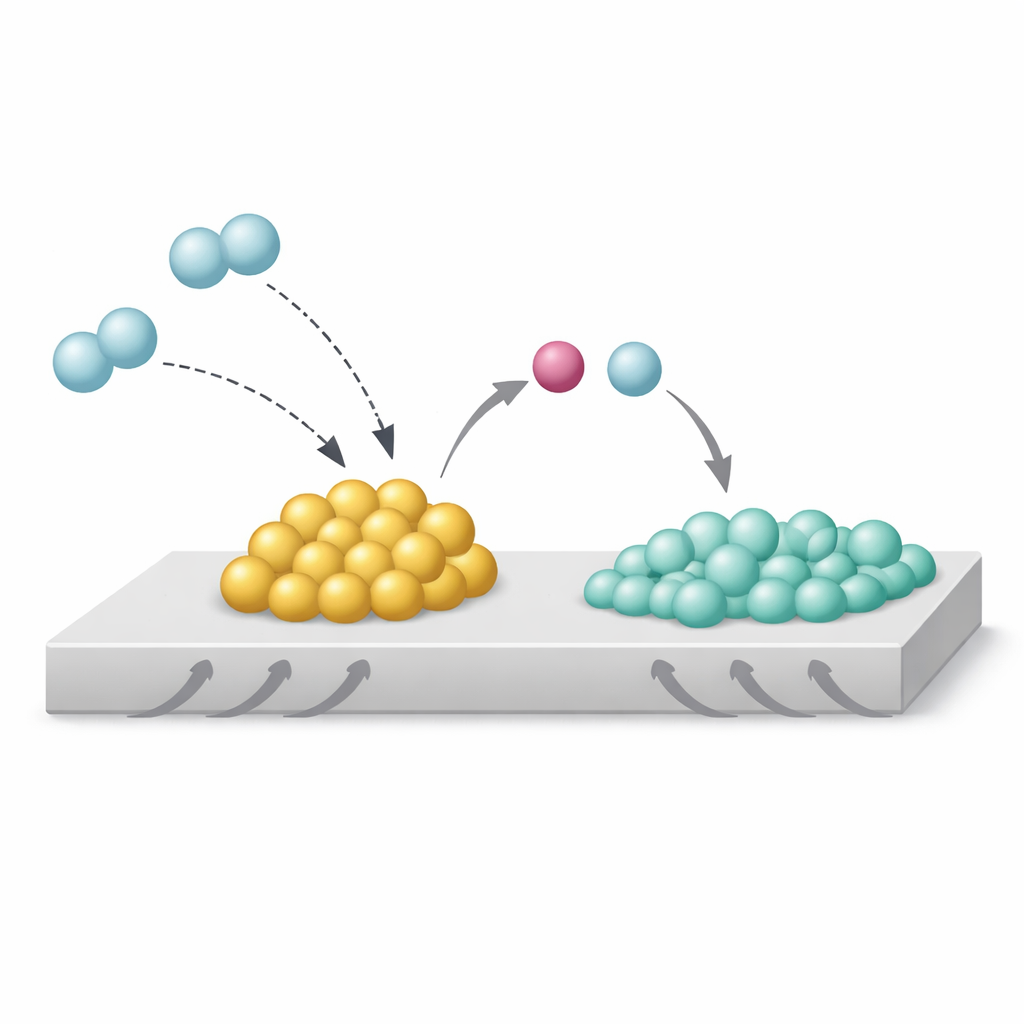
Os autores estudaram um sistema modelo: nanopartículas de ródio sobre dióxido de titânio, com e sem adição de sódio. Usando microscopia eletrônica avançada, espectroscopia de raios X e simulações computacionais, eles descobriram que o sódio se posiciona como óxido, Na₂O, exatamente na borda onde as partículas de ródio tocam o suporte. Sob hidrogênio, esse arranjo cria o que chamam de Interação Forte Metal–Base, ou SMBI. Nesses pontos de contato especiais, as moléculas de hidrogênio que chegam se rompem de forma heterolítica: o Na₂O, mais básico, captura a parte semelhante a próton, enquanto o ródio retém o parceiro rico em elétrons. Essa clivagem deixa a superfície de ródio incomumente rica em elétrons e impede que o hidrogênio se espalhe, ou “transborde”, para o suporte de dióxido de titânio.
Como esse efeito oculto direciona reações
Essa reformulação sutil de onde o hidrogênio e os elétrons ficam tem grandes consequências. Na hidrogenação de dióxido de carbono, ródio simples sobre dióxido de titânio favorece a hidrogenação intensa até metano. Quando o sódio é adicionado, o mesmo catalisador passa a produzir principalmente monóxido de carbono, um bloco de construção valioso, enquanto gera muito menos metano. Comportamento semelhante ocorre com lítio ou potássio, ou quando o ródio é substituído por níquel. Os autores mostram que, quando o hidrogênio pode transbordar livremente para o suporte, a hidrogenação profunda domina; quando a SMBI mantém o hidrogênio concentrado na fronteira metal–base e fora do suporte, produtos mais brandos são favorecidos.
Diferentes duplas ligações, resultados diferentes
Em seguida, a equipe investigou como a SMBI afeta reações de hidrogenação orgânica comuns envolvendo ligações duplas carbono–carbono, carbono–oxigênio e nitrogênio–oxigênio. Para uma dupla ligação carbono–carbono em acetato de vinila, a promoção com sódio torna o catalisador mais rápido, provavelmente porque o ródio rico em elétrons ajuda a enfraquecer essa ligação enquanto o hidrogênio, menos fortemente ligado, se adiciona eficientemente. Em contraste, para moléculas como acetofenona e nitrobenzeno, cujos grupos reativos preferem se acomodar no suporte de óxido, a mesma adição de sódio desacelera a reação. Aqui, o hidrogênio transbordado suprimido significa que o suporte não recebe hidrogênio suficiente para impulsionar essas transformações, mostrando que nem todas as duplas ligações se beneficiam igualmente do mesmo efeito promotor.
Projetando catalisadores com controle intencional
Combinando experimentos e teoria, os autores argumentam que a SMBI fornece uma maneira unificada de entender como promotores de metais alcalinos remodelam superfícies catalíticas. Em vez de agir como simples doadores de elétrons, os óxidos alcalinos atuam como fortes armadilhas de prótons, forçando o hidrogênio a se dividir de maneira polarizada e confinando o hidrogênio reativo próximo à interface metal–base. Essa percepção explica tendências enigmáticas em muitas reações de hidrogenação e metais, e aponta para uma regra prática de projeto: ao ajustar quanto e onde os óxidos alcalinos são colocados ao redor das partículas metálicas, os químicos podem deliberadamente direcionar reações para produtos específicos enquanto otimizam atividade e estabilidade para processos químicos mais limpos.
Citação: Jung, M., Dickieson, M.P., Chen, P. et al. Understanding alkali metal promotion in hydrogenation catalysis through Strong Metal–Base Interaction. Nat Commun 17, 2465 (2026). https://doi.org/10.1038/s41467-026-68952-w
Palavras-chave: catálise de hidrogenação, promotores de metais alcalinos, conversão de CO2, catalisadores heterogêneos, interfaces metal–óxido