Clear Sky Science · pt
Um inibidor alostérico da protease NS2B-NS3 do vírus Zika com eficácia oral em modelos de camundongos
Uma nova forma de superar um vírus perigoso
O vírus Zika ganhou as manchetes globais há uma década, quando infecções em gestantes foram associadas a bebês nascidos com cabeça anormalmente pequena e danos cerebrais. Ainda hoje não existe medicamento aprovado para tratar ou prevenir o Zika. Este estudo descreve um novo composto tipo comprimido promissor que desativa uma enzima viral chave de maneira inesperada e protege camundongos de infecções graves por Zika, apontando para um possível futuro remédio que poderia um dia proteger pessoas vulneráveis, especialmente durante surtos.
Por que o Zika ainda importa
O vírus Zika é transmitido principalmente por mosquitos Aedes e pertence à mesma família dos vírus da dengue e do Nilo Ocidental. A maioria das pessoas infectadas apresenta poucos ou nenhum sintoma, mas cerca de um em cada cinco desenvolve problemas que variam de febre e erupção cutânea a complicações sérias, como danos oculares, falência de órgãos e distúrbios do sistema nervoso. O maior perigo é para os fetos: a infecção durante a gravidez pode causar microcefalia e deficiência ao longo da vida. Como não há vacina ou tratamento antiviral aprovado, os médicos só podem oferecer cuidados de suporte. Por isso, os cientistas consideram o Zika uma prioridade para preparo pandêmico, buscando drogas que possam proteger populações em risco e conter novos surtos.
Caçando pontos fracos ocultos
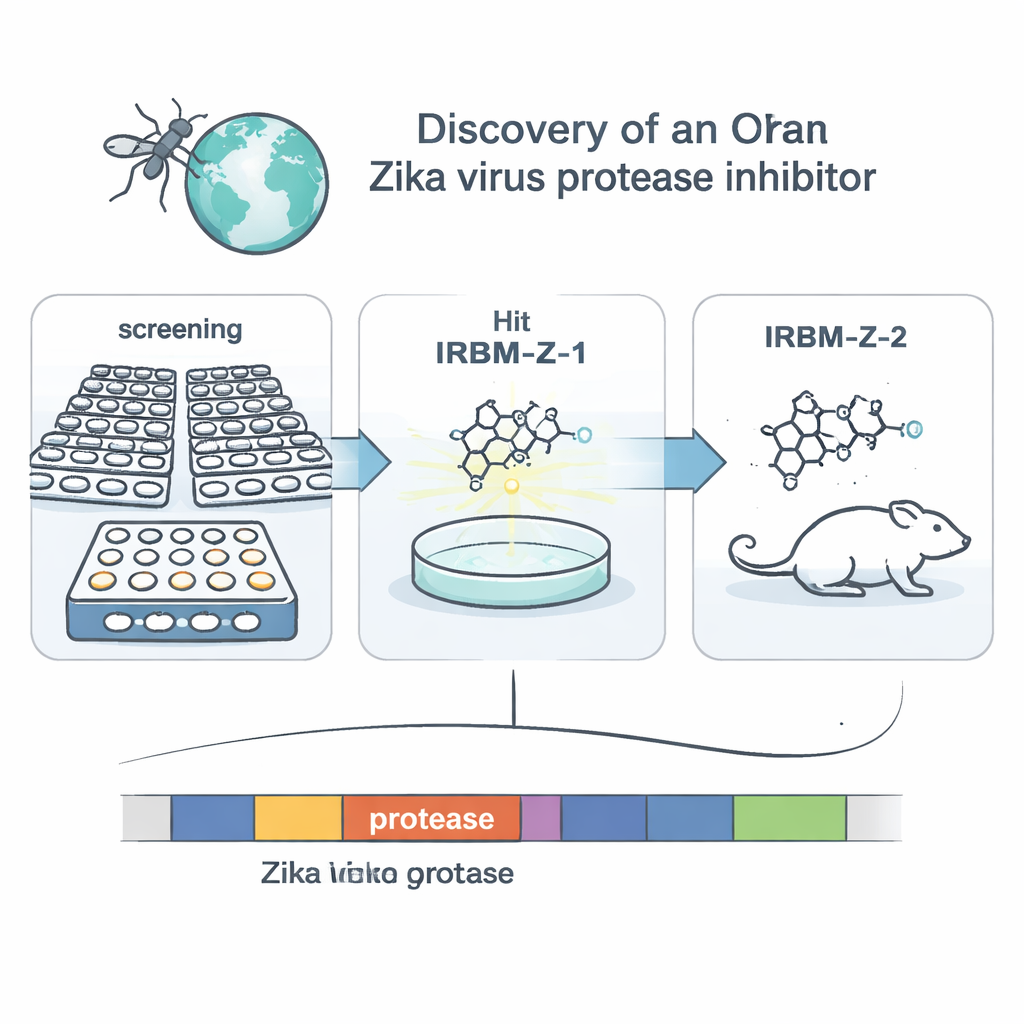
Os pesquisadores concentraram-se em uma enzima viral chamada protease NS2B–NS3. Essas “tesouras” moleculares cortam a grande proteína inicial do vírus nos pedaços necessários para montar novos vírus, tornando-a um alvo atraente para drogas. Em vez de desenvolver um fármaco para o local óbvio de corte, a equipe usou um sistema de triagem baseado em células que imita a replicação do Zika dentro de células de rim de macaco. Eles construíram um genoma Zika modificado, ou replicon, que carece de genes estruturais, mas carrega um repórter luciferase para que a emissão de luz acompanhe a cópia viral. Triando mais de 120.000 pequenas moléculas de uma biblioteca química nacional, selecionaram aquelas que reduziram fortemente o sinal de luz sem prejudicar as células e então cultivaram replicons virais que se tornaram resistentes a cada composto ativo. Essa investigação genética apontou para a protease como alvo-chave de uma família de compostos, liderada por uma molécula inicial chamada IRBM-Z-1.
Trancando a enzima na forma errada
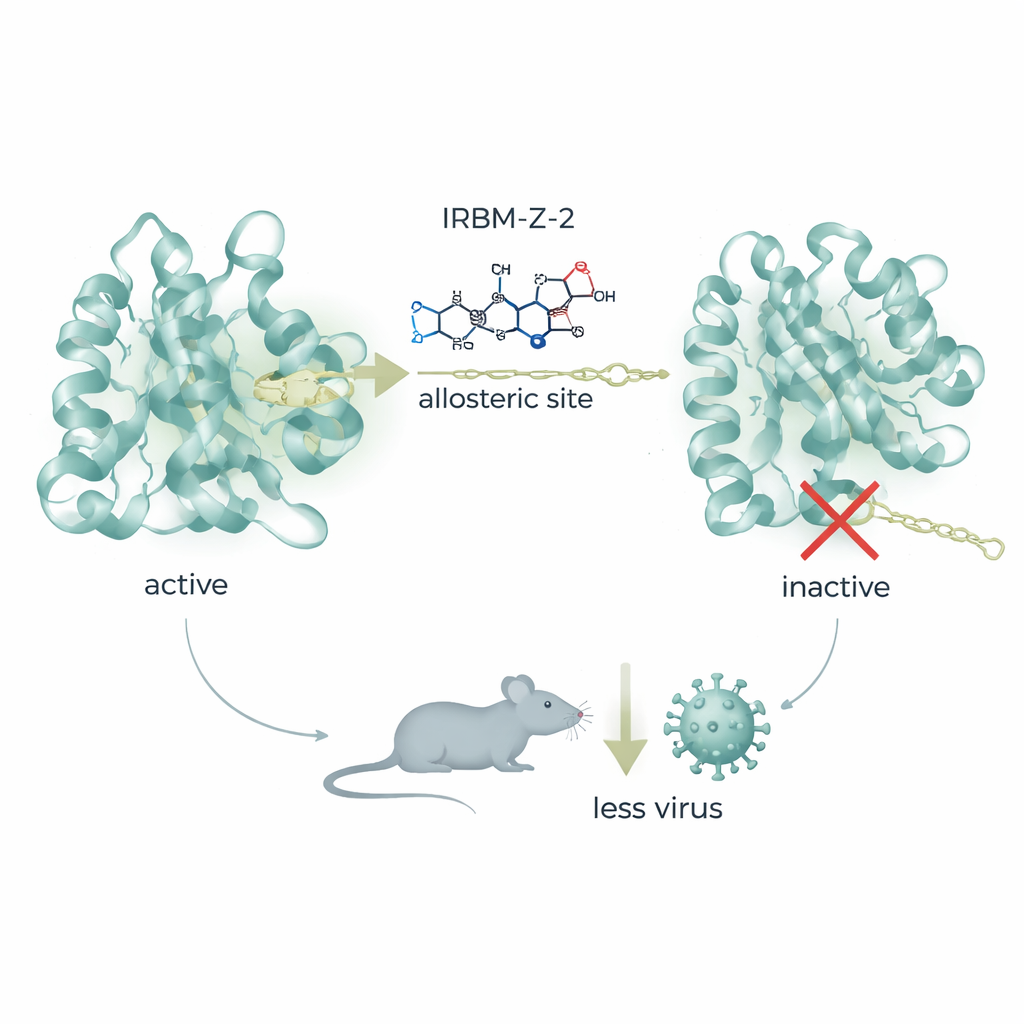
Testes bioquímicos mostraram que o IRBM-Z-1 não competia com o substrato usual no sítio de corte. Em vez disso, ele se comportou como um inibidor não competitivo, ou alostérico — ligando-se em um bolso separado e impedindo que a enzima adotasse sua forma ativa. Cristalografia de raios X de alta resolução revelou que o composto aninha-se em um bolso até então desconhecido, distante do centro catalítico. Ali, seu núcleo incomum “N-acilsidnona imina” forma uma rede de ligações de hidrogênio e interações de empilhamento que empurram uma região-chave da protease para uma conformação aberta e inativa. Uma única mudança de aminoácido nessa região, na posição 156, torna o vírus resistente, ressaltando o quão precisamente o composto explora esse sítio oculto. Esse bolso também difere dos sítios alostéricos descritos em flavivírus relacionados, oferecendo um ponto de apoio genuinamente novo para o design de drogas.
Do composto ativo ao fármaco protetor em camundongos
Guiada por informações estruturais, a equipe refinou o IRBM-Z-1 para uma molécula mais potente chamada IRBM-Z-2. Esse composto aprimorado bloqueia a protease do Zika em concentrações nanomolares, inibe fortemente a replicação viral em vários tipos celulares e mostra atividade contra proteases relacionadas da dengue e do Nilo Ocidental, poupando enzimas humanas. Em estudos animais, o IRBM-Z-2 exibiu comportamento “semelhante a um fármaco” favorável: foi estável no organismo, teve boa absorção oral e manteve níveis sanguíneos bem acima dos necessários para bloquear o vírus, sem sinais claros de toxicidade. Em camundongos AG129 altamente suscetíveis infectados com Zika, o tratamento diário — por injeção ou por via oral — reduziu dramaticamente a quantidade de RNA viral no sangue, preveniu perda de peso e sintomas da doença, e permitiu que todos os animais tratados sobrevivessem, enquanto os controles não tratados sucumbiram à infecção.
O que isso pode significar para futuros surtos
Em conjunto, esses achados apresentam uma nova classe de antivirais contra Zika que funcionam ao congelar uma enzima viral crítica em uma pose inativa, em vez de bloquear diretamente seu sítio ativo. Como o IRBM-Z-2 pode ser administrado por via oral, mostra forte proteção em modelos rigorosos de camundongo e até agora tem um perfil de segurança limpo, ele se destaca como um candidato promissor para desenvolvimento adicional como droga preventiva — potencialmente para proteger gestantes, profissionais de saúde e viajantes caso o Zika resurja. Mais amplamente, o bolso alostérico recém-descoberto pode inspirar drogas semelhantes contra vírus relacionados, abrindo uma nova frente na luta contra doenças transmitidas por mosquitos.
Citação: Ontoria, J.M., Torrente, E., Missineo, A. et al. An allosteric inhibitor of the Zika virus NS2B-NS3 protease with oral efficacy in mouse models. Nat Commun 17, 1439 (2026). https://doi.org/10.1038/s41467-026-68943-x
Palavras-chave: Vírus Zika, droga antiviral, inibidor de protease, modulação alostérica, doença transmitida por mosquitos