Clear Sky Science · pt
FCHo2, não talina, permite a ativação inside-out da integrina ɑvβ5 em adesões curvas
Como as células percebem a forma do entorno
Nossos corpos são formados por células que constantemente se agarram ao ambiente ao redor, puxando e empurrando para mover-se, dividir-se ou permanecer no lugar. Este artigo revela que as células não apenas sentem a rigidez do ambiente — elas também leem sua forma. Ao descobrir um sistema adesivo específico que é ativado apenas onde a membrana celular está fortemente curvada, os autores mostram que as células usam “apertos” internos diferentes para superfícies planas versus ambientes fibrilares, com implicações importantes para como os tecidos se formam e como os cânceres se espalham.
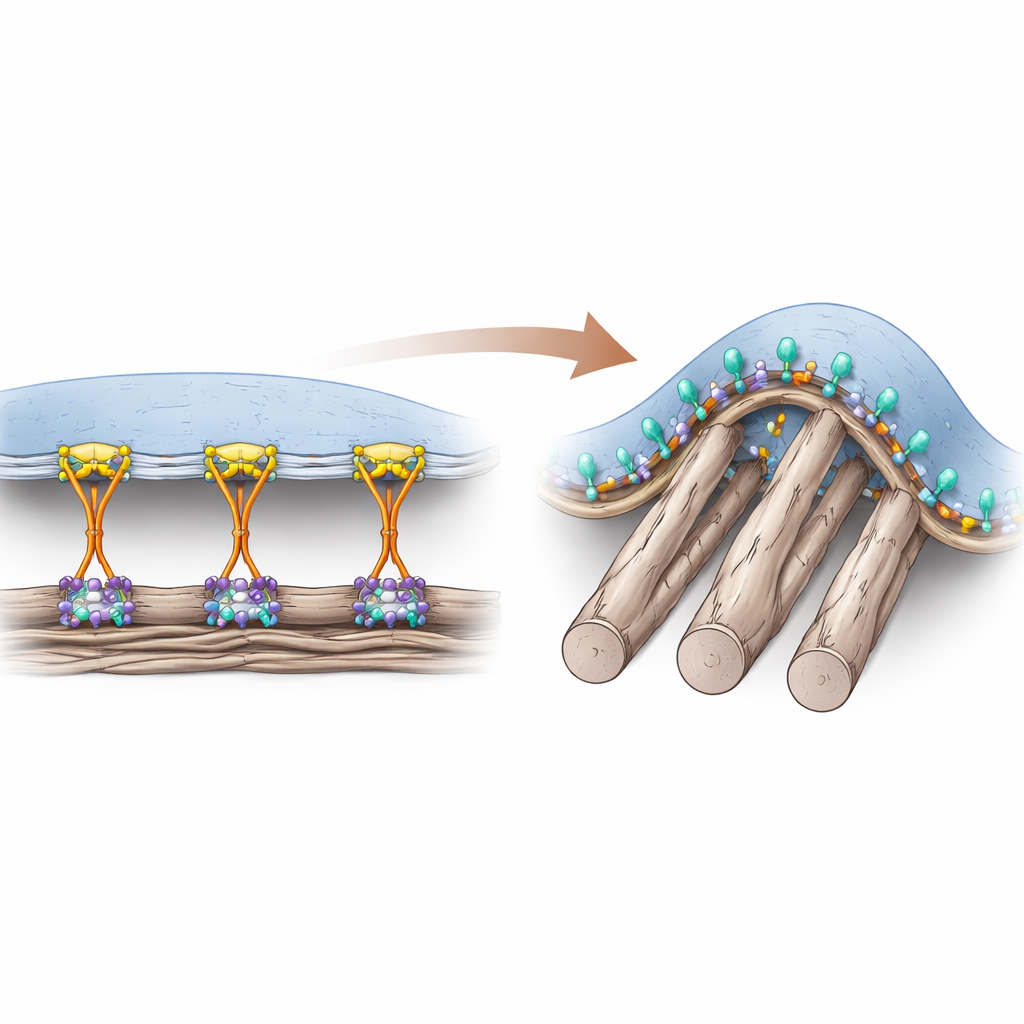
Duas maneiras de as células se prenderem
As células se ligam ao material rico em proteínas ao redor delas usando receptores de superfície chamados integrinas. Por anos, os pesquisadores supuseram que uma proteína auxiliar chamada talina era absolutamente essencial para ativar as integrinas “de dentro” da célula, permitindo uma ligação forte em locais de ancoragem clássicos conhecidos como adesões focais. Essas adesões se formam principalmente em superfícies planas e rígidas e transmitem grandes forças de tração através do citoesqueleto. No entanto, em tecidos vivos, muitas das fibras ao redor são macias e cilíndricas, criando pontos de contato curvos que não sustentam facilmente essas estruturas que exigem muita força. Os autores já haviam identificado um tipo diferente de estrutura adesiva, chamada adesão curva, que surge exatamente onde a membrana contorna fibras finas e que depende de uma integrina específica, αvβ5.
Apertos curvos usam um auxiliar diferente
No novo estudo, a equipe demonstra que a talina, embora ainda presente, não é o ativador chave da integrina αvβ5 em adesões curvas. Em vez disso, uma proteína sensora de curvatura chamada FCHo2 assume esse papel. Usando barras e pilares em escala nanométrica projetados com precisão para dobrar membranas celulares de forma controlada, eles observaram que αvβ5 se agrupa fortemente em regiões curvadas, mas apenas quando FCHo2 pode ligar-se a uma sequência muito curta — um motivo HDRRE — logo dentro da célula, na cauda β5. Quando esse motivo é perturbado, a integrina ainda funciona em adesões focais, mas não consegue mais formar adesões curvas. A redução de FCHo2 deixa as adesões focais clássicas em grande parte intactas, porém elimina as adesões curvas, enquanto a remoção da talina enfraquece severamente as adesões focais e deixa as adesões curvas amplamente inalteradas.
Um único resíduo de aminoácido como seletor de forma
Um mistério era por que uma integrina estreitamente relacionada, αvβ3, não pode formar adesões curvas embora sua cauda interna se pareça muito com a de β5. Ao trocar domínios entre as duas integrinas e introduzir mutações pontuais, os autores identificaram uma posição crucial próxima ao sítio de ligação da talina: a maioria das integrinas β tem um triptofano (W), mas β5 é única por possuir uma tirosina (Y766). Quando a tirosina de β5 foi substituída por triptofano, a integrina perdeu a capacidade de participar de adesões curvas e passou a comportar-se mais como β3, favorecendo apenas adesões focais. A mudança inversa — inserindo uma tirosina na quimera no estilo β3 — restaurou a sensibilidade à curvatura. Experimentos adicionais com variantes que mimetizam os estados fosforilado ou não fosforilado dessa tirosina sugerem que sua modificação química pode inclinar a integrina para adesões focais planas e de alta força ou para adesões curvas de baixa força.
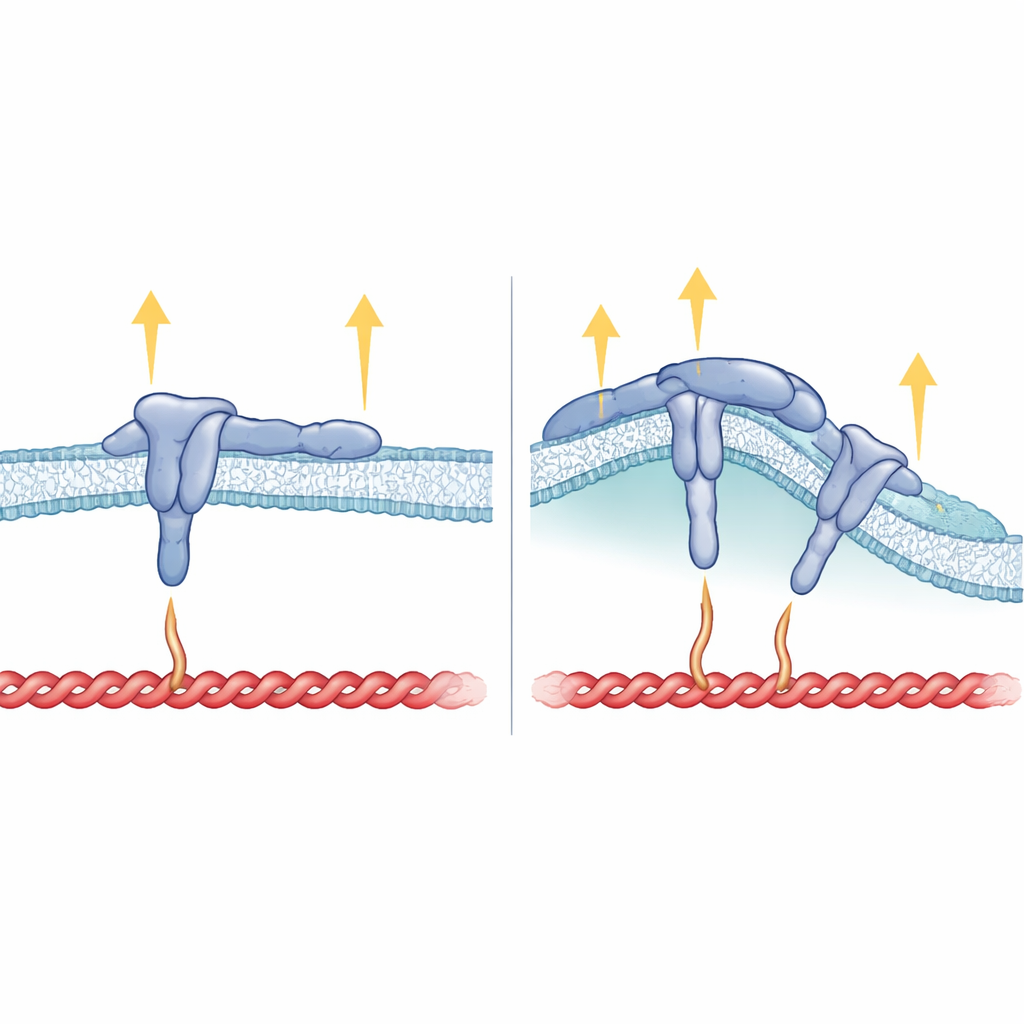
Como forma de membrana, estrutura da integrina e força se relacionam
Além da cauda interna, o trecho de β5 que atravessa a membrana também se mostrou crítico. Quando os pesquisadores substituíram o segmento transmembrana de β5 pelo de β3, a integrina resultante ainda pôde formar adesões focais, mas deixou de preferir sítios curvos e não mais seguia FCHo2. Isso sugere que a maneira como a integrina se assenta na membrana ajuda a orientar o motivo HDRRE para que FCHo2 possa se prender em regiões curvadas e estabilizar a αvβ5 ativa ligada ao ligante. Em adesões curvas, a talina parece tocar apenas uma parte mais distante da cauda da integrina e não suporta alta tensão, o que explica por que outros componentes que demandam força, como vinculina, tensina e kindlina, estão em grande parte ausentes ali. Em contraste, nas adesões focais, a talina prende tanto locais próximos quanto distantes na cauda e na membrana, suportando fortes forças de tração, mas bloqueando o acesso de FCHo2 à mesma região.
O que isso significa para o comportamento celular
Para um observador leigo, a mensagem deste trabalho é que as células dispõem de dois “modos de aperto” separados para se fixar ao entorno. Em áreas planas e rígidas, elas usam adesões focais dirigidas por talina, construídas para puxar com força. Em estruturas macias, fibrilares e curvas, elas mudam para adesões curvas dirigidas por FCHo2, que estabilizam a integrina αvβ5 com força muito menor. Uma mudança minúscula na sequência da integrina — e se esse sítio está quimicamente modificado — ajuda a decidir qual modo será usado. Esse sistema duplo permite que as células interpretem tanto a rigidez quanto a forma em ambientes tridimensionais, influenciando como migram, organizam tecidos e, potencialmente, como invadem durante doenças.
Citação: Lu, CH., Lee, C.E., Zhang, W. et al. FCHo2, not talin, enables inside-out activation of integrin ɑvβ5 in curved adhesions. Nat Commun 17, 2419 (2026). https://doi.org/10.1038/s41467-026-68942-y
Palavras-chave: integrinas, adesão celular, curvatura da membrana, FCHo2, citoesqueleto