Clear Sky Science · pt
Expansão clonal de células T CD8⁺ citotóxicas associada à ARIA por lecanemabe
Por que isso importa para pessoas com Alzheimer
O lecanemabe é um dos primeiros medicamentos capazes de limpar a amiloide do cérebro e retardar modestamente a perda de memória na doença de Alzheimer. Contudo, alguns pacientes em terapia desenvolvem inchaço cerebral ou pequenos sangramentos cerebrais, alterações visíveis em ressonâncias magnéticas agrupadas sob o termo anomalias de imagem relacionadas à amiloide (ARIA). Este estudo aborda uma pergunta crucial para pacientes e familiares: o que está acontecendo no sistema imunológico quando a ARIA surge, e será que um simples exame de sangue um dia poderia ajudar a prever quem tem maior risco?
A promessa e o risco de um novo tratamento para Alzheimer
O lecanemabe é um anticorpo administrado por infusão que mira aglomerados de uma proteína chamada beta‑amiloide, uma marca da doença de Alzheimer. Ao ajudar o organismo a remover a amiloide, ele pode retardar modestamente o declínio cognitivo. Porém, esse benefício vem acompanhado de uma preocupação de segurança: algumas pessoas desenvolvem ARIA, que pode incluir regiões de edema cerebral ou hemorragias pontuais. Esses efeitos colaterais exigem monitoramento frequente por ressonância magnética e podem limitar quem recebe o fármaco. Nem todos são igualmente vulneráveis—portadores de uma variante genética chamada APOE4 têm risco maior—mas os genes sozinhos não explicam por que a ARIA ocorre, especialmente logo após o início do tratamento. Como o lecanemabe é administrado pela corrente sanguínea, os autores raciocinaram que observar mais de perto as células imunes no sangue poderia revelar sinais de alerta precoces ou mesmo mecanismos que liguem o tratamento a lesões vasculares no cérebro. 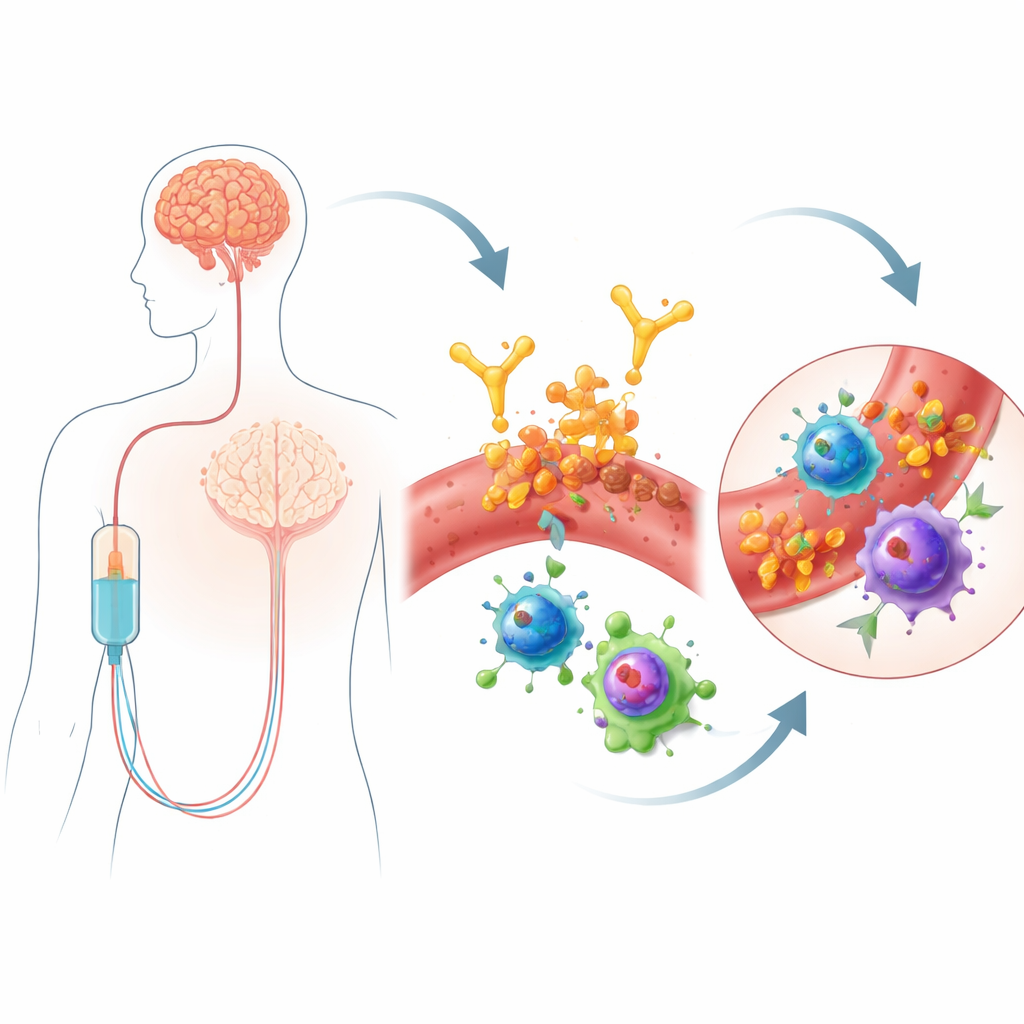
Monitorando células imunes em pacientes que desenvolveram e não desenvolveram ARIA
Os pesquisadores estudaram seis pessoas com Alzheimer recebendo lecanemabe em uma clínica regional de memória. Três desenvolveram diferentes formas de ARIA, e três pacientes pareados (semelhantes em idade, sexo, genótipo APOE e número de infusões) não desenvolveram. Amostras de sangue foram colhidas imediatamente antes das infusões, e a equipe usou uma abordagem intensiva “multiômica”: sequenciamento de RNA de célula única para ler quais genes estavam ativos em milhares de células imunes individuais, marcas baseadas em anticorpos para definir tipos celulares, sequenciamento de receptores de células T para rastrear clones, e metabolômica direcionada para medir centenas de pequenas moléculas envolvidas no metabolismo celular. Isso permitiu investigar não apenas quais tipos celulares estavam presentes, mas quão ativos estavam, que combustível estavam usando e se famílias específicas de células T se expandiam em resposta a algum gatilho.
Expansão de células T assassinas altamente armadas
Um padrão claro emergiu nos pacientes que desenvolveram ARIA. Em comparação com os controles, eles apresentaram uma proporção maior de células T CD8 “assassinas” e menos células T CD4 auxiliares. Dentro do conjunto de CD8, destacaram‑se dois subgrupos: células de memória efetora e uma forma terminalmente diferenciada conhecida como células TEMRA. Essas células TEMRA são como soldados veteranos—altamente especializadas para ataque, com forte maquinário para matar células‑alvo. Em pacientes ARIA‑positivos, as TEMRA eram mais numerosas, mais clonally expandidas (isto é, famílias específicas de células T haviam se multiplicado) e exibiam programas genéticos associados à citotoxicidade, migração através de vasos sanguíneos e sinais de estimulação crônica. Estados similares de células T já foram observados no envelhecimento, em infecções crônicas, na esclerose múltipla e no líquido cefalorraquidiano de pessoas com Alzheimer, onde podem se acumular perto de vasos sanguíneos e da superfície do cérebro.
Reprogramação metabólica e comunicação com outras células imunes
A equipe também constatou que essas células efetoras CD8 reprogramaram seu metabolismo. Em vez de dependerem principalmente da produção eficiente de energia nas mitocôndrias, elas migraram para a glicólise, uma via mais rápida, porém menos eficiente, que sustenta atividade de alta intensidade e curta duração. Medições de metabólitos em células sanguíneas corroboraram isso: níveis de lactato e piruvato estavam aumentados, enquanto componentes chave do ciclo do ácido cítrico estavam reduzidos, um padrão típico de células imunes inflamatórias. Monócitos, outro tipo de leucócito, mostraram mudanças complementares. Em pacientes ARIA‑positivos, monócitos ligaram genes para apresentação de antígenos, adesão a outras células e produção de quimiocinas—sinais químicos que atraem células T. Modelagens computacionais de pares ligante‑receptor sugeriram que monócitos estavam enviando sinais mais fortes de ativação e direcionamento às células efetoras CD8, criando um ambiente que encoraja essas células assassinas a interagir com as paredes dos vasos sanguíneos.
Códigos de endereço que direcionam células T aos vasos cerebrais
Como este estudo amostrou apenas o sangue, os autores recorreram a um conjunto de dados independente de célula única proveniente de cérebros de pacientes tratados com lecanemabe para investigar se os mesmos programas de células T se associavam a nichos vasculares no cérebro. Quando projetaram seus subconjuntos de CD8 nesse mapa cerebral, as células TEMRA e de memória efetora de pacientes ARIA‑positivos exibiram “códigos de endereço” transcricionais—combinações de moléculas de adesão e receptores de quimiocinas—que correspondiam a células endoteliais (vasos sanguíneos) no cérebro doente. Essas assinaturas sugerem que as células T assassinas expandidas não só estão altamente armadas e metabolicamente ativadas, mas também prontas para se direcionar e interagir com vasos cerebrais estressados em locais de depuração de amiloide. 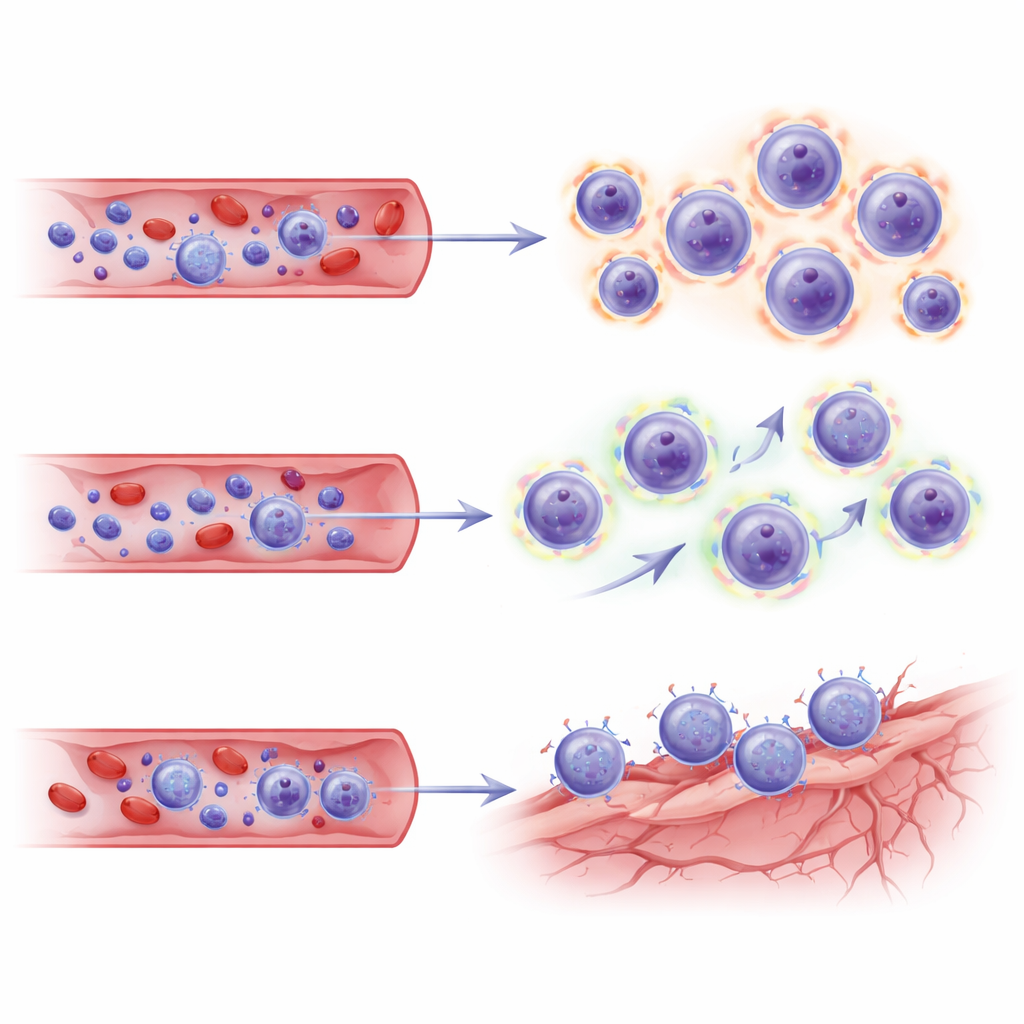
O que isso pode significar para pacientes e cuidados futuros
No conjunto, este estudo pequeno, porém detalhado, pinta a ARIA como algo além de um efeito colateral passivo da remoção de amiloide. Em vez disso, parece ligada a uma resposta imune coordenada no sangue: expansão e ativação metabólica de clones específicos de células T assassinas, sinalização reforçada de monócitos e características moleculares que favorecem o engajamento com vasos sanguíneos cerebrais. O trabalho não prova que essas células causam a ARIA—as mudanças imunes podem ser reação à lesão vascular e não sua origem—mas fornece hipóteses testáveis e um roteiro para biomarcadores baseados em sangue. No futuro, medir a abundância e o estado metabólico de células CD8 TEMRA, junto com moléculas sinalizadoras chave, pode ajudar a identificar pacientes com maior risco de ARIA, orientar cronogramas de monitoramento ou até inspirar estratégias direcionadas para reduzir temporariamente essa resposta imune preservando os benefícios das terapias que limpam a amiloide.
Citação: Johnson, L.A., Saito, K., Pallerla, A.V. et al. Clonal expansion of cytotoxic CD8⁺ T cells in lecanemab-associated ARIA. Nat Commun 17, 2180 (2026). https://doi.org/10.1038/s41467-026-68921-3
Palavras-chave: Doença de Alzheimer, lecanemabe, células imunes, vasos sanguíneos cerebrais, efeitos colaterais do tratamento