Clear Sky Science · pt
Proteínas TMEM63 atuam como scramblases de lipídios ativadas mecanicamente e moduladas por colesterol, contribuindo para a mecano-resiliência da membrana
Como as células permanecem intactas sob estresse físico
As células do nosso corpo são constantemente comprimidas, esticadas e agitadas, seja em corações batendo, músculos em atividade ou tumores empurrando o tecido. Este estudo revela como uma família de proteínas de membrana, chamada OSCA/TMEM63, ajuda as células a sobreviver a forças mecânicas intensas ao reorganizar os lipídios de sua camada externa. Compreender esse sistema amortecedor embutido pode abrir novas perspectivas sobre distúrbios da audição, da mielinização e até da disseminação do câncer.
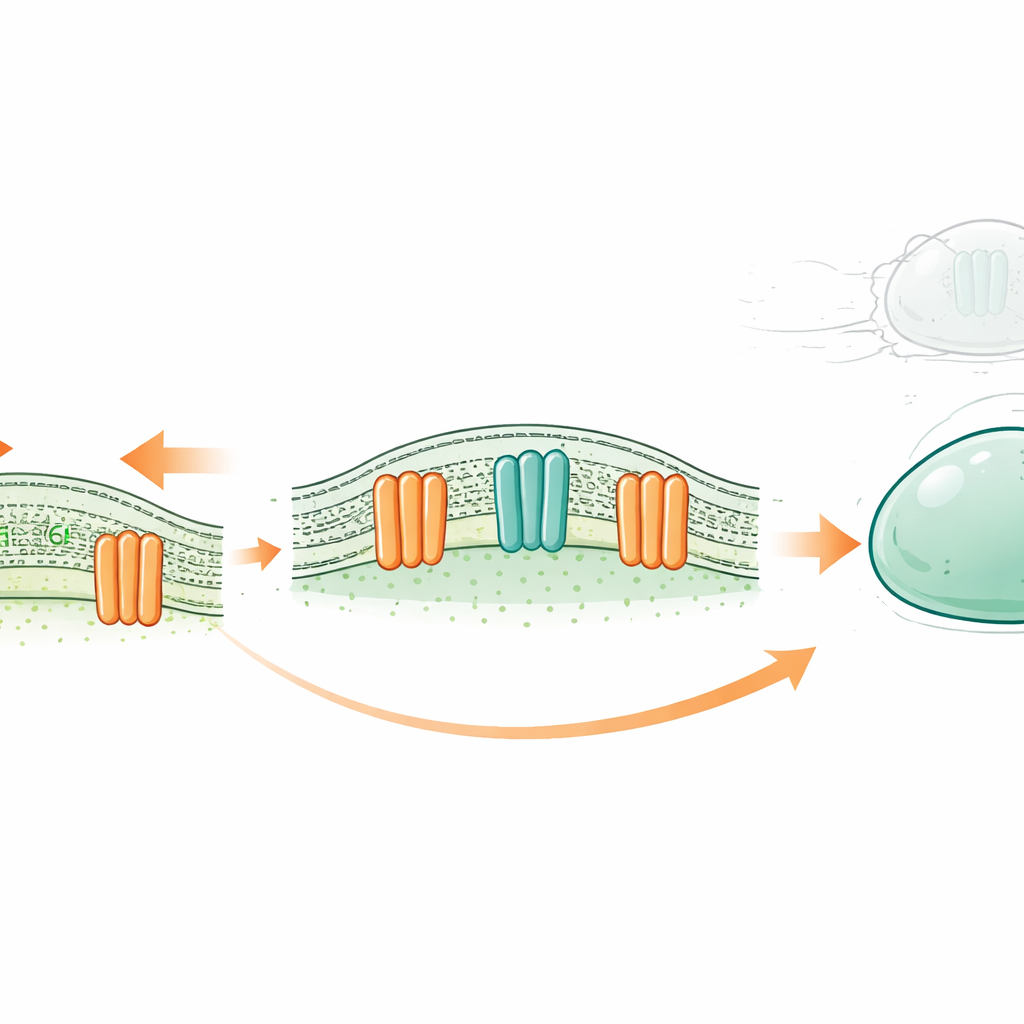
Um novo tipo de amortecedor celular
Cada célula é envolta por uma membrana oleosa fina composta por duas camadas de moléculas semelhantes a gorduras chamadas lipídios. Tradicionalmente, certas proteínas de membrana eram vistas apenas como canais iônicos — pequenas válvulas que deixam íons entrarem e saírem em resposta a estímulos como o estiramento. A família OSCA/TMEM63, encontrada de plantas a humanos, é conhecida por abrir em resposta à tensão na membrana. Trabalhos estruturais anteriores sugeriram que, ao contrário dos canais clássicos, seus poros são parcialmente revestidos por lipídios. Isso levantou uma possibilidade provocativa: será que esses canais também atuam como “scramblases”, invertendo lipídios entre as camadas interna e externa da membrana quando a célula está sob força?
Observando lipídios atravessarem a membrana
Para testar essa ideia, os autores combinaram simulações computacionais com sistemas experimentais reducionistas montados a partir de componentes purificados. Nas simulações, versões abertas de várias proteínas OSCA e TMEM63 foram inseridas em membranas modelo. Moléculas de lipídios moveram-se espontaneamente através de um sulco nessas proteínas, de um lado do bicamada para o outro, formando um cinturão que ligava as duas camadas enquanto deixava um caminho preenchido por água para íons. Em experimentos paralelos, a equipe construiu “bolhas” artificiais gigantes (vesículas) contendo lipídios fluorescentes e proteínas específicas. Quando um agente externo abafava a fluorescência na superfície externa, qualquer queda adicional no sinal só podia ser explicada por lipídios que haviam virado da camada interna para a externa. Vesículas contendo OSCA1.1, OSCA1.2, OSCA2.2 ou TMEM63A/B apresentaram essa perda extra de fluorescência, indicando scrambling ativo, enquanto canais de controle que não embaralham lipídios não o fizeram.
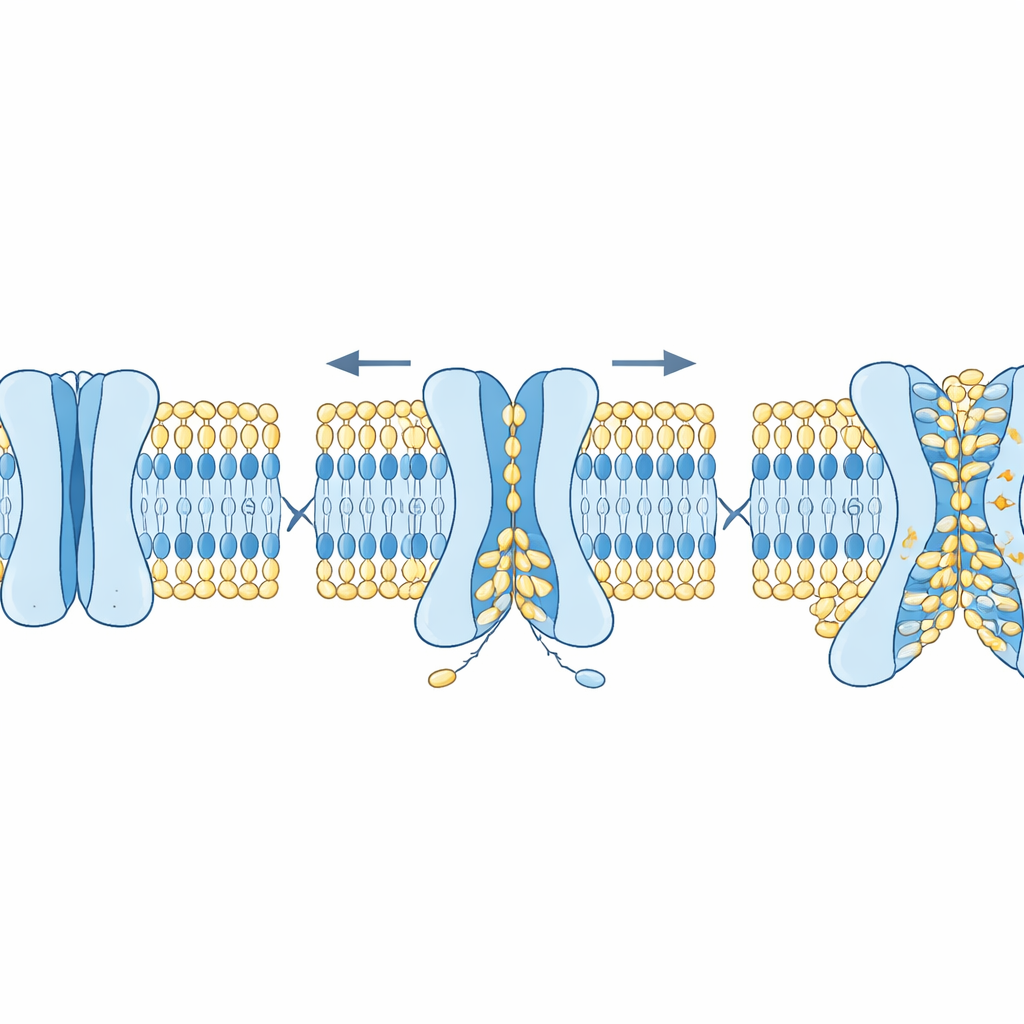
Como estrutura e colesterol regulam o processo
Os pesquisadores então investigaram quais características das proteínas TMEM63 controlam esse comportamento duplo. Usando AlphaFold2, geraram muitas conformações plausíveis das proteínas humanas TMEM63, variando de fechadas a progressivamente mais abertas. As simulações revelaram que um punhado de aminoácidos volumosos age como “gargalos” no sulco. Um resíduo limita principalmente o fluxo de íons, enquanto outros bloqueiam o movimento de lipídios. Mutar o gargalo de íons aumentou a condutância elétrica sem alterar muito o scrambling de lipídios, enquanto mutar o portão de lipídios fez com que os lipídios virassem com mais facilidade e até fez com que células exibissem sinais de “me coma” na superfície sem nenhum estímulo adicional. Outro regulador chave foi o colesterol, um componente que rigidifica as membranas celulares. Adicionar colesterol às membranas modelo retardou consideravelmente o scrambling de lipídios e estabilizou o estado fechado da TMEM63A, tanto em simulações quanto em estruturas por crio-microscopia eletrônica onde o colesterol se acomodava em sítios específicos da proteína.
Força mecânica como interruptor ligado
Se o colesterol normalmente mantém o scrambling sob controle dentro das células, o que o ativa no momento certo? A equipe usou moléculas em anel de açúcar chamadas ciclodextrinas para remover lipídios seletivamente das membranas e assim aumentar a tensão sem retirar o colesterol. Em vesículas do tamanho de células, a adição de ciclodextrina ativou o scrambling de lipídios pela TMEM63A apenas quando a proteína estava presente, provando que o estresse mecânico por si só pode disparar a inversão. Abordagens semelhantes em células vivas mostraram que a remoção leve de colesterol por si só não foi suficiente; foi necessário um desafio mecânico subsequente para observar scrambling robusto. Quando células geneticamente modificadas para expressar TMEM63A foram esticadas repetidamente, expuseram rapidamente certos lipídios na superfície externa — uma marca registrada do scrambling — enquanto células sem essas proteínas mostraram bem menos alteração.
Protegendo as células da ruptura
Além de inverter lipídios, o scrambling ativado mecanicamente alterou o comportamento físico das membranas sob estresse extremo. Em vesículas artificiais expostas a alta força, aquelas sem scramblases tendiam a estourar, enquanto vesículas contendo TMEM63A ou um scramblase conhecido encolhiam, formaram túbulos finos e permaneceram largamente intactas. Em uma linha celular de câncer cerebral humano que expressa naturalmente TMEM63A e TMEM63B, reduzir os níveis de qualquer uma das proteínas tornou as células mais propensas a se romper quando desafiadas com estresse mecânico intenso. Em conjunto, essas descobertas apoiam um modelo no qual as proteínas OSCA/TMEM63 atuam como válvulas que se abrem sob tensão e borram temporariamente a diferença usual entre as faces interna e externa da membrana. Ao permitir que os lipídios se redistribuam rapidamente, elas ajudam a equalizar o estresse e a prevenir rasgos catastróficos.
O que isso significa para saúde e doença
De maneira direta, este trabalho mostra que alguns canais sensíveis ao estiramento fazem mais do que conduzir sinais elétricos: eles também reorganizam a “pele” externa da célula para ajudá-la a sobreviver à compressão. As proteínas TMEM63 emergem como scramblases de lipídios ativadas mecanicamente cuja atividade é finamente regulada pela composição da membrana, especialmente pelo colesterol. Esse mecanismo de mecano-resiliência pode ser importante onde quer que as células estejam expostas a grandes forças, desde fibras nervosas isolantes e células sensoriais do ouvido até células cancerígenas que navegam por tecidos densos. Entender e, eventualmente, manipular essa função dupla de canal iônico e scramblase pode abrir novos caminhos para proteger tecidos vulneráveis — ou, inversamente, para tornar células cancerígenas difíceis de eliminar mais frágeis.
Citação: Lin, Y., Zhou, Z., Han, Y. et al. TMEM63 proteins act as mechanically activated cholesterol modulated lipid scramblases contributing to membrane mechano-resilience. Nat Commun 17, 2717 (2026). https://doi.org/10.1038/s41467-026-68919-x
Palavras-chave: canais iônicos mecanossensíveis, embaralhamento de lipídios, mecânica da membrana celular, regulação por colesterol, proteínas TMEM63 OSCA