Clear Sky Science · pt
Um peptídeo críptico neurotóxico originado do splicing críptico de PKN1 dependente de TDP-43
Ameaças ocultas dentro das células cerebrais
Muitas doenças do cérebro, incluindo esclerose lateral amiotrófica (ELA) e doença de Alzheimer, envolvem aglomerados de uma proteína chamada TDP-43. Os cientistas sabem que quando essa proteína deixa de funcionar corretamente, os neurônios perdem mensagens vitais e acabam morrendo. Este estudo revela uma reviravolta mais surpreendente: a falha de TDP-43 também pode fazer com que as células cerebrais fabriquem uma mini‑proteína tóxica até então desconhecida, que por sua vez prejudica circuitos de memória. Compreender esse ator oculto pode abrir novos caminhos para diagnóstico e tratamento em demências devastadoras.
Como um revisor celular mantém o RNA em ordem
Dentro dos neurônios, TDP-43 atua como um revisor do RNA, as mensagens intermediárias entre o DNA e as proteínas. Ele se liga a sequências curtas específicas e bloqueia a inserção de “pedaços extras” indesejados nessas mensagens. Quando TDP-43 é perdido ou mal localizado, como na ELA e em muitos casos de Alzheimer, esses pedaços extras — chamados éxons crípticos — podem invadir o RNA. Até agora, a maioria dos éxons crípticos conhecidos simplesmente causava perda da proteína normal ao tornar a mensagem instável e rapidamente degradada. Não estava claro se tais eventos também poderiam gerar novas proteínas nocivas.
Um splicing críptico cria um fragmento tóxico
Os autores concentraram-se em um gene chamado PKN1, que ajuda a manter a infraestrutura interna e o fluxo de sinal dos neurônios. Usando modelos celulares com redução de TDP-43, eles descobriram um éxon críptico previamente não reconhecido, apelidado de PKN1‑5a1, inserido entre dois segmentos normais do RNA de PKN1. Essa inserção introduz um sinal de parada precoce, produzindo um RNA encurtado. Notavelmente, parte dessa mensagem defeituosa escapa do sistema de controle de qualidade da célula e é traduzida em um fragmento estável da proteína PKN1 contendo apenas seus primeiros 207 aminoácidos. A equipe batizou esse produto truncado de PKN207. Eles mostraram que TDP-43 normalmente previne esse erro ligando-se a várias regiões ricas em UG que flanqueiam o éxon críptico; quando essa ligação é perdida, o éxon é empalado e PKN207 é produzido.
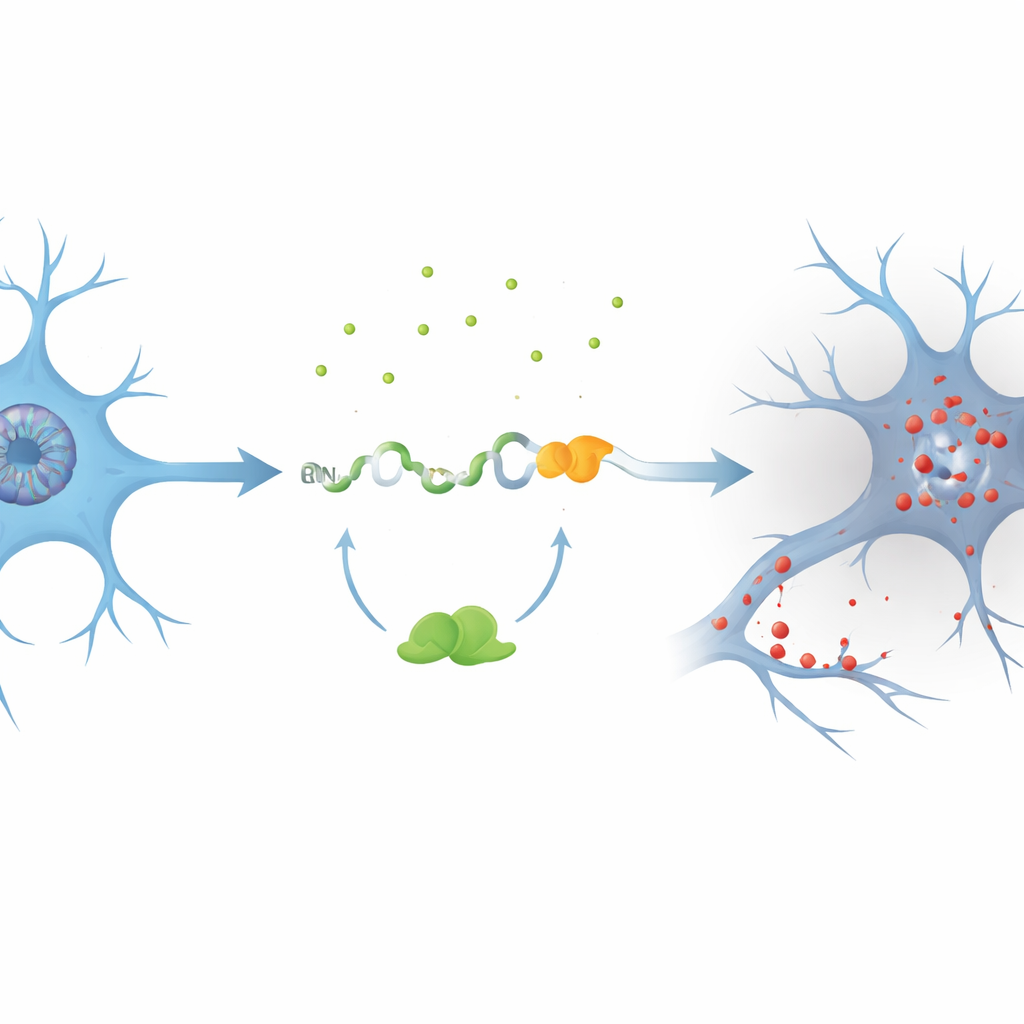
Evidências a partir de cérebros de pacientes e grandes conjuntos de dados
Para verificar se esse evento ocorre em doenças humanas, os pesquisadores vasculharam dados de sequenciamento de RNA de centenas de amostras cerebrais e de medula espinhal de pacientes com ELA. Eles encontraram ativação generalizada do éxon críptico PKN1‑5a1 em regiões conhecidas por serem afetadas pela patologia de TDP-43, como córtex motor e medula espinhal, mas não no cerebelo, relativamente poupado. Em seguida, geraram anticorpos altamente específicos que reconhecem apenas a cauda única do PKN207, e não a proteína PKN1 de comprimento total. Em tecido do hipocampo de pacientes com Alzheimer que também apresentavam TDP-43 anormal e fosforilado, esses anticorpos detectaram uma banda distinta correspondente ao PKN207, enquanto tal banda estava ausente em cérebros controle. Conjuntos adicionais de dados de Alzheimer confirmaram que o éxon críptico é ativado mesmo em estágios iniciais da doença, sugerindo que esse erro molecular pode começar muito antes dos sintomas serem óbvios.
Uma mini‑proteína com grande impacto na memória
A detecção de PKN207 em cérebros humanos doentes levantou a questão central: ele é prejudicial? Para testar isso, a equipe usou vírus para induzir a produção de PKN1 normal ou de PKN207 especificamente no hipocampo — uma área cerebral crítica para a memória — de camundongos jovens. Meses depois, ambos os grupos de camundongos mostraram aprendizado prejudicado no labirinto aquático de Morris, nadando por mais tempo para encontrar uma plataforma oculta. O líquido cefalorraquidiano continha níveis mais altos de uma proteína estrutural, a cadeia leve da neurofilamento, um marcador de dano axonal. Em neurônios em cultura, o aumento de PKN207 desencadeou lesão celular, medida pela liberação de uma enzima indicadora de dano à membrana. Perfis proteômicos detalhados do hipocampo revelaram alterações amplas em vias associadas à força sináptica (potenciação de longa duração) e a doenças neurodegenerativas bem conhecidas, com perturbação especialmente forte de moléculas que sustentam sinalização eficiente e um arcabouço saudável de fibras nervosas.
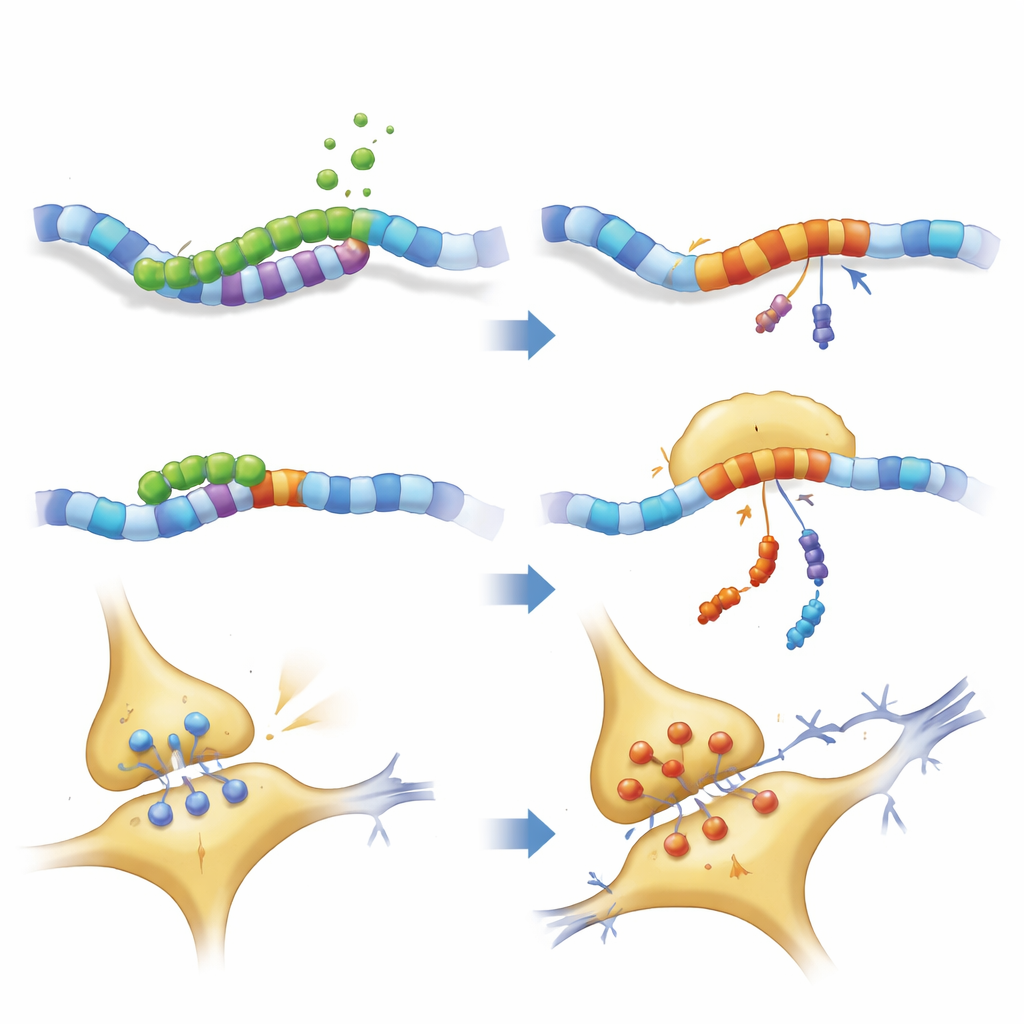
Como o fragmento desorganiza a fiação cerebral
Exames mais próximos da estrutura neuronal mostraram que tanto PKN1 de comprimento total quanto PKN207 perturbavam a rede de neurofilamentos que dá forma aos axônios e ajuda a transportar cargas. Proteínas motoras e de suporte-chave foram reduzidas, enquanto alguns componentes dos neurofilamentos se acumularam, sugerindo engarrafamentos de tráfego e possível aglomeração. Registros elétricos de fatias de hipocampo confirmaram que camundongos que expressavam PKN207 tinham potenciação de longa duração enfraquecida — o processo pelo qual sinapses se fortalecem após atividade repetida e uma base celular amplamente aceita para aprendizagem e memória. Embora PKN207 careça do domínio enzimático de PKN1, sua presença foi suficiente para imitar e às vezes superar os efeitos disruptivos da proteína completa, o que implica que a região N‑terminal compartilhada pode, por si só, interferir na homeostase neuronal.
Por que essa descoberta importa para doenças cerebrais
Este trabalho adiciona uma nova camada à nossa compreensão dos distúrbios relacionados ao TDP-43. Em vez de apenas causar perda de RNAs essenciais, a falha de TDP-43 também pode gerar uma micro‑proteína estável e tóxica que prejudica sinapses e cognição. O éxon críptico PKN1‑5a1 e seu produto peptídico PKN207 destacam-se agora como potenciais biomarcadores de disfunção precoce de TDP-43 e como alvos candidatos para terapias que corrijam o splicing ou bloqueiem o fragmento nocivo. De forma mais ampla, o estudo sugere que outros éxons ocultos podem igualmente dar origem a peptídeos promotores de doença, apontando os pesquisadores para um panorama rico — e antes negligenciado — de culpados moleculares na neurodegeneração.
Citação: Yang, M., Wang, Q., Yan, R. et al. A neurotoxic cryptic peptide arising from TDP-43-dependent cryptic splicing of PKN1. Nat Commun 17, 2963 (2026). https://doi.org/10.1038/s41467-026-68916-0
Palavras-chave: TDP-43, splicing críptico, PKN1, neurodegeneração, Alzheimer e ELA