Clear Sky Science · pt
Proteínas FOX em contrapeso controlam epigeneticamente o equilíbrio lítico‑latente do herpesvírus
Por que os herpesvírus ocultos importam
Muitas pessoas carregam vírus herpes simplex pelo resto da vida, frequentemente sem saber. Esses vírus podem ficar silenciosos dentro de neurônios por anos e então, subitamente, recrudescer, causando herpes labial, doenças oculares ou problemas mais graves em pessoas com imunidade comprometida. O que mantém o vírus adormecido na maior parte do tempo, e o que o reativa, tem sido um mistério de longa data. Este estudo desvenda uma parte chave desse sistema de controle: uma disputa entre dois grupos opostos de proteínas humanas que remodelam o DNA viral e determinam se o herpes permanece silencioso ou começa a produzir novos vírus.
Dois times celulares puxando em direções opostas
Os autores se concentraram em uma grande família de proteínas humanas que se ligam ao DNA, chamadas proteínas FOX, que normalmente ajudam a controlar nossos próprios genes durante o desenvolvimento e o metabolismo. Ao testar muitos membros da família FOX em células com características neuronais, eles encontraram dois campos distintos. Um grupo (incluindo proteínas como FOXF1) aumentou fortemente a replicação do vírus herpes simplex tipo 1 (HSV‑1) e de vários herpesvírus “alfa” relacionados. Outro grupo (FOXK1 e FOXK2) fez o oposto, reprimindo vigorosamente o crescimento viral. Esse equilíbrio não foi igual em todos os tipos celulares: células não neuronais e neurônios sob estresse tendiam a produzir mais das proteínas FOX ativadoras, enquanto neurônios sensoriais em repouso produziam muito pouco dessas ativadoras e altos níveis das proteínas repressoras FOXK.
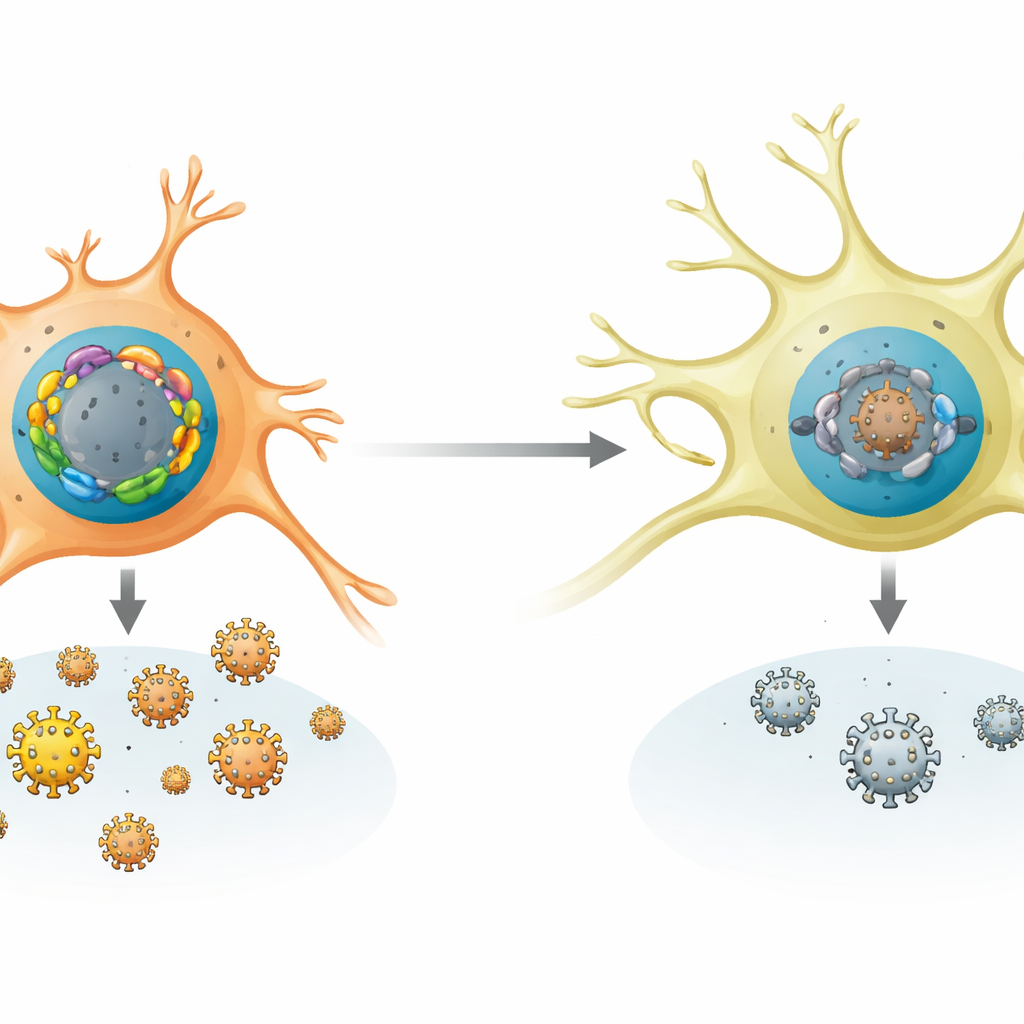
Como os neurônios favorecem o estado silencioso
A equipe comparou a atividade dos genes FOX em muitos tipos celulares humanos e de camundongo e em animais infectados. Neurônios sensoriais, o lar natural da latência do HSV‑1, mostraram um padrão que favorece o silêncio: expressão forte de FOXK1 e FOXK2, e expressão fraca da maioria dos genes FOX ativadores. Em camundongos, infecção inicial e sinais de estresse posteriores, como calor ou lesão tecidual, aumentaram seletivamente os níveis de vários genes Fox ativadores sem reduzir os repressivos. Em neurônios de camundongo em cultura e em camundongos vivos, deletar ou reduzir FOXK facilitou a replicação do HSV‑1 e sua reativação a partir da latência. Por outro lado, forçar neurônios a produzir proteínas FOX ativadoras extras foi suficiente para desencadear reativação mesmo sem gatilhos químicos, mostrando quão sensível o estado viral é a esse equilíbrio entre FOX.
Agarra o DNA viral e o abre ou fecha
Para entender o mecanismo subjacente, os pesquisadores mapearam onde as proteínas FOX se ligam no genoma viral. Eles descobriram que tanto o ativador FOXF1 quanto o repressor FOXK1 se ligam amplamente ao longo do DNA do HSV‑1, não apenas em alguns motivos de sequência específicos. Essa ligação depende de uma parte conservada das proteínas FOX que agarra o dorso da molécula de DNA em vez de letras individuais, permitindo que se fixem em quase qualquer lugar. Uma vez posicionados, os dois grupos de proteínas recrutam parceiros moleculares diferentes que remodelam a cromatina, a combinação do DNA com as proteínas de empacotamento. Proteínas FOX ativadoras, especialmente FOXF1, associam‑se à CBP e P300, enzimas que adicionam grupos acetil às histonas e afrouxam a cromatina. Isso torna o DNA viral mais acessível e aumenta a atividade dos genes virais iniciais, médios e tardios. FOXK1, em contraste, atua com fatores como SIN3A e MAX, ligados à desacetilação de histonas e repressão gênica, compactando a cromatina viral e mantendo os genes desligados.
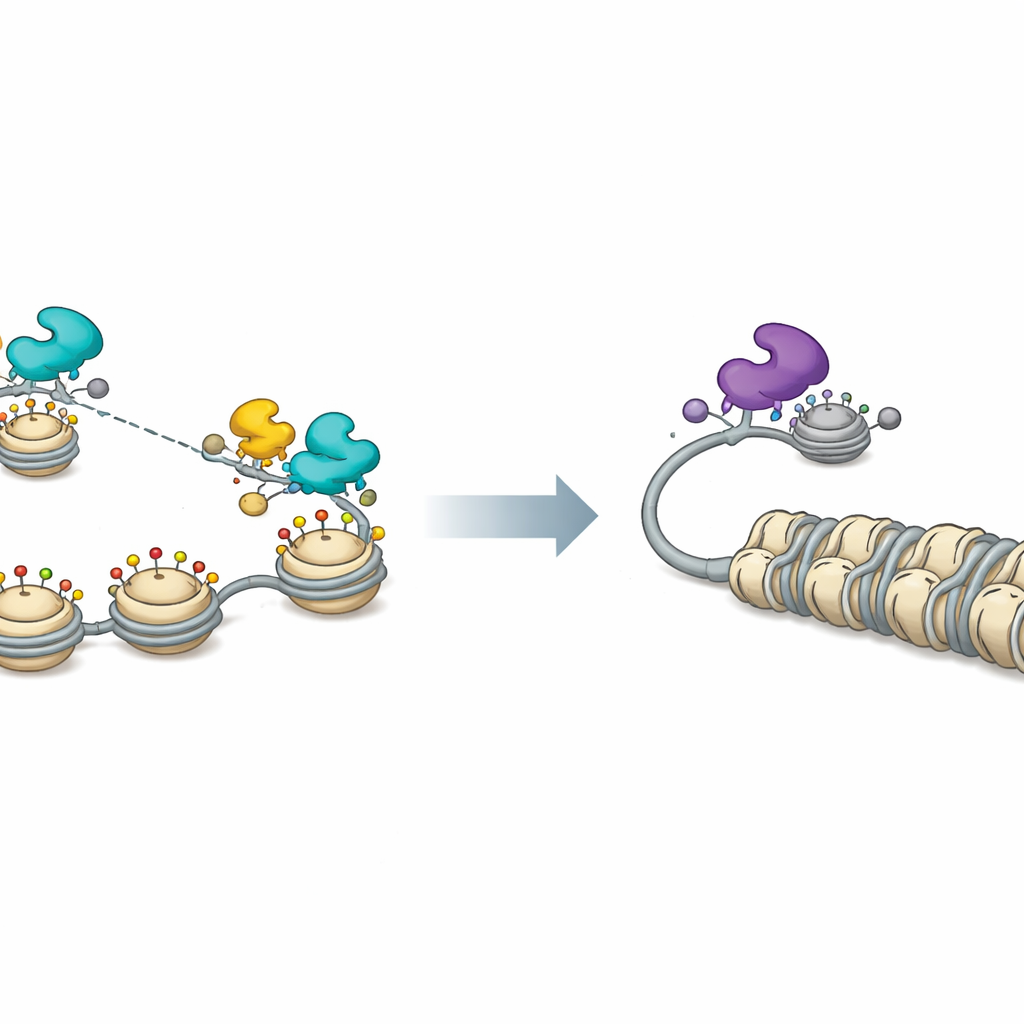
Um interruptor de cromatina para sono e vigília viral
Medições da cromatina viral confirmaram esse quadro. Quando FOXF1 estava presente, as histonas no DNA viral apresentavam marcas químicas associadas a cromatina aberta e ativa, e a acessibilidade geral dos promotores virais aumentou em todo o genoma. A expressão de FOXF1 também dispersou pequenas estruturas nucleares chamadas corpos nucleares de PML, que normalmente ajudam a manter o DNA viral reprimido. Bloquear CBP e P300 apagou muitos desses efeitos ativadores e reduziu a expressão gênica viral dirigida por FOXF1. No lado repressivo, os pesquisadores mostraram que os parceiros associados a FOXK1 e a atividade de desacetilases de histonas eram importantes para manter a replicação do HSV‑1 baixa; a inibição química das desacetilases tanto aumentou a produção viral quanto enfraqueceu a supressão mediada por FOXK1.
O que isso significa para controlar infecções ao longo da vida
Em conjunto, o trabalho sugere que o estado ativo ou dormente do HSV‑1 depende fortemente da mistura de proteínas FOX no neurônio hospedeiro. Neurônios sensoriais em repouso favorecem naturalmente o estado repressivo dominado por FOXK, empurrando o vírus para uma forma profundamente silenciosa e compactada em cromatina. Estresses ou outras condições que elevam proteínas FOX ativadoras podem desequilibrar essa balança, abrindo a cromatina viral e permitindo que o ciclo lítico reinicie. Ao revelar essa disputa epigenética, o estudo destaca novas maneiras pelas quais cientistas, no futuro, possam empurrar os herpesvírus de forma mais firme para uma latência inofensiva ou, alternativamente, forçá‑los a sair do esconderijo em condições controladas para que possam ser eliminados.
Citação: Xiang, Y., Yang, X., Zhang, J. et al. Counteracting FOX proteins epigenetically control the herpesvirus lytic-latent balance. Nat Commun 17, 2256 (2026). https://doi.org/10.1038/s41467-026-68915-1
Palavras-chave: latência do vírus herpes simplex, fatores de transcrição FOX, cromatina viral, regulação epigenética, reativação viral