Clear Sky Science · pt
Reaproveitamento evolutivo de um complexo tiolase metabólico possibilita biossíntese de antibióticos
Como micróbios comuns reinventam sua química
Muitos dos antibióticos e medicamentos dos quais dependemos são silenciosamente produzidos por bactérias. Esses pequenos químicos usam enzimas — máquinas moleculares — para construir compostos defensivos complexos. Este estudo revela como uma enzima central do metabolismo, antes dedicada às tarefas básicas da célula, foi reconfigurada evolutivamente em bactérias orais para fabricar um antibiótico potente. Compreender essa transformação não apenas explica como a natureza inventa nova química, mas também oferece pistas para o desenho de fármacos e biocatálise de próxima geração.
Do metabolismo básico à arma química
Todas as células vivas dependem de um conjunto de enzimas conservadas que sustentam seu metabolismo central, como degradar gorduras e construir moléculas essenciais. Um desses grupos, chamado superfamília das tiolases, normalmente ajuda a processar pequenas moléculas ricas em energia como acetil‑CoA e sustenta vias vitais para a síntese de lipídios e outros componentes celulares. Os autores descobriram que, em diversas espécies orais de Streptococcus, um complexo trifásico baseado em tiolase — composto por proteínas relacionadas a HMGS, ACAT e uma terceira proteína auxiliar — abandonou seu papel metabólico ancestral. Em vez disso, esse complexo passa a completar a biossíntese de um antibiótico chamado reutericyclin A, que ajuda essas bactérias a competir no ambiente lotado da cavidade bucal.
Um novo tipo de reação enzimática em uma estrutura de antibiótico
Ao reconstruir o complexo de Streptococcus em laboratório e alimentá‑lo com um precursor quimicamente sintetizado do reutericyclin A, os pesquisadores mostraram que o complexo realiza uma reação incomum de formação de ligação carbono–carbono conhecida como acilação C de Friedel–Crafts. Em vez de ligar um grupo acetil ao oxigênio, como muitas enzimas fazem, ele instala esse grupo diretamente em um átomo de carbono de um anel pirrolidina‑2,4‑diona — uma parte importante do arcabouço do reutericyclin. O complexo aceita tanto doadores acetil naturais, como acetil‑CoA, quanto vários doadores artificiais, e pode até executar a reação no sentido inverso, rompendo a ligação que criou. Essa flexibilidade amplia o repertório conhecido de aciltransferases biológicas e sugere como tais enzimas podem ser adaptadas para construir produtos químicos variados.
Reaproveitando um arcabouço proteico conservado
Usando microscopia crioeletrônica de alta resolução, a equipe elucidou a estrutura tridimensional do complexo de Streptococcus, denominado SmaATase. Apesar de sua nova função, o SmaATase mantém uma semelhança arquitetural marcante com um complexo relacionado em arqueias que participa da via do mevalonato para a construção de lipídios isoprenóides. Ambos são grandes conjuntos multiméricos formados por módulos repetidos e apresentam uma cavidade compartilhada onde o cofator CoA pode se ligar e mover‑se entre sítios ativos. Contudo, resíduos catalíticos chave essenciais para a reação metabólica original estão ausentes ou alterados na versão bacteriana. Testes bioquímicos confirmam que o SmaATase já não consegue sintetizar o produto ancestral HMG‑CoA e, em vez disso, usa acetil‑CoA puramente como doador para seus novos substratos de pequena molécula.
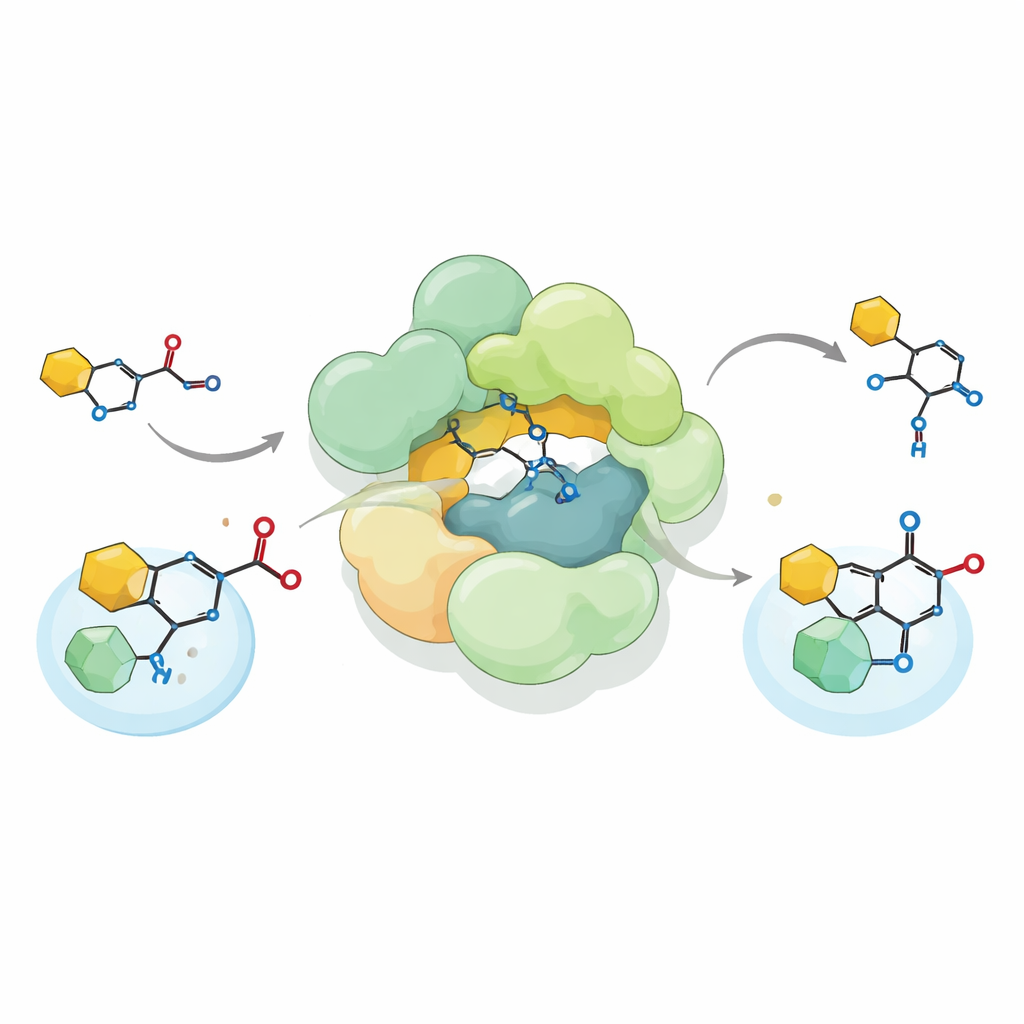
Uma trilha evolutiva do metabolismo até os antibióticos
Para entender como esse reaproveitamento pode ter ocorrido, os autores compararam sequências e atividades de complexos relacionados em muitas bactérias e arqueias. Eles identificaram mais de mil aglomerados gênicos contendo o mesmo trio de tipos enzimáticos. Alguns ainda sustentam a química clássica das tiolases; outros, como os encontrados em Pseudomonas, alimentam diferentes antibióticos de pequena molécula. Um complexo representativo de Pseudomonas fluorescens parece situar‑se em um ponto intermediário desse caminho evolutivo: seu domínio do tipo HMGS está desativado, mas sua unidade do tipo ACAT ainda realiza uma reação mais convencional em substratos ligados ao CoA. No SmaATase e em seu equivalente de Pseudomonas que produz o composto protetor de culturas DAPG, mudanças adicionais ao redor do sítio ativo moldaram as enzimas para reconhecer aceptores não padronizados, como anéis aromáticos ou núcleos de ácido tetramíco.
Por que um pequeno grupo acetil faz grande diferença
No fim, o ganho biológico dessa transformação molecular é evidente. Quando a equipe testou os antibióticos acetilados reutericyclin A e DAPG contra uma banca de bactérias Gram‑positivas, essas moléculas mostraram forte atividade letal, enquanto seus precursores não acetilados foram muito mais fracos ou quase inativos. Aquele pequeno grupo acetil, posicionado no lugar certo pelo complexo enzimático reaproveitado, transforma um arcabouço modesto em uma arma poderosa, permitindo que Streptococcus na boca ou Pseudomonas ao redor das raízes das plantas superem seus vizinhos. Este trabalho demonstra como a evolução pode reciclar estruturas enzimáticas existentes com mutações mínimas mas estratégicas, convertendo maquinário metabólico rotineiro em ferramentas especializadas de defesa química — e oferecendo um roteiro para engenheiros que desejam projetar novos catalisadores de formação de ligação carbono–carbono para descoberta de fármacos e biologia sintética.
Citação: Liao, G., Sun, R., Shen, Z. et al. Evolutionary repurposing of a metabolic thiolase complex enables antibiotic biosynthesis. Nat Commun 17, 2196 (2026). https://doi.org/10.1038/s41467-026-68910-6
Palavras-chave: evolução de enzimas, biossíntese de produtos naturais, química de antibióticos, reaproveitamento metabólico, acilação de Friedel–Crafts