Clear Sky Science · pt
Modelagem da fibrose pulmonar com iPSC humanas revela que inibição de p300/CBP suprime o estado transitório de células alveolares
Por que pulmões cicatrizados importam para todos nós
A fibrose pulmonar idiopática (FPI) é uma doença implacável em que os pulmões se transformam lentamente em tecido cicatricial, tornando cada respiração mais difícil. Os medicamentos atuais apenas desaceleram esse processo e frequentemente causam efeitos colaterais preocupantes. Este estudo utiliza ferramentas avançadas de células‑tronco e genômica para recriar pulmões cicatrizados no laboratório, fazendo uma pergunta simples, porém vital: podemos encontrar um interruptor que desvie células pulmonares danificadas de um estado prejudicial de volta para a reparação?
Uma janela cultivada em laboratório para um pulmão cicatrizado
Para investigar a FPI, os pesquisadores construíram pulmões miniaturizados a partir de células‑tronco pluripotentes induzidas humanas (iPSCs). Essas iPSCs foram guiadas para se tornarem células alveolares — as células que revestem os pequenos sacos de ar onde o oxigênio entra no sangue — e foram cultivadas junto com fibroblastos pulmonares, as células do tecido conjuntivo que formam cicatriz. Embutidos em um gel macio, esses “organoides alveolares” comportaram‑se de maneira muito semelhante ao tecido pulmonar real. Quando expostos à bleomicina, um medicamento quimioterápico conhecido por causar lesão pulmonar, os gels encolheram à medida que os fibroblastos os puxavam, imitando a contração tecidual observada na fibrose.
Usando este sistema, a equipe rastreou uma biblioteca de 264 pequenas moléculas e mediu automaticamente quanto cada droga impedia a contração do gel, com uma ferramenta de análise de imagem por deep learning garantindo leituras objetivas. Muitas substâncias não tiveram efeito, mas uma família destacou‑se claramente: inibidores das proteínas p300 e CBP, que ajudam a controlar como o DNA é embalado e quais genes são ativados. Todas as oito compostos direcionados a p300/CBP na biblioteca reduziram a contração em baixas doses, destacando essa via como um ponto promissor de intervenção na fibrose. 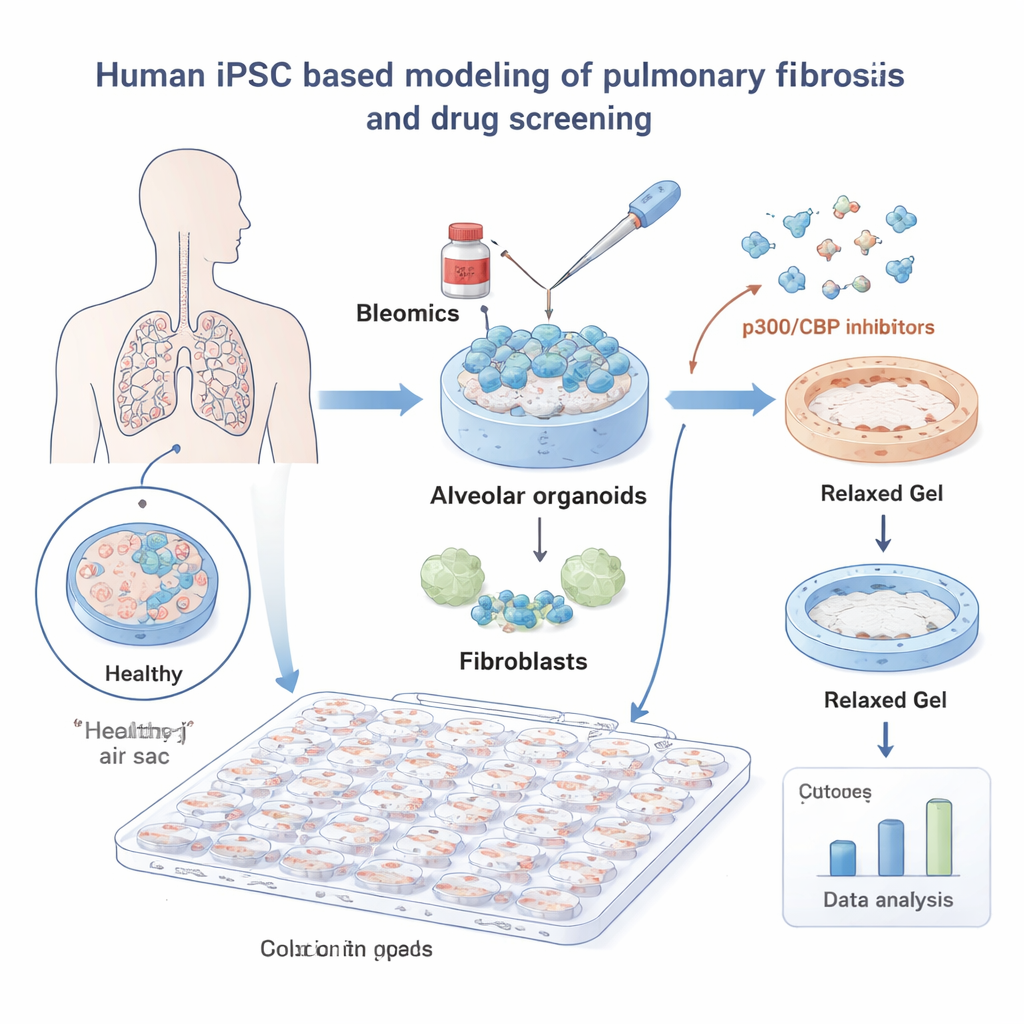
Os culpados: células pulmonares transitórias
Trabalhos recentes revelaram um tipo celular “intermediário” problemático em pulmões doentes, chamado estado transitório alveolar. Normalmente, células de suporte conhecidas como AT2 amadurecem em células AT1 ultrafinas que cobrem os alvéolos e permitem a troca gasosa. Na FPI, contudo, as AT2 frequentemente ficam presas nesse estado transitório, expressando genes de estresse e reparo enquanto falham em completar a transição para AT1 plenamente funcionais. Essas células transitórias se agrupam em regiões fibróticas e se comunicam intensamente com fibroblastos, mas não estava claro se elas eram mero subproduto do dano ou motor ativo da cicatrização.
Ao sequenciar RNA e mapear cromatina acessível em seus organoides, os autores mostraram que as células transitórias que surgiram em seu modelo corresponderam de perto àquelas encontradas em pulmões de pacientes com FPI. Essas células transitórias induzidas exibiram assinaturas genéticas de estresse, inflamação e remodelamento da matriz, e ativaram fortemente fibroblastos pulmonares adultos co‑cultivados. Crucialmente, quando p300/CBP foi bloqueado, marcadores do estado transitório diminuíram, a identidade AT2 foi melhor preservada e a ativação dos fibroblastos enfraqueceu. Em outras palavras, os fármacos não envenenaram as células de forma indiscriminada; em vez disso, impediram seletivamente que as AT2 ficassem presas nesse limbo prejudicial.
Desvendando os interruptores moleculares
Para entender como p300/CBP molda essa decisão de destino, a equipe examinou marcas químicas em histonas — proteínas que ajudam a embalar o DNA. Uma marca particular, a acetilação de H3K27, é comumente adicionada por p300/CBP em enhancers e promotores ativos. Nas células transitórias, regiões próximas a genes de resposta ao estresse e pró‑fibrose apresentavam forte acetilação de H3K27 e estavam enriquecidas em locais de ligação de fatores de transcrição como AP‑1 e HNF1B. Quando as células foram tratadas com inibidores de p300/CBP, essas marcas de acetilação diminuíram nesses locais, e a expressão de muitos genes pró‑fibrose caiu. Bloquear diretamente o AP‑1, ou reduzir AP‑1 e HNF1B com pequenos RNAs interferentes, igualmente conteve o programa transitório e a contração dos organoides, ligando esse trio — p300/CBP, AP‑1 e HNF1B — ao motor que alimenta o remodelamento fibrótico.
Além do cultivo, o estudo testou um inibidor, CBP30, em camundongos com lesão pulmonar induzida por bleomicina. Animais tratados com CBP30 tiveram menos células epiteliais transitórias, menor ativação de miofibroblastos formadores de cicatriz e expressão reduzida de marcadores de fibrose. Essa validação cruzada entre modelos humanos de células‑tronco e um modelo animal reforça a ideia de que p300/CBP não é apenas um artefato de laboratório, mas um regulador genuíno da cicatrização pulmonar. 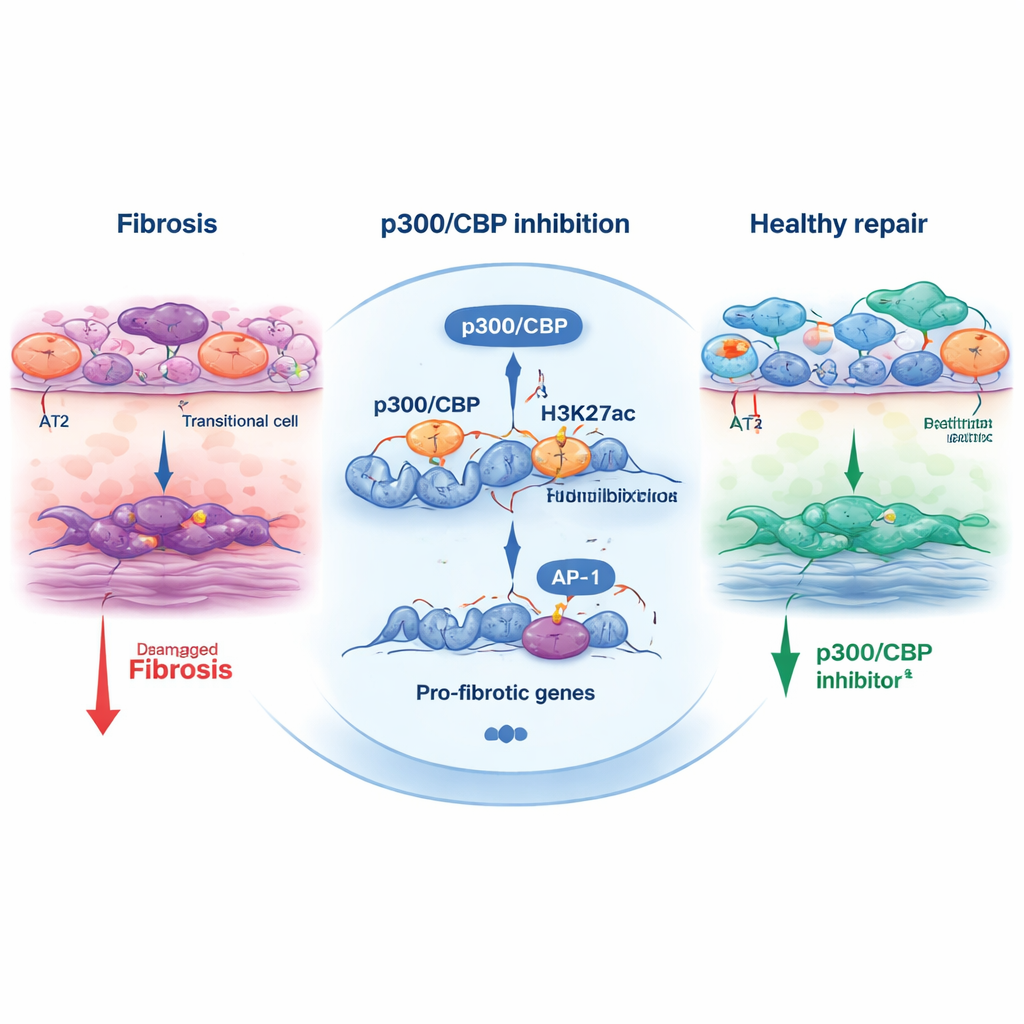
O que isso significa para tratamentos futuros
Para não especialistas, a principal conclusão é que os autores construíram um modelo humano realista de pulmões fibróticos e o usaram para destacar um novo alvo terapêutico. O trabalho sugere que a cicatrização pulmonar é impulsionada em parte por um estado celular transitório, induzido por estresse, que desorienta o tecido ao redor. Ao reduzir a atividade de p300/CBP, pode ser possível silenciar esse estado, manter as células alveolares em uma trajetória de desenvolvimento saudável e reduzir os sinais que empurram os fibroblastos ao excesso de atividade. Embora os inibidores de p300/CBP ainda precisem ser otimizados quanto à segurança e testados clinicamente, este estudo aponta para terapias que abordam a comunicação celular errônea na raiz da FPI, em vez de apenas retardar suas consequências.
Citação: Tsutsui, Y., Masui, A., Konishi, S. et al. Human iPSC-based Modeling of Pulmonary Fibrosis Reveals p300/CBP Inhibition Suppresses Alveolar Transitional Cell State. Nat Commun 17, 1214 (2026). https://doi.org/10.1038/s41467-026-68909-z
Palavras-chave: fibrose pulmonar idiopática, organoides alveolares, inibidores de p300/CBP, células epiteliais transitórias, células‑tronco do pulmão