Clear Sky Science · pt
Projetando plasmídeos com origens sintéticas de replicação
Por que reescrever o DNA microbiano importa
Muitas das ferramentas por trás da biotecnologia moderna, desde a produção de insulina até circuitos genéticos de ponta, dependem de pequenos círculos de DNA chamados plasmídeos. Esses trabalhadore s genéticos transportam genes projetados para bactérias, mas seu desenho básico mudou muito pouco ao longo das décadas. Este estudo mostra que o próprio núcleo dos plasmídeos — as sequências que dizem às células quando e com que frequência copiá-los — pode ser completamente reimaginado. Ao reconstruir esse “motor de cópia” do zero, os autores criam plasmídeos mais fáceis de ajustar, combinar e programar, abrindo caminho para diagnósticos, biomanufatura e biologia sintética mais flexíveis.
Ferramentas antigas com limites ocultos
Plasmídeos evoluíram naturalmente como DNA móvel, ajudando bactérias a compartilhar características como resistência a antibióticos ou novas formas de digerir fontes de alimento. No laboratório, engenheiros reaproveitam esses plasmídeos para carregar genes úteis, mas a maioria depende de alguns desenhos clássicos descobertos nos anos 1980. Esses desenhos antigos escondem um emaranhado de partes genéticas sobrepostas que controlam quantas cópias de um plasmídeo existem dentro de cada célula e se plasmídeos diferentes podem coexistir pacificamente. Como essas partes estão fundidas, alterar uma característica pode, de forma imprevisível, quebrar outra. Como resultado, os cientistas ficam com um menu curto de plasmídeos com números de cópia fixos e compatibilidade limitada, restringindo o quão complexos os sistemas projetados podem se tornar.
Reconstruindo o motor de cópia do zero
Os pesquisadores focaram em uma origem de replicação amplamente usada da família de plasmídeos pMB1. Em sua forma natural, essa origem usa uma conversa finamente equilibrada entre dois RNAs — um que inicia a cópia do DNA e outro que a interrompe — para manter o número de plasmídeos sob controle. A equipe primeiro “refatorou” esse sistema: separaram genes sobrepostos, desativaram um promotor embutido e colocaram peças-chave em cassetes genéticos limpos e separados. Isso por si só mostrou que a função central da origem podia ser preservada enquanto se simplificava seu layout, transformando uma peça bagunçada moldada pela evolução em algo mais parecido com uma máquina modular com componentes acessíveis.
Inserindo botões de controle sintéticos
Com a lógica de controle original exposta, os autores então a substituíram por reguladores totalmente sintéticos. Eles conectaram o primer de replicação a chaves de RNA projetadas que atuam como botões dimmer: pequenos RNAs controladores podem girar essas chaves para permitir ou bloquear a produção do primer e, por sua vez, a cópia do plasmídeo. Ao escolher variantes de chave diferentes e combiná-las com promotores de força variada, eles ajustaram o número de cópias do plasmídeo em mais de duas ordens de magnitude. Também exploraram diferentes disposições físicas dos cassetes de controle no DNA, descobrindo arranjos que melhoraram a estabilidade e permitiram encolher a região de replicação até um núcleo compacto e funcional, ao mesmo tempo em que adicionavam sistemas auxiliares naturais que evitam enredamentos problemáticos entre plasmídeos.
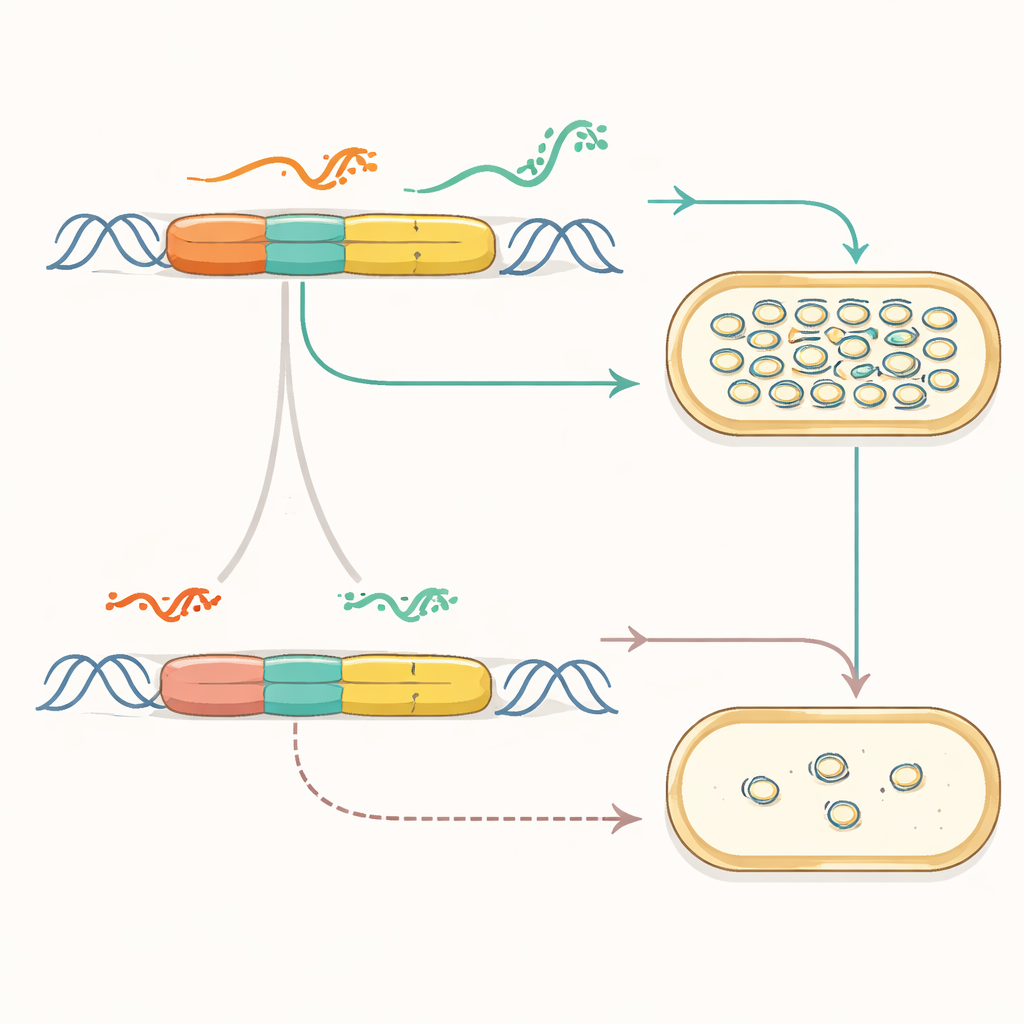
Transformando sinais químicos em contagem de DNA
Uma vez modularizado o motor de cópia, a equipe demonstrou que ele podia ser conectado para detectar o mundo externo. Eles ligaram a origem sintética a promotores indutíveis e a estruturas de RNA chamadas ribosswitches, que mudam de forma em resposta a pequenas moléculas. Nesses novos plasmídeos, adicionar um químico como IPTG ou cumato fez com que o número de cópias do plasmídeo — e, portanto, um sinal repórter — aumentasse ou diminuísse. Múltiplos sinais puderam ser combinados de modo que uma molécula estimulasse a cópia enquanto outra a restringia. Os pesquisadores até construíram pares de plasmídeos, cada um respondendo a um químico diferente, e acompanharam suas mudanças de número de cópias na mesma célula por sequenciamento de DNA, efetivamente transformando contagens de plasmídeos em um código de barras da história ambiental.
Muitos plasmídeos personalizados em uma única célula
Um teste chave dessa abordagem foi verificar se vários plasmídeos controlados de forma independente podiam coexistir. Apoiado por uma biblioteca de reguladores de RNA ortogonais, o grupo construiu seis plasmídeos diferentes, cada um com sua própria origem sintética e marcador de antibiótico, e introduziu todos os seis simultaneamente em E. coli. O sequenciamento de plasmídeos completos ao longo de vários dias confirmou que todos os seis permaneceram presentes, embora suas abundâncias relativas tenham variado. Tentativas de fazer o mesmo com seis plasmídeos convencionais falharam, ressaltando como o desenho refatorado e os sistemas de estabilidade adicionados tornam os novos plasmídeos mais compatíveis e robustos quando estão em alta densidade dentro de uma única célula.
O que isso significa para a biotecnologia futura
Para um não especialista, a conclusão é direta: os autores transformaram plasmídeos de ferramentas rígidas e “tamanho único” em uma plataforma personalizável. Suas origens sintéticas de replicação funcionam como motores plug-and-play cuja velocidade, sensibilidade e entradas podem ser escolhidas sob demanda. Isso torna possível construir bactérias que registram exposições químicas como mudanças no número de cópias de DNA, testar muitos caminhos genéticos em paralelo ao distribuí‑los por múltiplos plasmídeos ou equilibrar finamente crescimento e produção em linhagens industriais. Embora alguns compromissos de estabilidade ainda persistam, este trabalho mostra que a mecânica central da replicação de plasmídeos não está mais fora do alcance da engenharia, abrindo novo espaço para inovação na biologia sintética.
Citação: Liu, B., Seet, Z.R.D., Peng, X. et al. Engineering plasmids with synthetic origins of replication. Nat Commun 17, 2255 (2026). https://doi.org/10.1038/s41467-026-68907-1
Palavras-chave: plasmídeos sintéticos, origem de replicação, reguladores de RNA, controle do número de cópias, biologia sintética