Clear Sky Science · pt
O receptor de succinato 1 restringe a hematopoiese e previne a progressão da leucemia mieloide aguda
Quando o Combustível Celular Sai do Controle
Nosso sangue é constantemente renovado por uma pequena população de células-tronco escondida na medula óssea. Este estudo investiga como um subproduto metabólico comum, o succinato, e seu sensor na superfície celular atuam como um freio nesse sistema de renovação. Quando esse freio falha, o equilíbrio entre a produção sanguínea saudável e o crescimento canceroso pode pender para a leucemia mieloide aguda (LMA), um câncer sanguíneo agressivo. Entender esse interruptor de controle oculto pode levar a tratamentos mais precisos que contenham a doença restaurando as salvaguardas naturais do organismo.
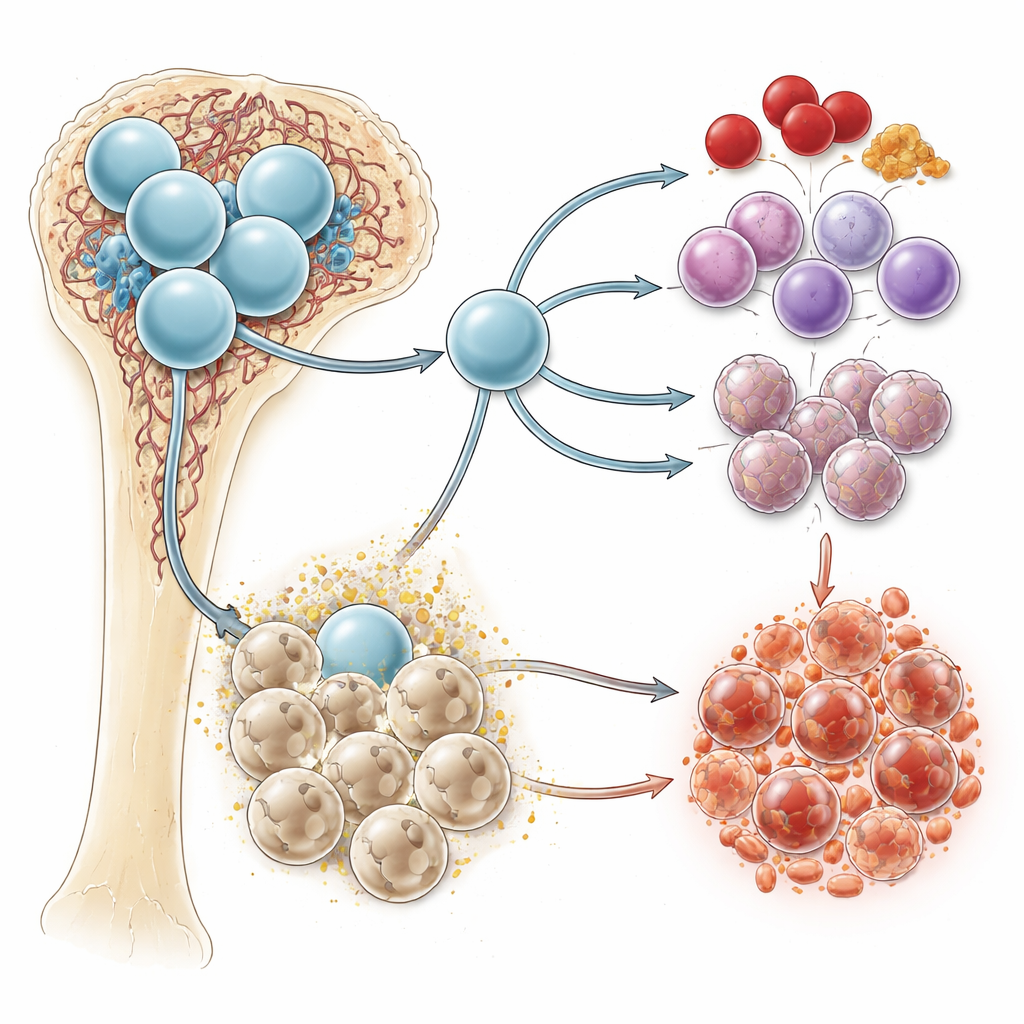
Um Sinal Químico com Dupla Função
O succinato é um subproduto rotineiro de como as células queimam combustível, especialmente dentro das mitocôndrias, as usinas de energia da célula. Em condições de baixo oxigênio — como as encontradas na medula óssea — o succinato tende a se acumular. Ele pode agir dentro das células, alterando o metabolismo e as respostas inflamatórias, e também pode escapar para o exterior para atuar como um sinal. Na superfície celular, um receptor chamado SUCNR1 detecta o succinato e transmite sua presença para o interior. Trabalhos anteriores vincularam succinato e SUCNR1 à inflamação e a ambientes favoráveis ao câncer, mas seu papel direto na formação do sangue e na leucemia era pouco claro.
Um Sinal de Alerta em Pacientes com Leucemia
Os pesquisadores analisaram dados de expressão gênica de centenas de pacientes com LMA e descobriram que os níveis de SUCNR1 variam amplamente entre os indivíduos. Pacientes cujas células leucêmicas produziam pouco SUCNR1 apresentaram sobrevida global e sobrevida livre de progressão mais curtas, mesmo após ajuste por idade, sexo e subtipos clínicos padrão. Certos subgrupos genéticos de LMA tendiam a apresentar SUCNR1 particularmente baixo. Quando a equipe transplantou células humanas de LMA deficientes em SUCNR1 em camundongos imunodeficientes e depois injetou os animais com ácido succínico (que se torna succinato no organismo), a carga leucêmica na medula óssea aumentou. Isso sugeriu que, em cânceres com baixo SUCNR1, succinato extra pode, na verdade, impulsionar a progressão da doença em vez de contê-la.
O Freio Oculto nas Células-Tronco do Sangue
Para entender como o SUCNR1 age na formação normal do sangue, os cientistas recorreram a camundongos geneticamente modificados. Quando SUCNR1 foi deletado, seja no animal inteiro ou apenas nas células formadoras de sangue, a medula óssea tornou-se hiperativa. Células-tronco e progenitoras expandiram-se, e tanto células mieloides (como monócitos e granulócitos) quanto células B aumentaram no sangue e no baço. Essas células com características de tronco sobreviveram melhor e formaram mais colônias em placas de cultura, embora fossem um pouco menos capazes de restabelecer a produção sanguínea quando transplantadas em competição com células normais. Uma linhagem de camundongo repórter mostrou que apenas um subconjunto de células-tronco e progenitoras realmente expressa SUCNR1; essas células SUCNR1-positivas tinham potencial de enxerto particularmente limitado. No geral, o receptor atuou como uma restrição ao tamanho e à atividade do pool de células-tronco.
Da Defesa Equilibrada à Sobrecarga Inflamatória
O perfil detalhado de expressão gênica de células-tronco e progenitoras sem SUCNR1 revelou uma mudança marcante. Assinaturas de células-tronco primitivas e silenciosas foram suprimidas, enquanto genes ligados à inflamação, espécies reativas de oxigênio e células sanguíneas maduras foram aumentados. Duas moléculas se destacaram: S100A8 e S100A9, um par de “alarminas” que amplificam a sinalização inflamatória. Esses fatores estavam aumentados tanto dentro do compartimento de células-tronco quanto no fluido circundante da medula óssea. Quando a equipe tratou camundongos deficientes em SUCNR1 com tasquinimode, um fármaco que bloqueia a sinalização de S100A9, a expansão excessiva de células-tronco e progenitoras, bem como a superprodução de células mieloides e B, foi em grande parte revertida. Em outras palavras, grande parte do dano causado pela perda de SUCNR1 pôde ser desfeito cortando o circuito de alarme S100A8/S100A9.
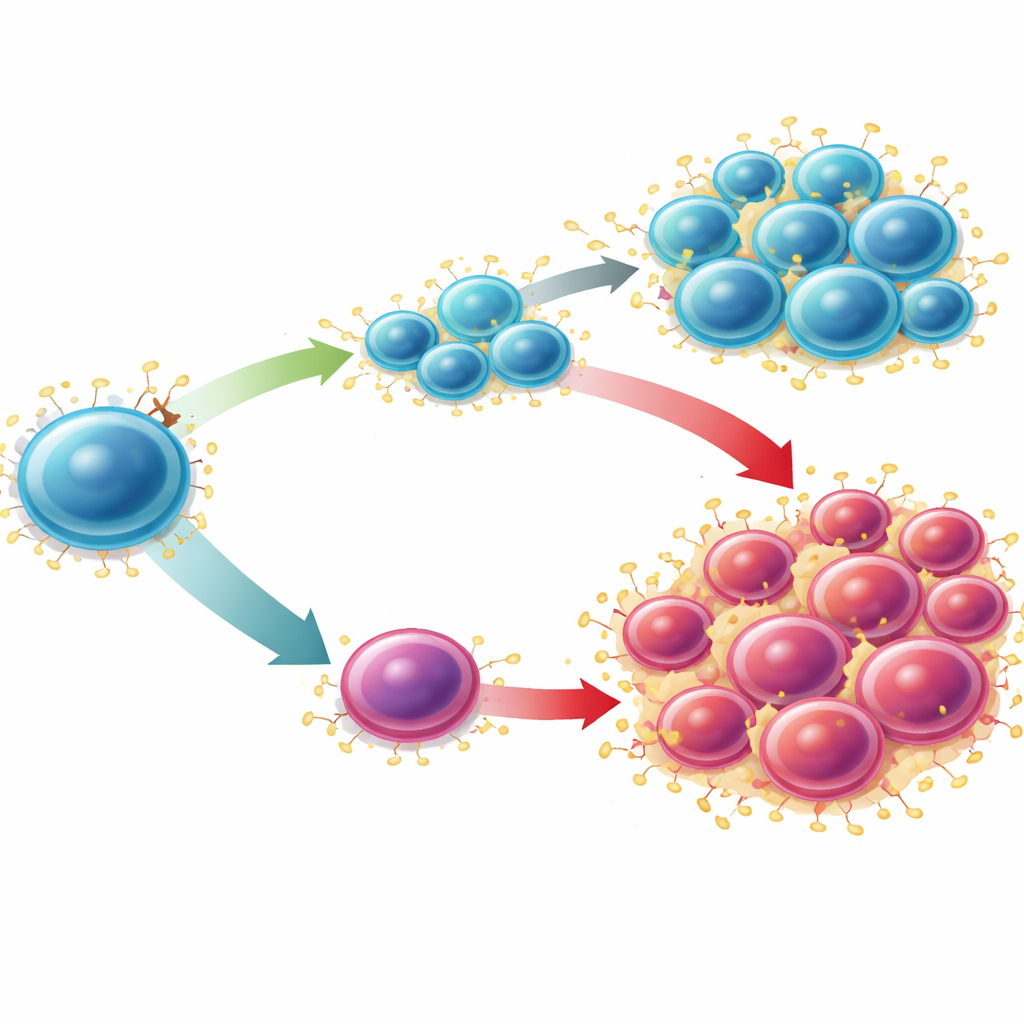
Transformando uma Vulnerabilidade em Estratégia Terapêutica
Os cientistas então questionaram se essa via poderia ser explorada terapeuticamente na LMA. Em uma leucemia murina agressiva dirigida pela mutação MLL-AF9 — onde os níveis de Sucnr1 são muito baixos — bloquear S100A9 com tasquinimode, especialmente quando combinado com um composto potente que ativa SUCNR1, reduziu células com características de células-tronco leucêmicas e diminuiu a carga da doença na medula óssea e no baço. Análises de dados de RNA de célula única de modelos humanos de LMA tratados com o quimioterápico citarabina mostraram que os agrupamentos celulares resistentes eram ricos em S100A8 e S100A9, enquanto SUCNR1 era escasso e associado a um subconjunto metabolicamente ativo que encolheu após o tratamento. Em linhagens celulares humanas de leucemia, ativar SUCNR1 aumentou a morte celular induzida pela quimioterapia e pôde desencadear apoptose por si só quando SUCNR1 era superexpresso. Em conjunto, essas descobertas posicionam o baixo SUCNR1 não apenas como um marcador de mau prognóstico, mas também como uma fraqueza: células leucêmicas que perderam esse freio podem depender fortemente do eixo S100A8/S100A9 e ser particularmente sensíveis a estratégias que reativem a sinalização de SUCNR1 ou bloqueiem o alarme downstream.
Uma Nova Alavanca para Controlar a Leucemia
Para o leitor leigo, a mensagem central é que um subproduto metabólico aparentemente mundano, o succinato, e seu receptor SUCNR1 formam um sistema de segurança inesperado na formação do sangue. Quando SUCNR1 está presente e ativo, mantém as células-tronco sob controle e previne crescimento desordenado. Quando SUCNR1 é perdido ou baixo — comum em alguns pacientes com LMA — succinato e alarminas inflamatórias como S100A8 e S100A9 podem empurrar células-tronco e progenitoras para a superexpansão e para a leucemia. Combinando fármacos que atenuam esse alarme inflamatório com agentes que restauram ou mimetizam a sinalização de SUCNR1, pode ser possível reorientar o sistema para uma produção sanguínea equilibrada e melhorar a eficácia da quimioterapia existente.
Citação: Cuminetti, V., Boet, E., Heugel, M. et al. Succinate receptor 1 restricts hematopoiesis and prevents acute myeloid leukemia progression. Nat Commun 17, 2403 (2026). https://doi.org/10.1038/s41467-026-68906-2
Palavras-chave: leucemia mieloide aguda, receptor de succinato, células-tronco hematopoéticas, metabolismo e câncer, sinalização inflamatória