Clear Sky Science · pt
Oxidases de álcool projetadas catalisam transesterificação em meio aquoso sem hidrólise concorrente
Por que essa história enzimática importa
Muitos produtos do dia a dia, de medicamentos e aromatizantes alimentares ao biodiesel, dependem de um tipo simples de ligação química chamada éster. Produzir e ajustar esses ésteres de forma eficiente, econômica e ambientalmente correta é um objetivo central da química verde. O problema é que a água — o solvente ideal do ponto de vista de segurança e sustentabilidade — geralmente sabota essas reações, degradando ésteres tão rápido quanto eles são formados. Este estudo descreve uma enzima projetada que consegue formar ésteres em água enquanto praticamente ignora a presença do solvente, abrindo caminho para uma química industrial mais limpa.
Reorientando uma enzima conhecida para um novo papel
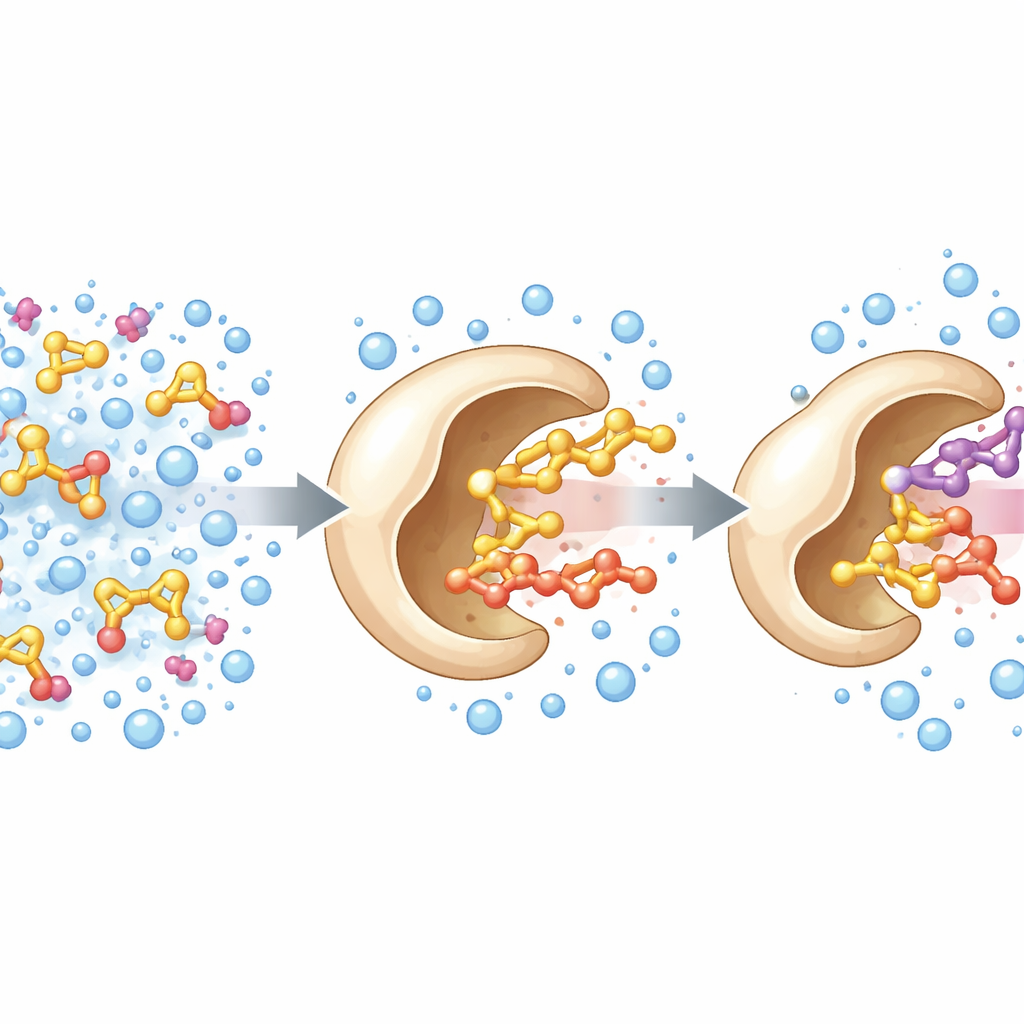
Os pesquisadores partiram de uma enzima conhecida, uma alcool oxidase de um fungo que degrada madeira. Na natureza, essa enzima usa um cofator flavínico para extrair elétrons de álcoois pequenos, como metanol. A equipe procurou ampliar seu escopo para que ela pudesse processar álcoois mais volumosos, mais relevantes para químicos finos e aromas. Com o mapa da estrutura tridimensional da enzima em mãos, focaram em três aminoácidos que atuam como uma espécie de portal para o sítio ativo. Ao randomizar essas posições e rastrear as variantes geradas, descobriram um triplo mutante — denominado PcAOx‑VPN — capaz de processar eficientemente álcoois maiores como o benzilálcool, enquanto perdia grande parte da atividade original em relação a moléculas pequenas como o metanol.
Talento inesperado: formando ésteres em água
Ao testar o PcAOx‑VPN em misturas destinadas a dissolver substratos oleosos, a equipe notou picos extras em suas análises. Eram produtos acetilados: a enzima estava transferindo um grupo acila de um doador de éster ativado para álcoois, uma reação conhecida como transesterificação. Notavelmente, isso ocorreu em tampão aquoso — algo que normalmente favorece hidrólise concorrente, na qual a água ataca e destrói o éster. Aqui, o PcAOx‑VPN uniu álcoois e doadores de acila como acetato de vinila para formar novos ésteres com rendimentos frequentemente acima de 80% e apenas reações laterais modestamente presentes. A mesma enzima atuou sobre uma ampla variedade de álcoois — lineares, aromáticos, quirais e contendo enxofre — e mostrou preferência marcada por uma das formas imagem‑especular em vários casos.
Mantendo a água fora do caminho
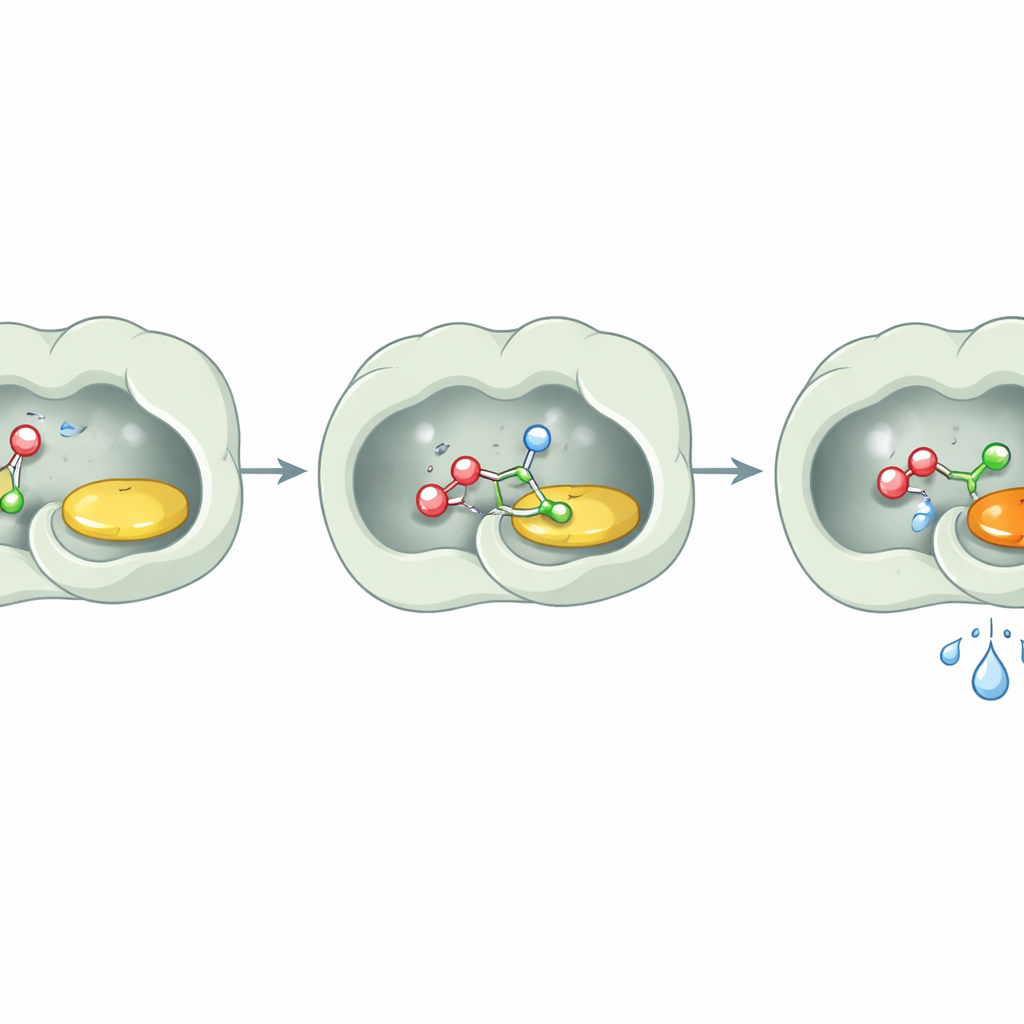
Uma surpresa chave foi o que a enzima não fez: ela não hidrolisou os ésteres de forma notável. Mesmo após longas incubações com substratos éster e água, o PcAOx‑VPN os deixou essencialmente intactos, a menos que um doador de acila adicional fosse fornecido. Estudos estruturais oferecem uma explicação simples. O sítio ativo é revestido por aminoácidos aromáticos e em grande parte oleosos que criam um bolso altamente hidrofóbico. Análises detalhadas não encontraram moléculas de água próximas ao cofator flavínico, e ferramentas computacionais confirmaram que o canal que leva ao sítio ativo também é pouco receptivo à água. Em essência, a enzima constrói uma pequena sala seca dentro de um mundo aquoso. Álcoois e ésteres ativados podem entrar e reagir, mas as moléculas de água são mantidas à distância, de modo que não têm chance de degradar o produto.
Como a reação provavelmente funciona internamente
Experimentos mecanísticos e análise de mutações revelaram que dois aminoácidos, uma histidina e uma asparagina, são centrais tanto para o papel natural de oxidação da enzima quanto para seu novo talento para transesterificação. A histidina atua como base, ajudando a remover um próton do álcool entrante e tornando‑o mais reativo, enquanto a asparagina estabiliza o estado carregado resultante. Juntos, eles promovem o ataque do álcool ao doador de acila para formar um intermediário de curta vida que colapsa no éster desejado. O estado oxidado do cofator flavínico também é necessário: sob condições sem oxigênio, quando o flavina se reduz, a transesterificação cessa e só recomeça quando o ar é reintroduzido. Notavelmente, quando o mesmo trio de mutações foi instalado em oxidases relacionadas de outros fungos, essas enzimas também adquiriram atividade robusta de transesterificação, sugerindo que esse comportamento pode ser generalizável.
O que isso significa para uma química mais verde
Para não especialistas, a mensagem central é que os autores ensinaram uma enzima conhecida a um novo truque: construir ésteres úteis diretamente em água, enquanto efetivamente ignoram a tendência da água de desfazer o trabalho. Ao esculpir um bolso seco e favorável a óleos dentro de uma proteína e ajustar alguns aminoácidos chave, criaram um catalisador que prefere álcoois à água como parceiro reacional. Como o mesmo princípio de projeto funciona em enzimas relacionadas, essa abordagem pode ser estendida a uma família de catalisadores para fabricar aromas, fragrâncias, químicos finos e possivelmente biocombustíveis em processos mais seguros e sustentáveis que dependem menos de solventes orgânicos agressivos e mais da água.
Citação: Wu, B., Ma, Y., Feng, C. et al. Engineered alcohol oxidases catalyse transesterification in aqueous media without competing hydrolysis. Nat Commun 17, 2183 (2026). https://doi.org/10.1038/s41467-026-68899-y
Palavras-chave: engenharia de enzimas, biocatálise, química verde, síntese de ésteres, flavoproteínas