Clear Sky Science · pt
Adaptação pós-traducional mediada por PRMT3 ao jejum regula a flexibilidade metabólica
Por que o horário das refeições e o combustível corporal importam
Muitas pessoas experimentam o jejum ou a alimentação com restrição de tempo para perder peso ou melhorar a glicemia, mas os resultados podem ser variáveis. Este estudo examina o funcionamento interno do nosso metabolismo para entender por quê. Focando na gordura abdominal em camundongos e em amostras humanas, os pesquisadores descobriram um interruptor molecular que ajuda o tecido adiposo a decidir entre queimar ou armazenar combustível, e mostram como tanto o horário das refeições quanto um medicamento podem virar esse interruptor em favor da saúde.
Um motor flexível dentro da nossa gordura
Nosso corpo funciona melhor quando consegue alternar suavemente entre queimar gordura durante o jejum e queimar açúcar após as refeições. Essa “flexibilidade metabólica” muitas vezes se perde na obesidade, tornando mais difícil lidar com flutuações na oferta e na demanda de energia. A equipe estudou a gordura branca visceral — a gordura profunda do abdome fortemente associada ao diabetes e às doenças cardíacas — e descobriu que marcas químicas específicas em proteínas, chamadas grupos metil, mudam com a alimentação e o jejum. Em camundongos e em humanos, duas dessas marcas, MMA e ADMA, se acumulam na gordura visceral conforme aumentam o peso corporal e o índice de massa corporal, sugerindo que são marcadores de um metabolismo lento e menos adaptável.
Um sinal alimentar que rígido o metabolismo
Os pesquisadores focaram em uma enzima nas células adiposas chamada PRMT3, que adiciona essas marcas de metil. Em camundongos, os níveis de PRMT3 na gordura visceral aumentam durante a noite, quando os animais se alimentam, e caem durante o dia, quando jejuam, acompanhando de perto o padrão de MMA e ADMA. Esse ritmo depende da insulina e de uma proteína de sinalização chave, AKT: quando a comida ou a insulina injetada ativa AKT, o PRMT3 é ligado e mais intensamente modificado, o que por sua vez aumenta a quantidade de proteínas metiladas. Bloquear AKT ou inibir diretamente o PRMT3 achata rapidamente esse sinal de metilação, chegando a imitar o efeito de um jejum muito mais longo.
Reconfigurando células de gordura do armazenamento para a queima
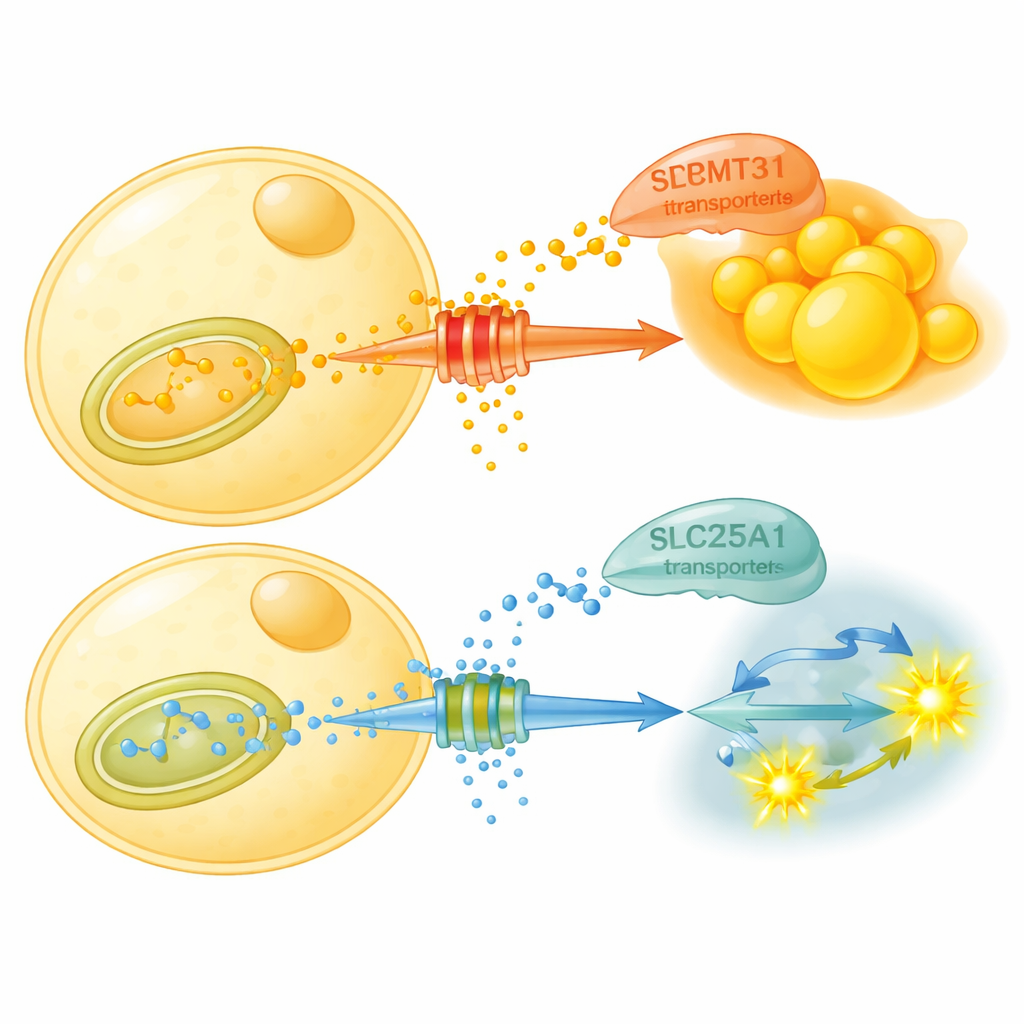
O que essa marcação química realmente faz? O estudo mostra que o PRMT3 estabiliza uma proteína transportadora chamada SLC25A1 nas mitocôndrias — as usinas de energia da célula. SLC25A1 transporta citrato, um intermediário metabólico chave, para fora das mitocôndrias para o fluido celular, onde alimenta a produção de nova gordura. O PRMT3 metila dois sítios específicos de arginina na SLC25A1, tornando o transportador mais estável e incentivando a exportação de citrato e a formação de gordura. Quando o PRMT3 é bloqueado, os níveis de SLC25A1 caem, a exportação de citrato diminui e as células adiposas mudam para degradar açúcar em vez de produzir mais gordura. Em camundongos alimentados com uma dieta rica em gordura, um fármaco que bloqueia o PRMT3 reduz a gordura corporal, melhora o controle da glicemia e aumenta uma medida chamada razão de troca respiratória, mostrando que os animais alternam com mais facilidade para queimar carboidratos.
Programas de jejum e alterações genéticas apontam para a mesma via
Os pesquisadores então perguntaram se padrões comuns de jejum usam esse mesmo interruptor. Sob um protocolo de alimentação com restrição de tempo 16:8 — 16 horas de jejum e 8 horas de alimentação — os camundongos perderam peso e melhoraram o manejo da glicose sem reduzir o consumo calórico total. A gordura visceral deles mostrou níveis mais baixos de PRMT3, SLC25A1 e proteínas metiladas, e o uso de combustível ficou mais flexível, especialmente à noite, quando normalmente se alimentam. Notavelmente, administrar o fármaco que bloqueia o PRMT3 em horários específicos do dia produziu muitos dos mesmos benefícios do protocolo 16:8. Remover geneticamente a SLC25A1 apenas nas células adiposas também protegeu os camundongos da hiper glicemia e do fígado gorduroso induzidos pela dieta, novamente ao aumentar a degradação de açúcar e o uso de energia no tecido adiposo, mesmo sem reduzir a massa de gordura.
O que isso significa para terapias futuras
Em conjunto, os achados sugerem que a gordura abdominal profunda contém um interruptor sensível ao tempo, controlado por insulina, AKT, PRMT3 e SLC25A1, que determina se nossos corpos permanecem metabolicamente ágeis ou ficam travados em um modo de armazenamento. A alimentação com restrição de tempo parece empurrar esse interruptor em direção à flexibilidade ao diminuir o PRMT3 e seus efeitos downstream. Um medicamento que iniba o PRMT3 pode reproduzir muitas dessas vantagens em camundongos obesos, sugerindo uma futura droga que torne os benefícios metabólicos do jejum mais acessíveis. Para leitores em geral, a mensagem é que quando comemos, e não apenas o que comemos, pode remodelar a forma como o tecido adiposo lida com o combustível — com consequências importantes para o peso, a glicemia e a saúde a longo prazo.
Citação: Huang, Z., Liu, X., Chen, X. et al. PRMT3-mediated post-translational adaptation to fasting regulates metabolic flexibility. Nat Commun 17, 2264 (2026). https://doi.org/10.1038/s41467-026-68883-6
Palavras-chave: flexibilidade metabólica, alimentação com restrição de tempo, gordura visceral, metilação de proteínas, metabolismo da glicose