Clear Sky Science · pt
Um nanodispositivo baseado em DNA detecta sinalização purinérgica e aciona um interruptor imunológico para resolver a inflamação
Reduzindo o sistema de alarme do corpo
Quando nossos tecidos são lesionados, as células liberam uma explosão de “sinais de alarme” químicos que atraem células imunes para combater infecções e remover detritos. Essa resposta é vital, mas se o alarme tocar alto demais ou por tempo demais, pode causar inflamação nociva nos pulmões, rins e outros órgãos. Este estudo descreve um dispositivo minúsculo e programável, baseado em DNA, que consegue detectar quando o sinal de alarme está forte demais e silenciosamente reduzi-lo, ajudando o sistema imune a mudar do modo ataque para o modo reparação.
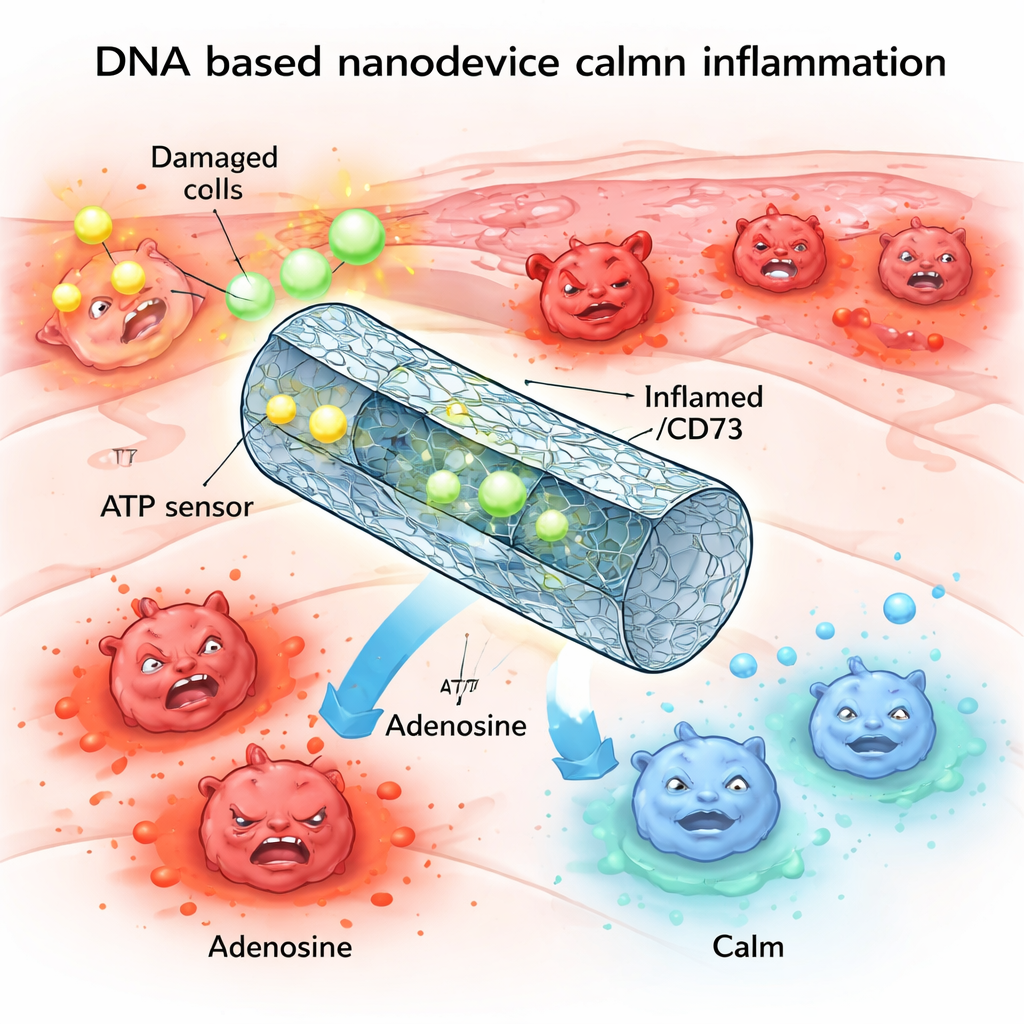
Um alarme químico que pode passar do limite
Uma das moléculas de alarme do corpo é o ATP, mais conhecido como a “moeda energética” dentro das células. Durante lesão ou estresse, grandes quantidades de ATP vazam de células danificadas para o espaço extracelular. Ali, esse ATP extracelular atua como um sinal de socorro, ligando-se a receptores em células imunes e empurrando-as para um estado altamente inflamatório. Em condições saudáveis, enzimas na superfície celular degradam rapidamente o excesso de ATP em adenosina, uma molécula relacionada que tem efeito calmante e anti-inflamatório. Mas em muitas doenças inflamatórias crônicas ou graves, essa maquinaria de degradação está prejudicada, deixando o ATP alto, a adenosina baixa e os tecidos presos em um ciclo de dano.
Construindo um tubo inteligente de DNA
Os pesquisadores propuseram imitar e reparar esse sistema de controle natural usando nanotecnologia de DNA. Eles construíram um tubo oco de DNA, dobrado de forma semelhante ao origami, e o equiparam com dois componentes principais: “sensores” que reconhecem ATP e enzimas que convertem ATP em adenosina. Em seu estado de repouso, travado, o tubo fica fechado por segmentos curtos de DNA que também funcionam como sensores de ATP. Quando os níveis de ATP sobem acima de um determinado limiar típico de tecidos lesionados, o ATP se liga a esses segmentos, fazendo o tubo abrir e expor as enzimas ENPP1 e CD73 em seu interior. Estas então degradam o excesso de ATP e produzem adenosina, deslocando suavemente o equilíbrio químico local do perigo para a resolução.
Comprovando que o interruptor funciona
Em testes de laboratório controlados, a equipe confirmou que seu tubo de DNA permanece fechado em baixos níveis de ATP, mas se abre de forma confiável quando o ATP se torna abundante, muito parecido com uma válvula de emergência. Uma vez destravado, o dispositivo converte continuamente o ATP em produtos intermediários e, finalmente, em adenosina, sem prejudicar significativamente a atividade das enzimas. Em células imunes expostas a altos níveis de ATP, esse nanodispositivo reduziu subprodutos tóxicos nas mitocôndrias, diminuiu a ativação de vias inflamatórias como NF-κB e o inflamassoma NLRP3, e aumentou sinais ligados às ações calmantes da adenosina. Em outras palavras, o dispositivo fez mais do que apenas eliminar o ATP; ele reorganizou ativamente o comportamento celular de inflamatório para regulatório.
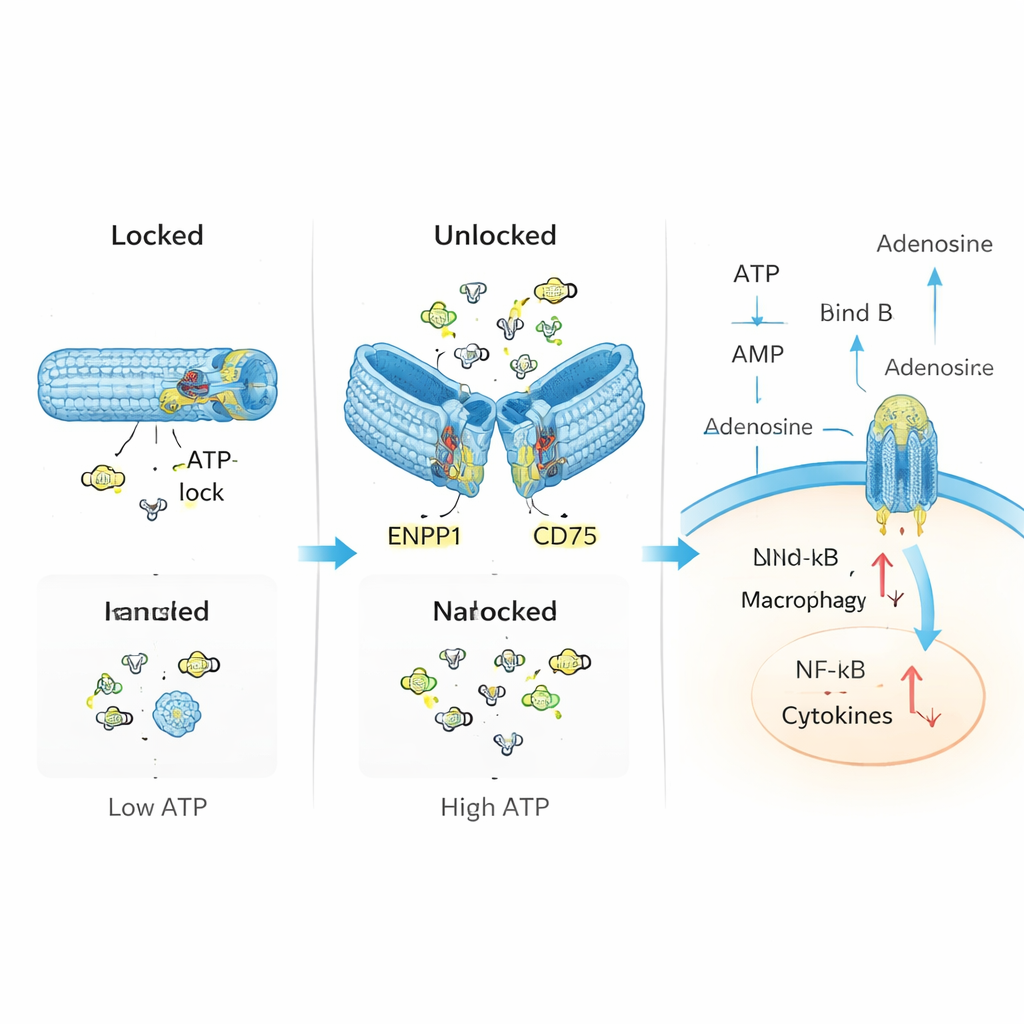
Carregando até os locais de lesão
Projetar um interruptor inteligente é uma coisa; levá-lo ao local certo no corpo é outra. Para resolver esse problema de entrega, os pesquisadores anexaram seus tubos de DNA à superfície de monócitos circulantes, um tipo de leucócito que naturalmente migra para tecidos inflamados. Usando uma âncora de DNA ligada ao colesterol, eles “estacionaram” um grande número de nanodispositivos na membrana de cada célula, onde os dispositivos permaneceram majoritariamente na superfície em vez de serem engolidos pela célula. Em modelos murinos de lesão aguda dos pulmões e dos rins, esses monócitos decorados se acumularam nos órgãos danificados muito mais eficientemente do que dispositivos livres em circulação, e os nanodispositivos ainda responderam especificamente ao alto ATP nos tecidos lesionados.
Auxiliando a cura dos tecidos
Em camundongos com lesão pulmonar ou renal induzida quimicamente, o tratamento com o dispositivo de DNA reduziu o dano tecidual, o acúmulo de células imunes e as moléculas mensageiras inflamatórias. A versão transportada por monócitos funcionou melhor, oferecendo proteção mais forte do que o dispositivo livre ou as enzimas isoladas. Análises genéticas e metabólicas mais profundas dos tecidos pulmonares mostraram que essa abordagem não apenas diminuiu genes inflamatórios, mas também ajudou a restaurar o metabolismo energético perturbado nas células. Importante, os dispositivos mostraram baixa toxicidade e não desencadearam reações imunes prejudiciais em animais saudáveis.
Por que isso importa para terapias futuras
Para um público não especializado, a mensagem principal é que este trabalho demonstra um “termostato” molecular programável para inflamação. Construído a partir de DNA e enzimas naturais, o nanodispositivo detecta quando um sinal de perigo está forte demais e o converte automaticamente em um sinal calmante, ajudando as células imunes a se acalmarem e os tecidos a se repararem. Embora ainda em estágio experimental inicial, essa estratégia sugere uma nova classe de tratamentos que não bloqueiam simplesmente vias imunes por toda parte, mas reequilibram localmente os sinais químicos nos locais de lesão, oferecendo potencialmente controle preciso sobre inflamações prejudiciais em muitas doenças.
Citação: Li, W., Liu, S., Zhou, X. et al. A DNA-based nanodevice senses purinergic signaling and drives an immune switch for resolving inflammation. Nat Commun 17, 2030 (2026). https://doi.org/10.1038/s41467-026-68879-2
Palavras-chave: nanodispositivo de DNA, ATP extracelular, inflamação, sinalização por adenosina, nanomedicina