Clear Sky Science · pt
Imunoterapia anti-TLR2 modula a propagação de α-sinucleína de neurônios para oligodendrócitos em modelos murinos e humanos
Por que esta pesquisa importa
A atrofia de múltiplos sistemas (AMS) é um distúrbio cerebral raro, porém de progressão rápida, que combina problemas de movimento semelhantes ao Parkinson com falhas do equilíbrio e do sistema autonômico, como quedas de pressão arterial. Os médicos conseguem aliviar sintomas, mas atualmente não conseguem desacelerar a doença em si. Este estudo revela como uma proteína mal dobrada se espalha entre células cerebrais para danificar o "isolamento dos fios" do cérebro, e mostra que um tratamento com anticorpo direcionado pode interromper esse processo em modelos animais e celulares. O trabalho aponta para uma estratégia concreta e com potencial farmacológico que, um dia, pode alterar o curso da AMS em vez de apenas tratar seus sintomas.
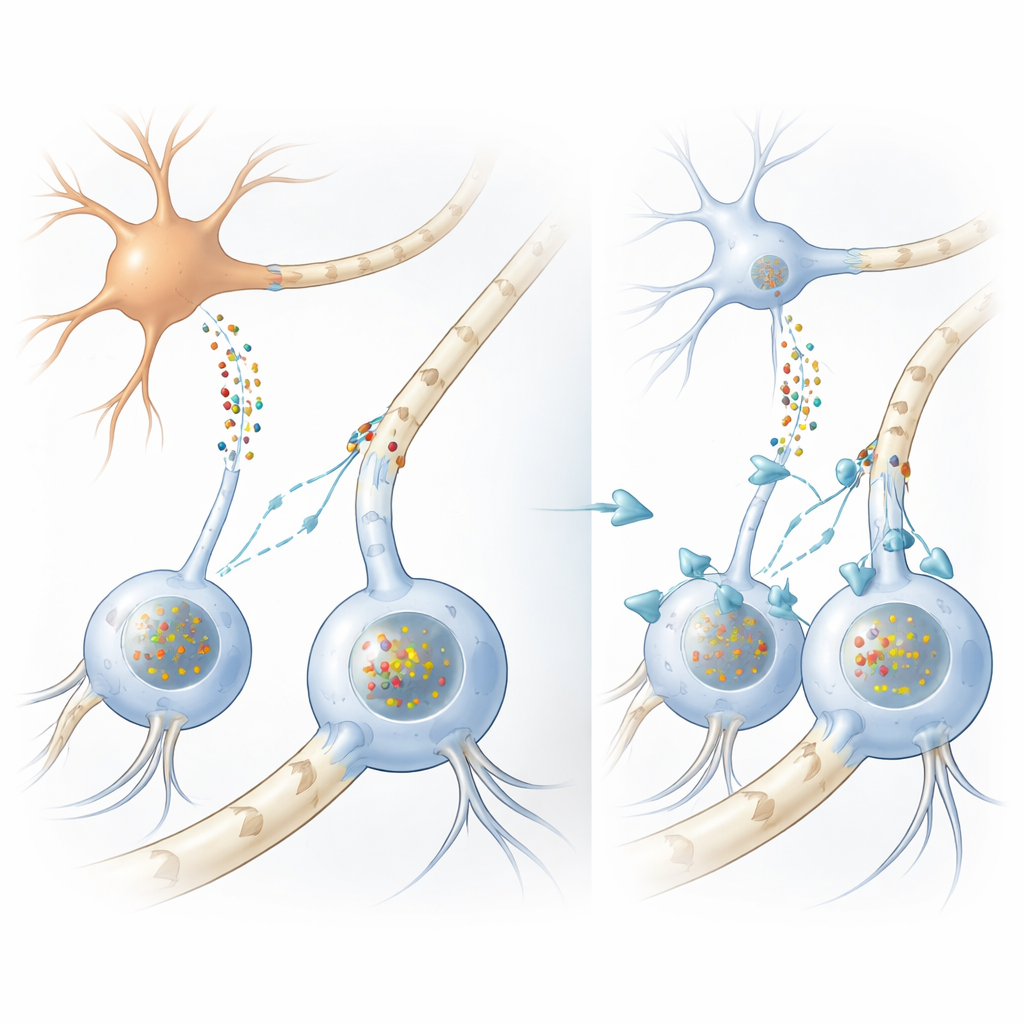
Como o circuito cerebral se altera
Em muitos distúrbios do movimento, incluindo a doença de Parkinson, aglomerados de uma proteína chamada alfa-sinucleína se acumulam dentro de neurônios. Na AMS, contudo, os aglomerados mais marcantes se formam dentro de células de suporte chamadas oligodendrócitos, que normalmente envolvem os axônios com bainhas gordurosas de mielina que aceleram os sinais elétricos. Curiosamente, os oligodendrócitos produzem muito pouca alfa-sinucleína por conta própria, deixando um enigma antigo: de onde vêm os depósitos maciços dessa proteína nessas células? Os autores primeiro confirmaram, usando amostras cerebrais humanas e análises de RNA em larga escala, que os oligodendrócitos realmente produzem bem menos alfa-sinucleína do que os neurônios, reforçando a ideia de que a proteína nociva deve chegar de fora.
Proteína transmitida do neurônio para a célula de suporte
Para testar isso, a equipe construiu vários modelos complementares. Em placas, cultivaram células humanas semelhantes a oligodendrócitos a partir de células-tronco neurais e as submeteram a meio condicionado por células semelhantes a neurônios que foram geneticamente modificadas para liberar grandes quantidades de alfa-sinucleína. As células de suporte captaram essa proteína e desenvolveram aglomerados muito parecidos com as inclusões gliais observadas em cérebros de AMS, com as mesmas marcas químicas e proteínas auxiliares. Quando os pesquisadores observaram uma linhagem de camundongos que produz alfa-sinucleína humana mutante apenas em neurônios, encontraram novamente aglomerados da proteína humana dentro de oligodendrócitos na substância branca, apesar de essas células não expressarem o gene humano. Juntos, esses experimentos mostram que a alfa-sinucleína pode se mover de neurônios para oligodendrócitos e formar inclusões semelhantes às da doença.
A porta na superfície celular
Em seguida, os cientistas investigaram como a proteína entra nos oligodendrócitos. Trabalhos anteriores haviam identificado o sensor imune Toll-like receptor 2 (TLR2) na superfície celular como um ponto de ancoragem para a alfa-sinucleína em neurônios e microglia. Ao explorar conjuntos de dados de expressão gênica de cérebros de pacientes com AMS, a equipe descobriu que os oligodendrócitos desses pacientes apresentavam níveis incomumente altos de TLR2 em comparação com controles, e que níveis mais altos de TLR2 estavam ligados a níveis mais baixos de genes relacionados à mielina, como a proteína básica da mielina. Essa relação não apareceu em diversos conjuntos de dados independentes de Parkinson, sugerindo que a sensibilidade dos oligodendrócitos à alfa-sinucleína via TLR2 é uma característica distintiva da AMS, e não um traço geral de todos os distúrbios sinucleínicos.
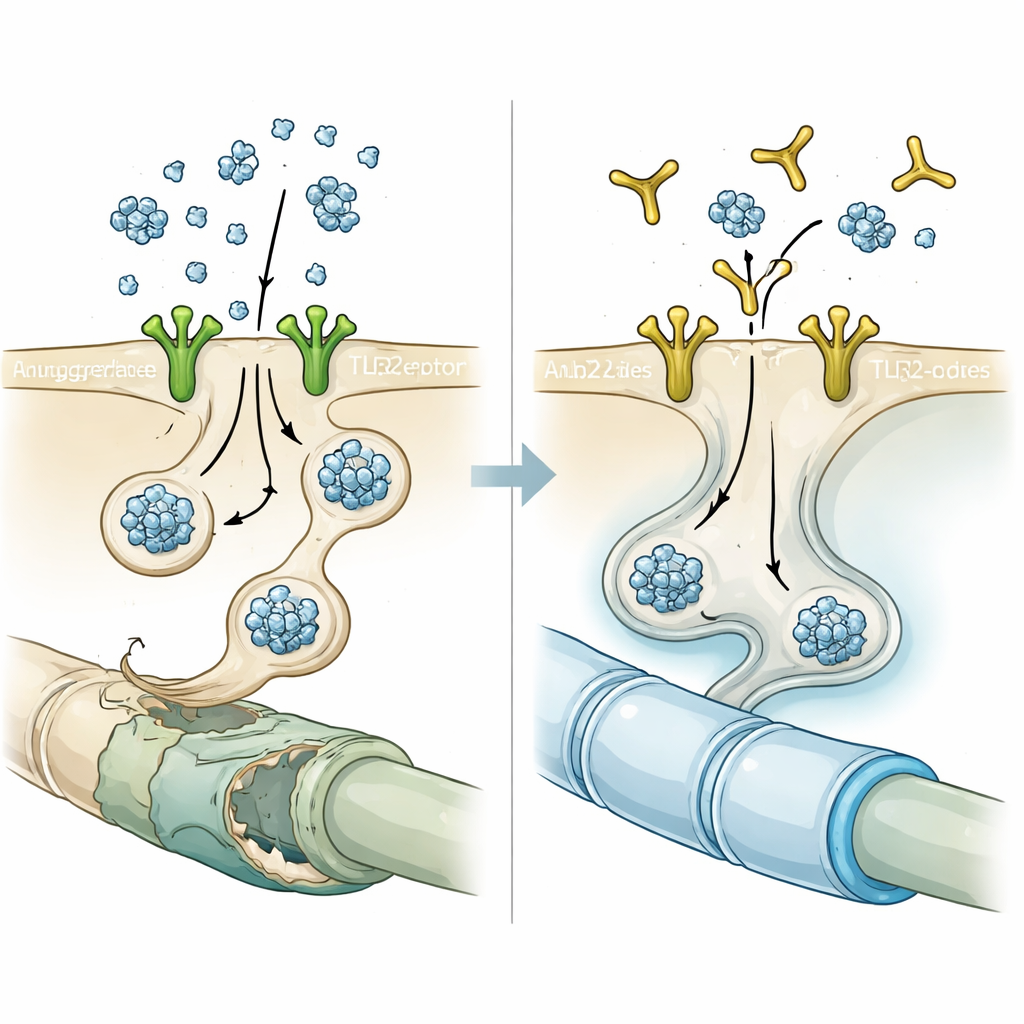
Bloqueando a porta com um anticorpo
Munidos dessa pista, os pesquisadores testaram o NM-101, um anticorpo projetado para se ligar ao TLR2 e impedir sua ativação. Em culturas celulares, o pré-tratamento breve de oligodendrócitos com NM-101 antes de adicionar alfa-sinucleína derivada de neurônios reduziu fortemente o número e a intensidade dos aglomerados semelhantes a inclusões. Em camundongos que ou superproduziam alfa-sinucleína neuronal ou receberam injeções de fibrilas pré-formadas de alfa-sinucleína, infusões semanais de NM-101 diminuíram a proteína agregada na substância branca, atenuaram respostas inflamatórias de microglia e astrócitos e reduziram a ativação de uma enzima inflamatória chamada caspase-1 dentro dos oligodendrócitos. Animais tratados viveram mais e tiveram desempenho melhor em testes motores, sugerindo que os efeitos protetores do anticorpo eram funcionalmente relevantes, e não apenas curiosidades microscópicas.
Resgatando o isolamento danificado
Como os oligodendrócitos são os produtores de mielina do cérebro, a equipe examinou se a transferência de alfa-sinucleína prejudicava a mielina e se o bloqueio de TLR2 poderia ajudar. Sequenciamento de RNA de célula única de oligodendrócitos derivados de humanos expostos à alfa-sinucleína condicionada por neurônios revelou mudanças amplas, afastando-se de um estado maduro produtor de mielina para um perfil mais imaturo, semelhante ao de progenitores, com muitos genes-chave da mielina reprimidos. Estudos paralelos de expressão gênica em oligodendrócitos capturados por laser de pacientes com AMS e do modelo murino mostraram uma assinatura comum: redução da expressão de genes envolvidos na formação e manutenção da mielina. Ao microscópio eletrônico, a substância branca dos camundongos com alfa-sinucleína exibiu bainhas de mielina mais finas e desorganizadas. O tratamento com NM-101 reverteu muitas dessas alterações, espessando a mielina, restaurando níveis de proteínas da mielina e normalizando a expressão de genes necessários para a maturação dos oligodendrócitos.
O que tudo isso significa para tratamentos futuros
O estudo sustenta uma narrativa clara: na AMS, a alfa-sinucleína produzida por neurônios pode se espalhar para oligodendrócitos por meio do TLR2 em sua superfície, onde se acumula, desencadeia inflamação, desvia o programa de desenvolvimento das células e corrói o revestimento de mielina dos circuitos cerebrais. Ao bloquear o TLR2 com um anticorpo direcionado, os pesquisadores foram capazes de interromper essa cadeia de eventos em modelos murinos e celulares humanos, reduzindo inclusões tóxicas, acalmando a inflamação, reparando a mielina e melhorando a sobrevivência e a motricidade. Embora o próprio NM-101 ainda precise de testes rigorosos em humanos, o trabalho estabelece a transferência proteica dependente de TLR2 como um motor central da patologia similar à AMS e destaca a imunoterapia anti-TLR2 como uma estratégia promissora para desacelerar ou prevenir essa doença devastadora.
Citação: Bae, EJ., Ham, S., Jeong, Y.W. et al. Anti-TLR2 immunotherapy modulates neuron-to-oligodendrocyte propagation of α-synuclein in mouse and human models. Nat Commun 17, 2175 (2026). https://doi.org/10.1038/s41467-026-68870-x
Palavras-chave: atrofia de múltiplos sistemas, alfa-sinucleína, oligodendrócitos, danos à mielina, imunoterapia