Clear Sky Science · pt
Evolução coordenada de famílias gênicas molda o genoma de Mucorales dimórficos
Um fungo, dois corpos
Alguns fungos podem viver uma vida dupla, alternando entre uma forma unicelular “levedura” e uma forma ramificada de “bolor”. Essa habilidade de mudar de forma os ajuda a sobreviver a ambientes em mudança e, em alguns casos, a invadir tecidos humanos. O estudo aqui resumido revela como um grupo desses fungos, os Mucorales, reorganiza e utiliza seus genes para sustentar ambos os estilos de vida dentro de um mesmo genoma.
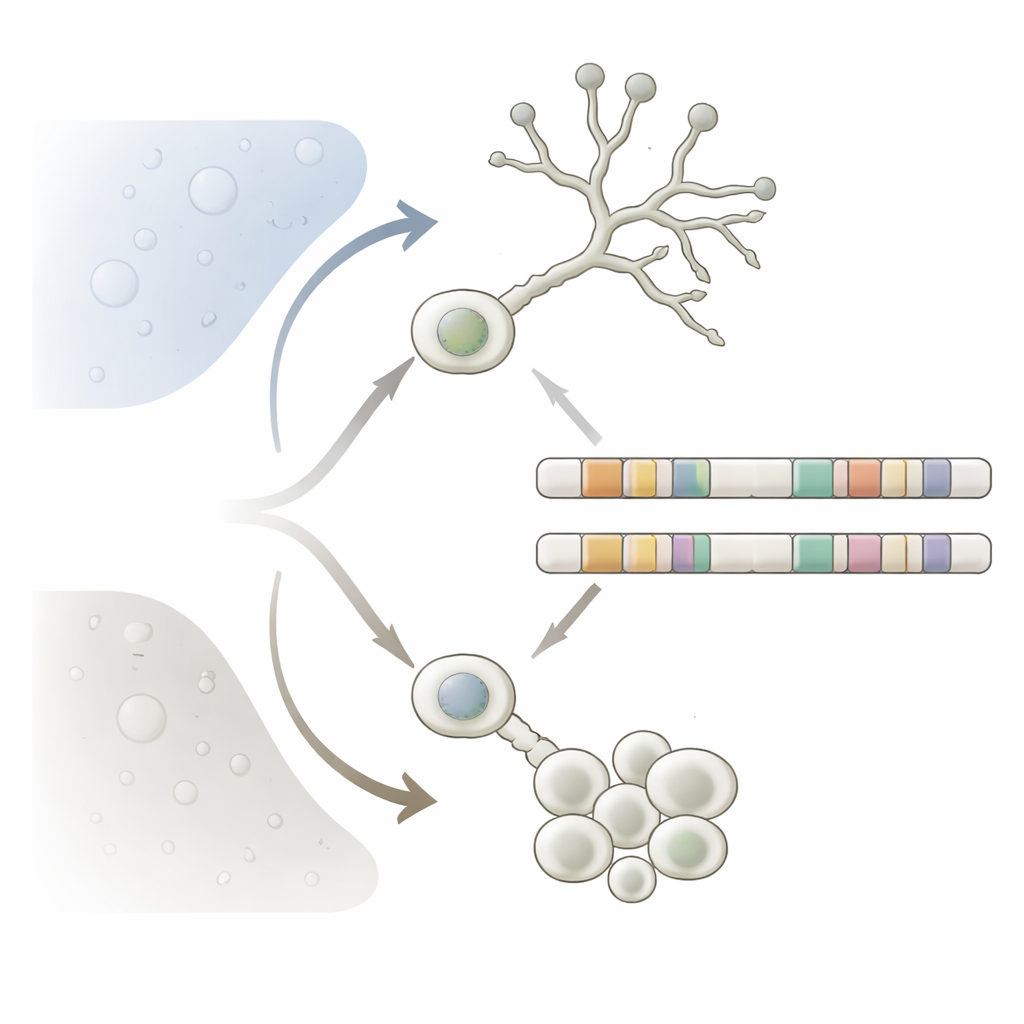
Por que fungos que mudam de forma importam
Fungos dimórficos são importantes não só para a ecologia, mas também para a saúde humana. Nos Mucorales, a forma leveduriforme é composta por células redondas isoladas que favorecem condições com baixo oxigênio e ricas em açúcar, crescendo por brotamento. A forma micelial forma longos filamentos que prosperam em ambientes ricos em oxigênio e podem invadir tecidos e superfícies. Em várias espécies de Mucorales, apenas a forma filamentosas é fortemente infecciosa, causando mucormicose, uma doença severa em pessoas com o sistema imune debilitado. Entender como esses fungos trocam de forma pode revelar por que são tão adaptáveis, por que resistem a alguns medicamentos e quais características genéticas distinguem espécies dimórficas perigosas de suas parentes inofensivas.
Um genoma concebido para alternância
Os autores focaram no fungo modelo Mucor lusitanicus e acompanharam-no em quatro estágios: levedura, micélio inicial, a reversão de volta à levedura e micélio maduro. Ao sequenciar RNA, mediram quais genes estavam ativos em cada estado. Eles descobriram que cerca de 70% de todos os genes alteram sua atividade durante a mudança de forma, muito mais do que em muitos outros fungos. Células em forma de levedura tendem a ativar genes para metabolismo básico e síntese de blocos construtores celulares, enquanto micélios favorecem genes envolvidos em sinalização interna e no citoesqueleto, que dá suporte ao crescimento filamentoso. Essa ampla reprogramação mostra que o dimorfismo não é um ajuste menor, mas uma reconfiguração de organismo inteiro.
Genes duplicados com funções divididas
Uma descoberta central é que muitos genes existem em pares ou pequenas famílias cujas cópias se especializaram para uma forma ou outra. A equipe primeiro revisitou um exemplo conhecido: dois genes ferroxidase e dois genes transportadores de ferro que, em conjunto, importam ferro, um nutriente vital. Um membro de cada par é usado na levedura, o outro no micélio. Deletar as cópias específicas da levedura prejudicou o crescimento em levedura, mas deixou o crescimento micelial em grande parte intacto, e o inverso aconteceu com as cópias miceliais. Estendendo essa análise a todo o genoma, os pesquisadores identificaram 490 dessas “famílias dimórficas” nas quais ao menos uma cópia é específica de levedura e outra é específica de micélio. No total, aproximadamente um em cada nove genes do genoma pertence a tais famílias, cobrindo muitos papéis celulares diferentes. Isso sugere que, em vez de depender de uma única versão de uma proteína para funcionar em todas as condições, o fungo evoluiu versões gêmeas ajustadas às condições muito diferentes da vida leveduriforme líquida e pobre em oxigênio versus a vida micelial sólida e rica em oxigênio.
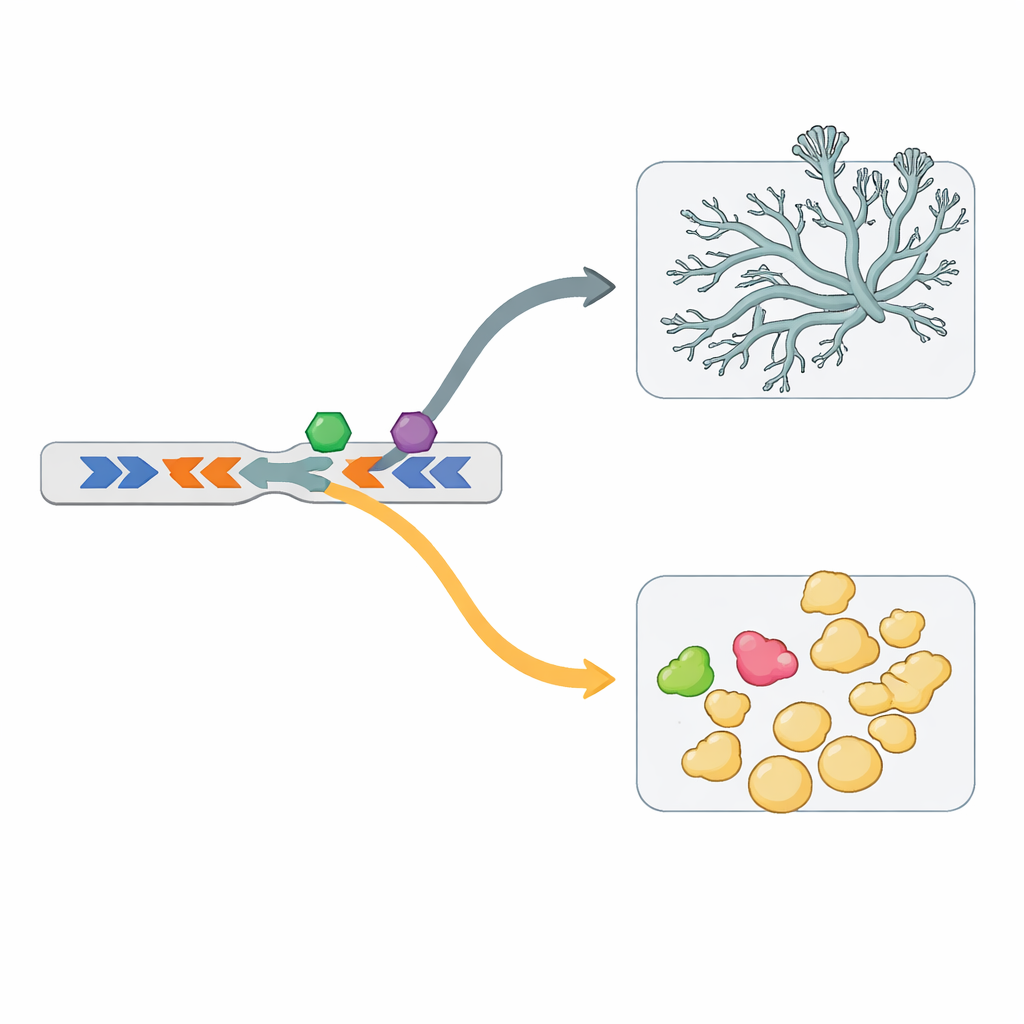
Genes em frente a frente e novos interruptores de controle
O genoma não apenas duplica genes, mas também os organiza em disposições especiais. Muitos dos genes de importação de ferro, por exemplo, ficam em pares “cabeça a cabeça”: dois genes colocados em direções opostas, compartilhando uma região central de controle. Um desses pares é ativo na levedura, o par vizinho no micélio. Trocar experimentalmente essas regiões de controle compartilhadas inverteu o momento em que cada gene era ativado, provando que esse arranjo funciona como um interruptor coordenado. Uma varredura por todo o genoma encontrou mais de mil desses pares cabeça a cabeça, com centenas envolvidos no dimorfismo. As regiões de controle compartilhadas para pares ligados à levedura e ao micélio carregam motivos de DNA distintos, implicando que são lidas por fatores regulatórios diferentes.
Reguladores mestres e pistas evolutivas
Para encontrar esses reguladores, os pesquisadores usaram o DNA das regiões de controle compartilhadas dos genes de importação de ferro como isca para capturar proteínas que se ligam ali. Eles identificaram duas proteínas anteriormente não caracterizadas, chamadas DFL e DKL, e criaram linhagens mutantes sem cada uma delas. Esses mutantes exibiram um bloqueio acentuado na alternância: mutantes DKL não conseguiam mais formar levedura, e ambos os mutantes perderam o padrão normal de ativação gênica em milhares de genes relacionados ao dimorfismo. Observando espécies relacionadas, a equipe verificou que Mucorales dimórficos tendem a manter famílias gênicas duplicadas e específicas por forma, estruturas cabeça a cabeça e o gene dfl, enquanto fungos próximos que não trocam de forma frequentemente carecem dessas características. Esse padrão sugere que esses traços genômicos evoluíram em conjunto como um kit para o dimorfismo e podem servir como marcadores para prever quais espécies provavelmente são mudadoras de forma.
O que isso significa para doenças fúngicas
Em termos simples, este trabalho mostra que fungos Mucorales reconstruíram seus genomas em torno do desafio de viver duas vidas separadas. Eles resolvem isso duplicando genes importantes, ajustando uma cópia para levedura e a outra para micélio, conectando muitos deles em unidades de controle frente a frente e usando reguladores dedicados para coordenar qual versão é usada em cada momento. Como a forma invasiva e causadora de doença costuma ser o micélio, e porque alguns dos genes afetados lidam com captação de ferro e sensibilidade a medicamentos, essas descobertas apontam para novas formas de prever quais fungos podem se tornar perigosos e de projetar tratamentos que interrompam sua capacidade de mudar de forma.
Citação: Tahiri, G., Navarro-Mendoza, M.I., Lax, C. et al. Coordinated gene family evolution shapes the genome of dimorphic Mucorales. Nat Commun 17, 2148 (2026). https://doi.org/10.1038/s41467-026-68866-7
Palavras-chave: dimorfismo fúngico, Mucorales, duplicação gênica, regulação do genoma, patogênese fúngica