Clear Sky Science · pt
Empilhamento antiparalelo de pili Csu impulsiona a montagem tridimensional de biofilmes de Acinetobacter baumannii
Como germes hospitalares constroem cidades protegidas
Alguns dos germes hospitalares mais resistentes sobrevivem aos antibióticos escondendo-se em comunidades viscosas e tridimensionais chamadas biofilmes. Este estudo faz uma pergunta simples, porém crucial: como bactérias isoladas se entrelaçam para formar estruturas em camadas tão robustas? Ao ampliar com microscópios eletrônicos avançados, os pesquisadores descobriram um “Velcro” microscópico feito de filamentos semelhantes a pelos que permitem ao patógeno perigoso Acinetobacter baumannii tecer-se em aglomerados 3D protetores. Compreender essa estrutura de suporte oculta pode abrir novas maneiras de desmontar biofilmes e tornar os medicamentos existentes mais eficazes.
Pelinhos minúsculos que mantêm as bactérias unidas
A. baumannii, uma causa importante de infecções hospitalares de difícil tratamento, está coberta por finos pelos superficiais chamados pili Csu. Trabalhos anteriores mostraram que esses pili são essenciais para formar biofilmes robustos em forma de cúpula, mas ninguém sabia como eles realmente trançam as células em uma estrutura 3D. Usando várias formas de microscopia eletrônica, os autores confirmaram primeiro que, em cultura líquida, os pili geralmente sobressaem separadamente de cada bactéria, como espinhos em um carrapicho. Em colônias densas crescidas em superfície, porém, o quadro muda dramaticamente: muitos pili se agrupam firmemente, formando faixas largas e planas que correm entre células vizinhas, criando uma malha extensa e de aparência delicada em três dimensões. 
Escadas planas construídas a partir de filamentos pareados
Para entender como essas faixas se formam, a equipe purificou os pili Csu e observou seu comportamento isolado. Ao longo de dias a semanas, filamentos individuais começaram a emparelhar-se e então a fundir-se em “superacúmulos” multi-filamento, formando eventualmente uma rede semelhante a gel que imitava de perto as estruturas vistas em biofilmes reais. A crio-microscopia eletrônica de alta resolução revelou o projeto subjacente. Cada pilus não é um tubo liso, mas uma haste em ziguezague. Quando duas hastes ficam lado a lado em direções opostas, elas tocam em pontos de canto repetidos, formando junções laterais estáveis. Muitos desses pares antiparalelos podem então alinhar-se em uma pilha muito fina e em forma de chapa — essencialmente uma escada ou fita microscópica que tem apenas um filamento de espessura, mas muitos filamentos de largura.
Um plano embutido para crescimento 3D
As estruturas detalhadas mostram que essa capacidade de empilhamento está codificada na geometria dos próprios pili. O padrão em ziguezague repete-se em uma distância muito curta, criando muitos pontos potenciais de contato ao longo de cada filamento. Como resultado, uma vez que dois pili se encontram na orientação correta, pode formar-se uma cadeia de junções como um zíper, estendendo rapidamente a chapa. Importante, a forma como as hastes se orientam garante que os contatos geralmente ocorram entre pili de células diferentes, e não da mesma, o que promove naturalmente a ligação célula–célula. As pilhas permanecem flexíveis e elásticas, de modo que o biofilme em crescimento pode absorver estresse físico sem se desfazer. Os pesquisadores observaram que durante a divisão celular, células filhas frequentemente ficam com seus pili posicionados frente a frente, o que incentiva a formação de pilhas exatamente onde é necessário para unir as células em um aglomerado 3D. 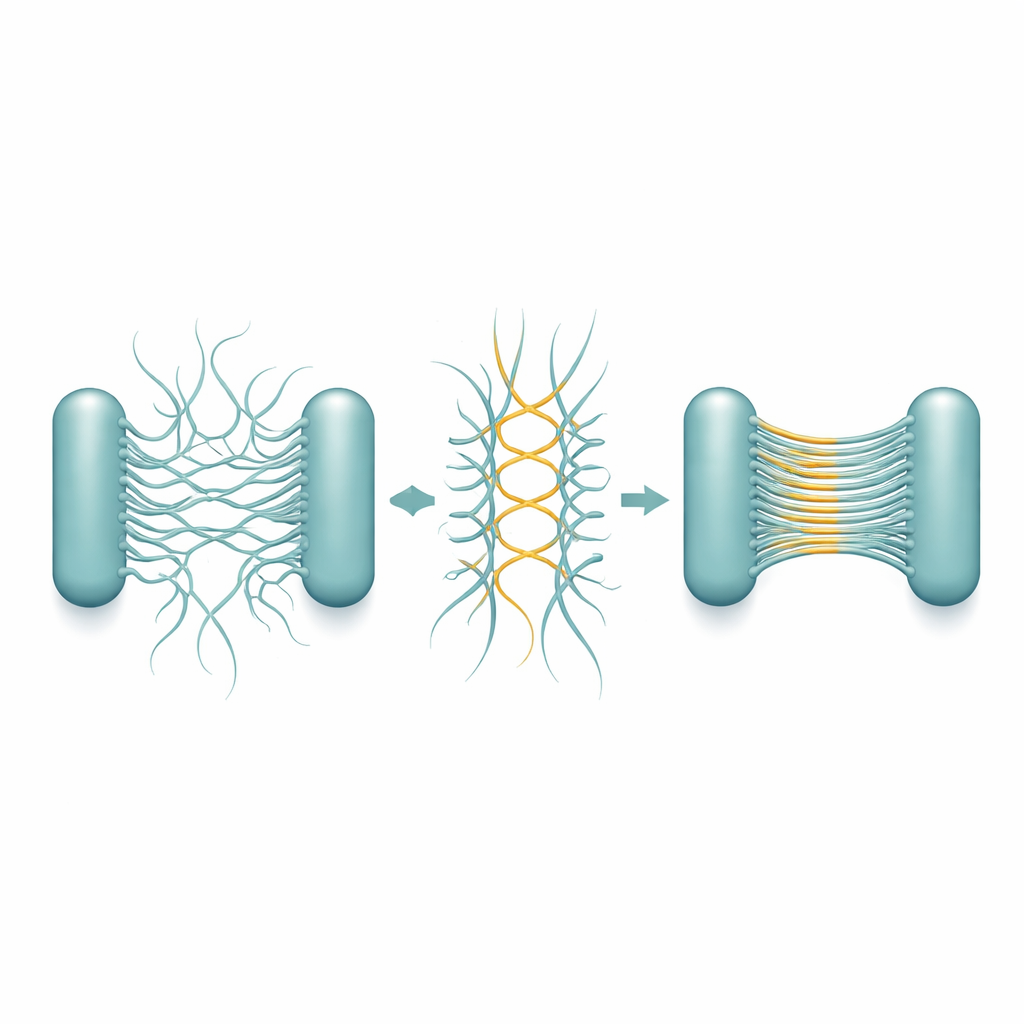
Cola, preenchimento e andaime inicial
O estudo também examinou como outros componentes do biofilme contribuem. Um polímero açucarado chamado PNAG e DNA solto de células rompidas são conhecidos por se acumular em biofilmes maduros. A microscopia revelou essas substâncias preenchendo as fendas estreitas entre as bactérias e envolvendo as pilhas de pili, muito parecido com concreto vertido ao redor de vergalhões de aço. Ainda assim, quando a equipe removeu PNAG e DNA, as bactérias continuaram a formar plataformas organizadas mantidas apenas pelas pilhas de pilus Csu. Isso mostra que os pili constroem o andaime primário, enquanto o material circundante posteriormente cimenta e estabiliza a estrutura.
Novos pontos fracos nas fortalezas bacterianas
Em termos simples, este trabalho explica como A. baumannii usa seus pelos de superfície para entrelaçar-se em aglomerados resistentes e multicamadas que medicamentos e células do sistema imune têm dificuldade em penetrar. Os pili atuam primeiro como ganchos para agarrar superfícies e depois como tiras flexíveis que se empilham em chapas planas, atando células vizinhas em todas as direções. Polímeros açucarados e DNA então preenchem as lacunas, transformando essa rede de tiras em uma fortaleza sólida. Ao identificar a maneira precisa pela qual os pili aderem uns aos outros, o estudo destaca um novo alvo: drogas ou moléculas que bloqueiem os contatos pilus–pilus poderiam enfraquecer os andaimes dos biofilmes por dentro, facilitando a eliminação de infecções bacterianas persistentes.
Citação: Malmi, H., Pakharukova, N., Paul, B. et al. Antiparallel stacking of Csu pili drives Acinetobacter baumannii 3D biofilm assembly. Nat Commun 17, 2508 (2026). https://doi.org/10.1038/s41467-026-68860-z
Palavras-chave: biofilmes, Acinetobacter baumannii, pili, resistência a antibióticos, crio-microscopia eletrônica