Clear Sky Science · pt
respostas cGAS-IFN-I extraindo DNA nuclear de células moribundas via nucleocitose
Como nosso sistema imune lê o DNA dos mortos
Quando nossas células morrem durante infecções, câncer ou pelo desgaste cotidiano, seus restos precisam ser limpos sem provocar inflamação excessiva. Este artigo revela uma forma surpreendente pela qual células imunes podem, na verdade, perfurar o núcleo de células moribundas, extrair seu DNA e usá‑lo como sinal de perigo. Compreender esse sistema oculto de limpeza e alarme pode mudar a maneira como pensamos sobre antivirais, autoimunidade, terapias contra o câncer e efeitos colaterais de medicamentos.
Um alarme de DNA escondido dentro de células imunes
Nossas células têm um sensor chamado cGAS que detecta DNA no lugar errado — flutuando no citosol em vez de estar protegido no núcleo ou nas mitocôndrias. Quando o cGAS encontra esse DNA, ele dispara um programa de alarme potente que produz interferons tipo I, proteínas chave na resposta antiviral e na regulação imune. Os cientistas sabiam que vírus podiam entregar seu material genético às células para ativar essa via, e que pedaços do nosso próprio DNA podem às vezes vazar e causar doenças autoimunes. Mas uma questão básica permanecia: como grandes quantidades do nosso DNA, especialmente vindas de células mortas, alcançam o cGAS sem serem simplesmente digeridas nos “estômagos” celulares chamados lisossomos?
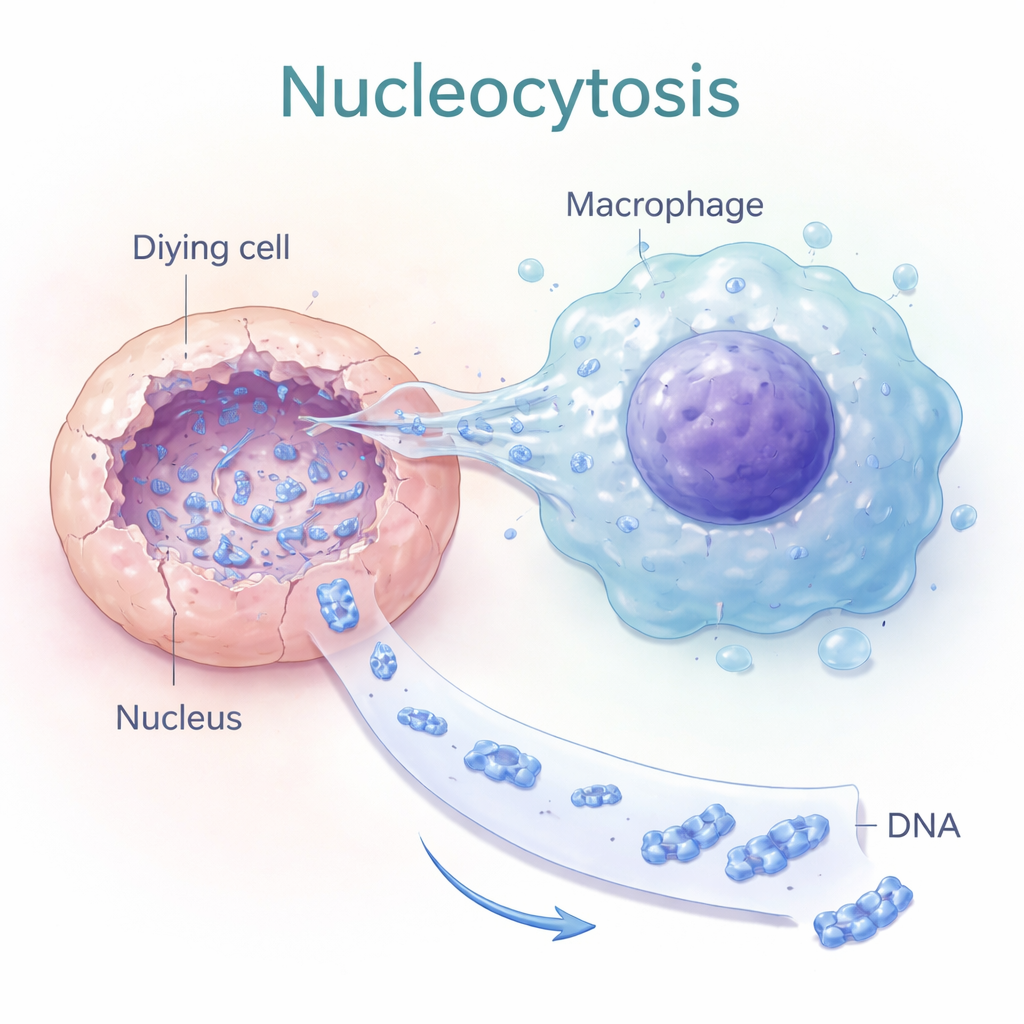
Nucleocitose: perfurando núcleos de células mortas
Os autores descobriram um processo que chamam de “nucleocitose”, no qual certos macrófagos — células imunes que normalmente engolfam detritos — fazem algo muito mais direcionado. Em vez de engolir uma célula morta inteira, eles estendem finas protrusões em forma de dedo diretamente no núcleo da célula em morte. Imagens de células vivas mostraram a intensidade do DNA caindo dentro do núcleo da célula morta enquanto aumentava dentro do macrófago ligado, indicando extração ativa do DNA nuclear. Essa transferência dependia do esqueleto interno da célula (actina) e de moléculas de sinalização que controlam a forma celular, sugerindo que a nucleocitose é um comportamento mecânico intencional, não um vazamento passivo.
Quando antivirais ligam o alarme de DNA
Durante a pandemia de COVID‑19, drogas como a hidroxicloroquina foram amplamente testadas como antivirais, mas suas ações precisas no organismo permaneceram obscuras. Os pesquisadores descobriram que a hidroxicloroquina e vários medicamentos relacionados, ditos “anfifílicos catiónicos”, podem ativar fortemente a via cGAS–STING–interferon — mas apenas em um subconjunto de macrófagos. Essas drogas perturbam os lisossomos ao elevar seu pH e ao bloquear uma enzima chamada PPT1, que ajuda a degradar marcas lipídicas em proteínas. O efeito combinado empurra algumas células para uma forma especial de morte na qual uma proteína chamada calreticulina se acumula no núcleo. Os macrófagos então estendem preferencialmente protrusões em direção a esses núcleos ricos em calreticulina, extraem DNA via nucleocitose e desencadeiam intensa produção de interferon em poucas células — suficiente para criar um sinal antiviral local forte sem inundar todo o organismo.
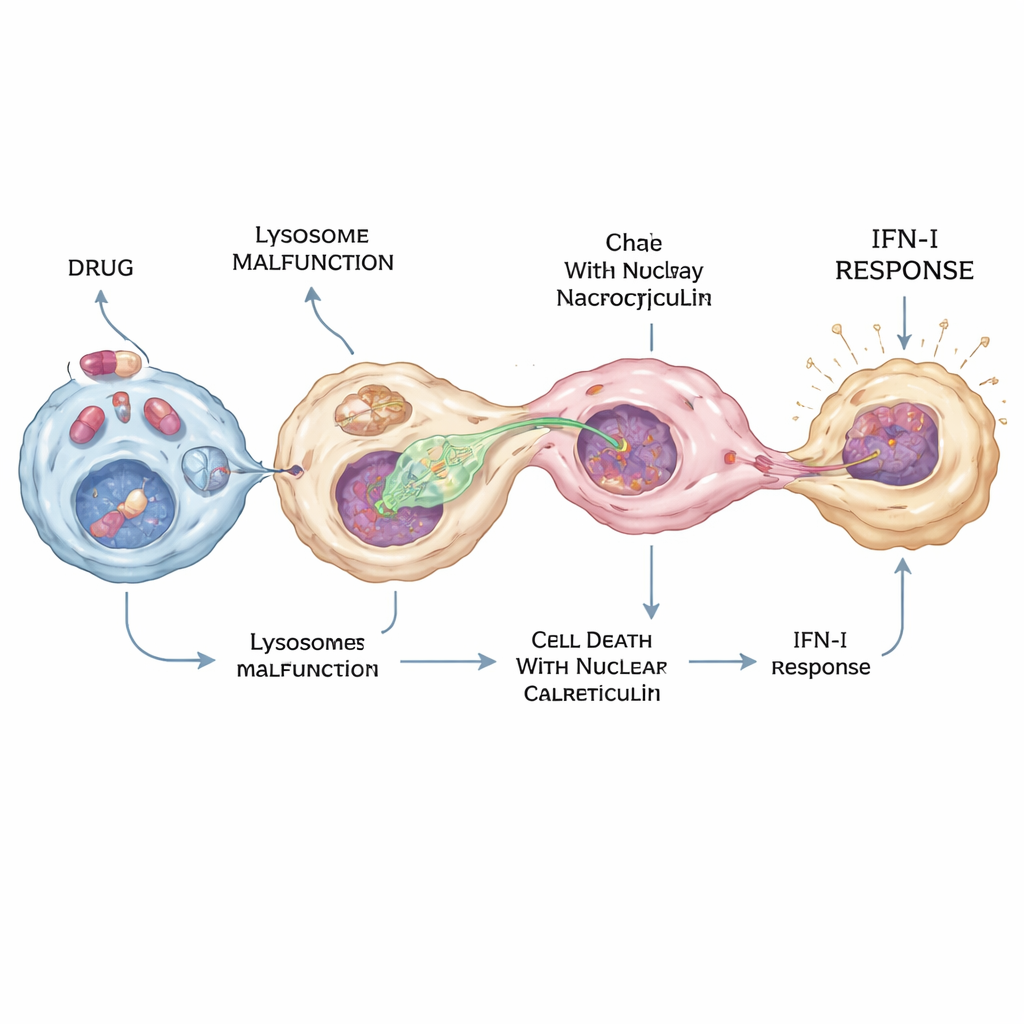
Da defesa local à doença e efeitos colaterais
Estudando tanto culturas celulares quanto pulmões de camundongos, a equipe mostrou que macrófagos tratados com droga podem provocar uma resposta de interferon dependente de STING que permanece em grande parte local — por exemplo, no pulmão — em vez de se tornar sistêmica. Isso ajuda a explicar por que drogas como a hidroxicloroquina podem apresentar benefícios antivirais ou antitumorais em alguns tecidos, mas também por que podem causar efeitos colaterais específicos de órgão, como toxicidade ocular ou cardíaca quando usadas a longo prazo. O mesmo processo de nucleocitose poderia contribuir plausivelmente para doenças autoimunes ou inflamatórias sempre que células mortas e estresse lisossomal coincidam, pois oferece uma via direta para o DNA próprio ativar o alarme cGAS.
Por que isso importa para tratamentos futuros
Para um não especialista, a mensagem principal é que células imunes não apenas comem passivamente células mortas; elas podem minerar ativamente seus núcleos em busca de DNA e usá‑lo como sinal de socorro. Essa via de nucleocitose explica como nosso próprio DNA pode ativar com segurança defesas antivirais poderosas de maneira focada e local, ao mesmo tempo em que ressalta como drogas que perturbam lisossomos ou PPT1 podem involuntariamente disparar esse mecanismo. Ao aprender a modular a nucleocitose — seja projetando antivirais e tratamentos contra o câncer mais inteligentes, seja evitando sinais indesejados de DNA próprio em doenças autoimunes — os pesquisadores esperam aproveitar esse mecanismo recém‑descoberto para terapias mais seguras e precisas.
Citação: Negishi, H., Wada, Y., Shirasaki, Y. et al. cGAS-IFN-I responses by extracting nuclear DNA from dying cells via nucleocytosis. Nat Commun 17, 1658 (2026). https://doi.org/10.1038/s41467-026-68839-w
Palavras-chave: nucleocitose, cGAS-STING, hidroxicloroquina, interferon tipo I, macrófagos