Clear Sky Science · pt
Evolução da fotocatálise redox de manganês com luz de baixa energia a partir da fotocatálise com luz visível de alta energia
Diminuindo a intensidade da luz, mantendo a química
Químicos frequentemente usam luz intensa e de alta energia — como lâmpadas azuis fortes ou ultravioleta — para impulsionar reações que constroem moléculas complexas. Mas essa luz “dura” pode desperdiçar energia, danificar partes sensíveis das moléculas e é difícil de usar em profundidade dentro de tecidos ou grandes reatores. Este estudo mostra como sais de manganês simples e baratos podem ser montados diretamente no frasco de reação para trabalhar com luz muito mais suave, no vermelho e no infravermelho próximo, mantendo ainda a química poderosa de formação de ligações que é valiosa para descoberta de fármacos e ciência de materiais.
Por que luz mais suave importa
Luz de alta energia é um pouco como usar um maçarico para acender uma vela: resolve o problema, mas pode queimar tudo ao redor. Em reações químicas, isso pode levar a reações excessivas, destruição de grupos sensíveis e controle pobre. Luz mais suave — especialmente vermelha e infravermelha próxima, que carregam menos energia — penetra mais profundamente em líquidos e até em tecidos biológicos e é geralmente mais compatível com moléculas complexas e frágeis. O desafio é que a maioria dos catalisadores acionados por luz existente é sintonizada para absorver luz de maior energia, e redesenhá‑los geralmente exige sínteses longas e complexas. Os autores propuseram reduzir o “orçamento de fótons” dessas reações sem ter que reconstruir os catalisadores do zero.
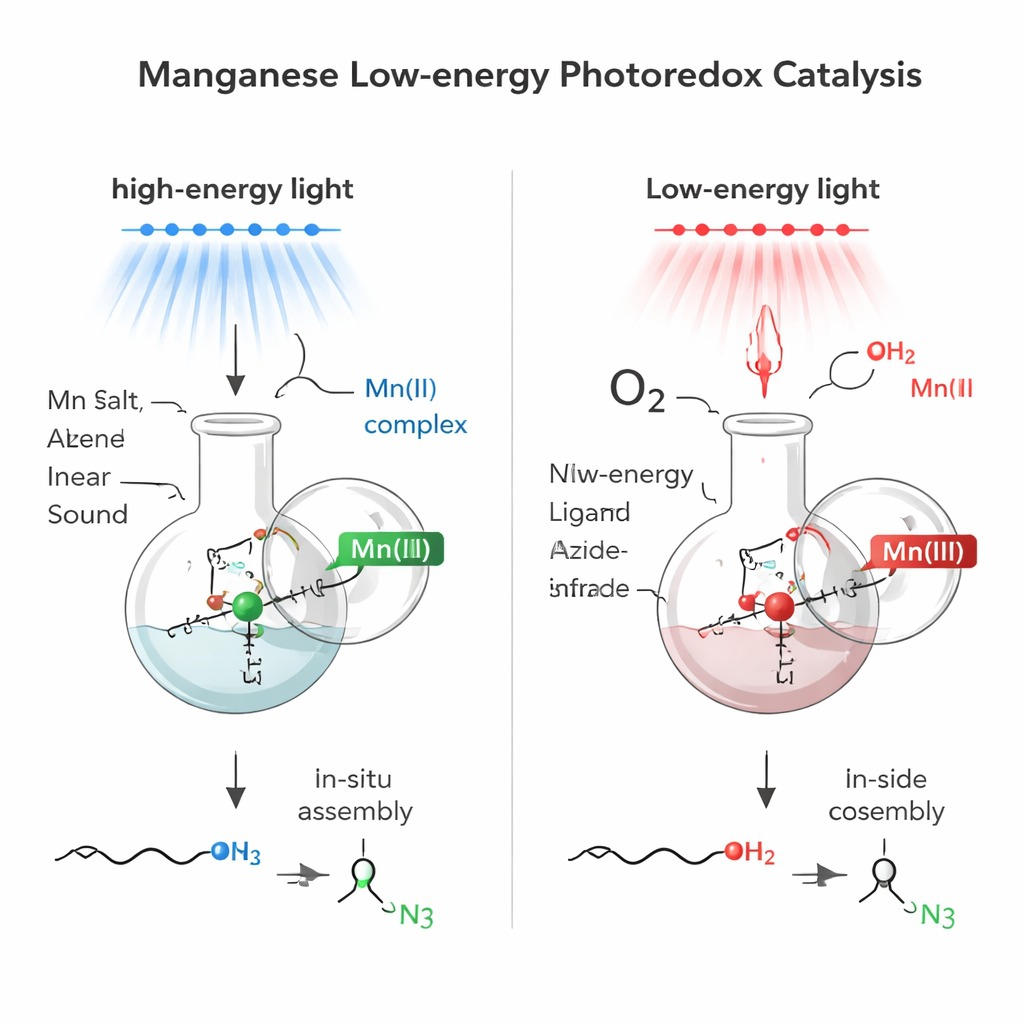
Construindo o catalisador no local
Em vez de preparar complexos metálicos elaborados antecipadamente, a equipe usou uma estratégia in situ: simplesmente misturaram sais de manganês comerciais com uma pequena molécula auxiliar (um ligante) e uma fonte de azida diretamente na mistura reacional. Essa auto‑montagem criou um sistema absorvedor de luz baseado em manganês. Com um sal de manganês(II), a mistura absorvia fortemente luz azul e podia gerar “radicais azido” de curta vida a partir de um reagente comum chamado TMSN3. Esses fragmentos reativos então se adicionavam através de ligações duplas carbono‑carbono (alcenos), colocando um grupo azida (N3) na extremidade menos substituída da dupla — um padrão conhecido como adição anti‑Markovnikov. Notavelmente, água comum serviu como fonte de hidrogênio, tornando o processo simples e eficiente em termos atômicos.
Do azul ao vermelho profundo
Os pesquisadores então perguntaram se um sistema de manganês intimamente relacionado poderia funcionar com luz de energia muito mais baixa, na região do vermelho profundo e do infravermelho próximo. Ao mudar do manganês(II) para o manganês(III) e ajustar finamente o meio reacional, eles criaram uma nova mistura que absorvia luz até cerca de 850 nanômetros — bem no infravermelho próximo. Sob essa luz suave, o complexo de manganês(III) ainda produzia radicais azido, mas agora na presença de ar (como fonte de oxigênio) e de um álcool simples, a reação instalou tanto um grupo azida quanto um grupo alcoólico através do alceno em um único passo. O resultado é um álcool 2‑azido, um bloco de construção particularmente útil porque contém duas alças altamente versáteis — N3 e OH — em átomos de carbono vizinhos.
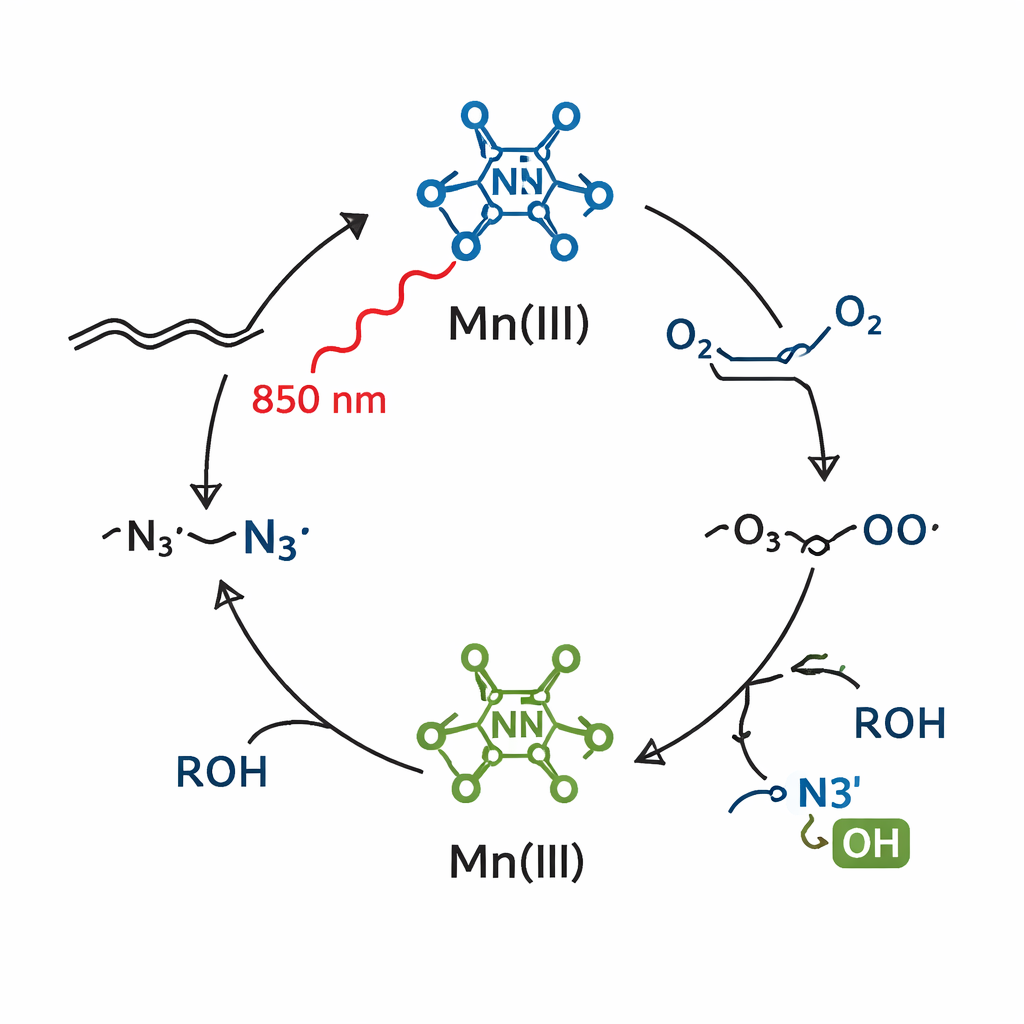
De alcenos simples a moléculas complexas com caráter farmacêutico
Com ambos os sistemas — o de luz azul e o de luz de baixa energia — em mãos, a equipe testou uma ampla variedade de alcenos. Converteram muitos materiais de partida diferentes em azidas alquila ou álcoois 2‑azido em rendimentos moderados a altos, mesmo quando as moléculas carregavam grupos que tipicamente interferem com catalisadores metálicos, como aminas não protegidas, álcoois, grupos contendo enxofre e sistemas cíclicos complexos. Também demonstraram “funcionalização em estágio tardio” modificando moléculas avançadas com caráter farmacêutico, transformando fármacos existentes em novos derivados com azida e, em alguns casos, grupos alcoólicos adicionados. Essas novas funcionalidades podem posteriormente ser transformadas em outras estruturas ricas em nitrogênio ou ligadas a alvos biológicos, ampliando a caixa de ferramentas da química medicinal.
Química que economiza energia com promessa prática
O trabalho mostra que é possível “evoluir” uma reação com luz azul de alta energia para um processo de baixa energia em infravermelho próximo simplesmente mudando como um sal metálico comum é montado em solução. Os sistemas de manganês construídos in situ evitam sínteses demoradas de catalisadores, usam um metal abundante e relativamente pouco tóxico e podem até ser acionados pela luz natural do sol. Para não especialistas, a mensagem chave é que nem sempre precisamos de luzes mais duras ou metais raros e caros para realizar química exigente. Ao projetar catalisadores que se formam a partir de peças simples e que respondem a luz mais suave, essa abordagem aponta para modos mais eficientes em energia, escaláveis e compatíveis biologicamente de fabricar as moléculas complexas das quais dependem a medicina moderna e os materiais.
Citação: Yang, W., Song, Y., Yu, X. et al. Evolution of manganese low-energy photoredox catalysis from high-energy visible light photocatalysis. Nat Commun 17, 2062 (2026). https://doi.org/10.1038/s41467-026-68837-y
Palavras-chave: catálise fotoredox, catálise com manganês, luz de baixa energia, funcionalização de alcenos, radicais azido