Clear Sky Science · pt
Priming versus propagating: distinct immune effects of alpha- versus beta-particle emitting radiopharmaceuticals when combined with immune checkpoint inhibition in mice
Transformando a radiação em aliada do sistema imune
Médicos oncologistas tentam cada vez mais recrut ar o sistema imunológico para combater tumores, mas muitos cânceres ainda ignoram ou resistem a esses fármacos. Este estudo aborda uma pergunta atual: diferentes tipos de radiação dirigida podem ser usados não apenas para reduzir tumores diretamente, mas também para treinar o sistema imune a atuar melhor — e a escolha do radiofármaco altera a forma como esse treinamento ocorre?
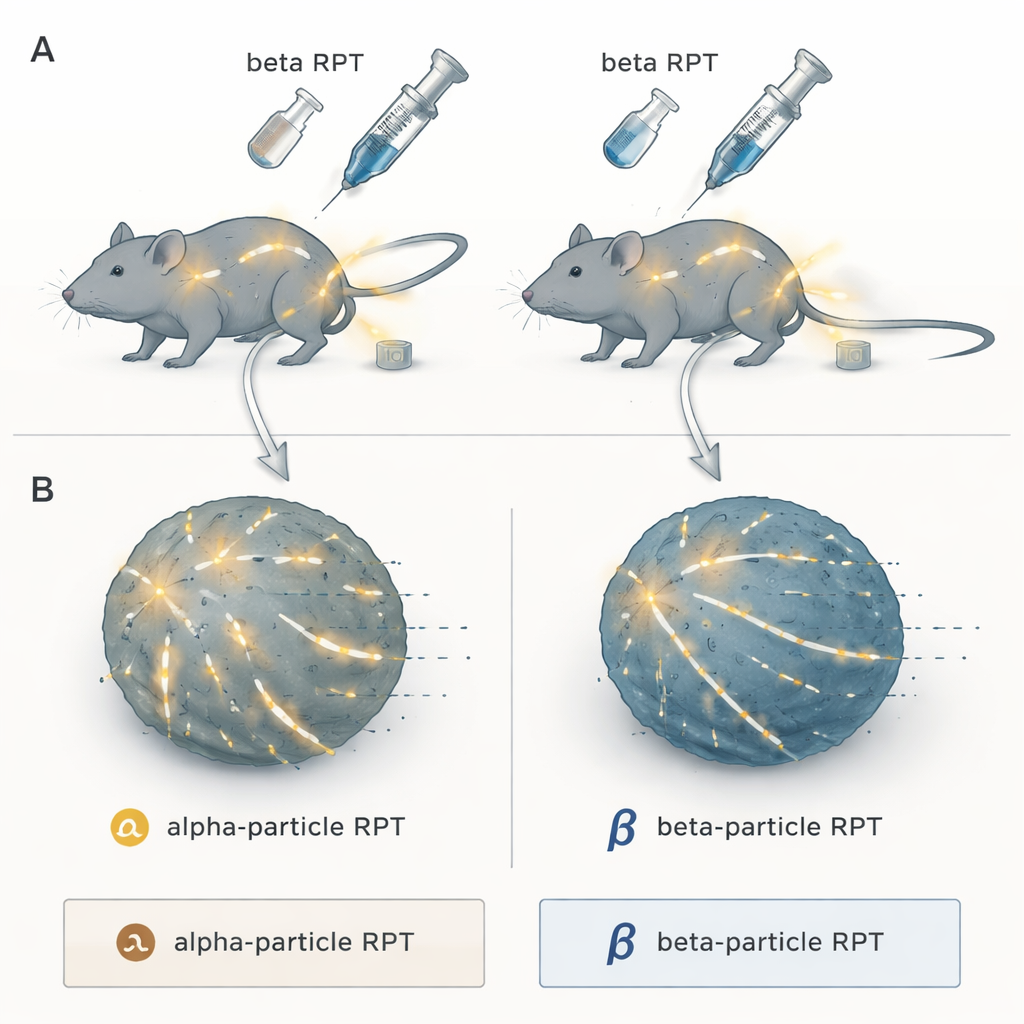
Dois tipos de radiação de precisão
Os pesquisadores concentraram‑se na terapia radiofarmacêutica, uma abordagem de “buscar e destruir” em que uma carga radioativa é ligada a uma molécula que naturalmente se direciona aos tumores. Após a injeção, ela circula pelo corpo e entrega radiação aos depósitos do câncer onde quer que estejam, algo que a radioterapia externa convencional não faz facilmente em doença disseminada. A equipe comparou duas categorias principais: emissores de partículas alfa, que liberam rajadas extremamente densas de energia em distância muito curta, e emissores de partículas beta, que produzem radiação de menor densidade que percorre maior distância no tecido. Todos foram ligados ao mesmo composto que busca tumores, o NM600, de modo que apenas o tipo de radiação — e não o direcionamento — diferiu.
Combinando radiação com bloqueadores de checkpoints imunes
Sozinhos, fármacos que bloqueiam checkpoints como anti‑PD‑L1 e anti‑CTLA4 podem liberar os freios das células imunes, mas funcionam melhor quando o tumor já é visível ao sistema imune. Em modelos murinos de melanoma, câncer de próstata e de cólon, os cientistas administraram uma dose baixa cuidadosamente escolhida de NM600 baseada em alfa ou beta, com ou sem combinação de inibidores de checkpoint. Eles também variaram quando os imunoterápicos foram dados — antes, logo após ou bem depois do tratamento radioativo — para ver como o tempo afetava desfechos como crescimento tumoral, sobrevida e memória imune a longo prazo.
Quando a radiação beta se destaca: amplificando uma resposta existente
Em um modelo de câncer de cólon “imune‑quente” que já responde à imunoterapia, os melhores resultados vieram do NM600 emissor de beta, especialmente quando os imunoterápicos foram iniciados cedo ou em tempo intermediário. Os tumores diminuíram mais, os camundongos viveram mais e os animais curados frequentemente rejeitaram o mesmo câncer quando reintroduzido meses depois. Perfis imunológicos detalhados mostraram que o tratamento à base de beta mais o bloqueio de checkpoint não criou tanto uma nova resposta, mas amplificou a que já existia: linfócitos T citotóxicos tumor‑específicos pré‑existentes expandiram‑se, tornaram‑se mais ativados e produziram mais sinais de ataque. Em resumo, emissores beta foram excelentes em propagar uma resposta imune em andamento.
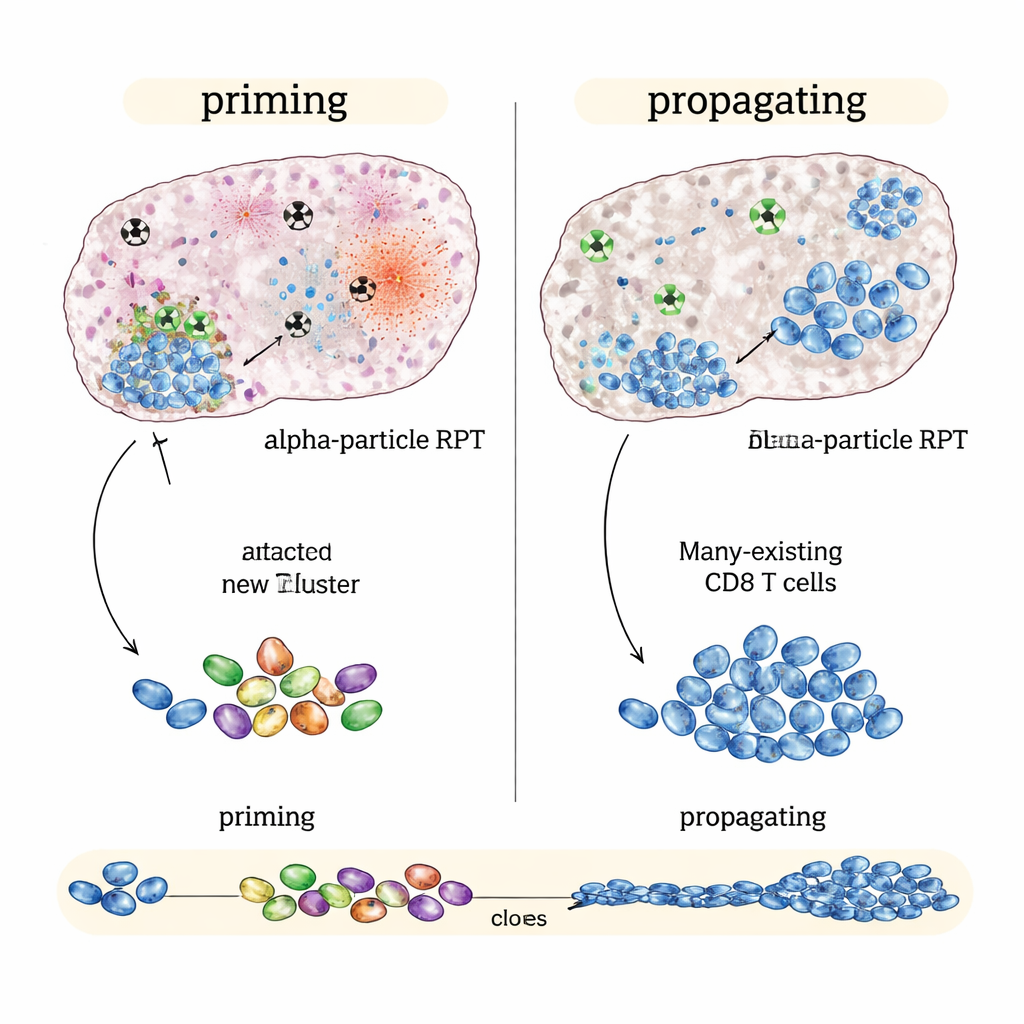
Quando a radiação alfa se destaca: desencadeando um novo ataque imune
Em contraste, em tumores “imune‑fri os” como um modelo de melanoma e um de câncer de próstata que respondem pouco aos bloqueadores de checkpoint sozinhos, a versão emissora de alfa teve desempenho melhor que os emissores de beta à mesma dose média no tumor. A terapia à base de alfa mais os imunoterápicos retardou mais o crescimento tumoral e estendeu ainda mais a sobrevida. Análises genéticas de célula única sugeriram o porquê: a radiação alfa causou dano intenso e localizado que pareceu gerar fortes sinais de alerta dentro do tumor, preservando estruturas imunes próximas. Esse padrão foi associado a respostas de células T mais amplas e diversas e a indícios de que novos linfócitos T citotóxicos reconhecedores do tumor estavam sendo formados e vinculados a células de memória de longa duração — evidência de priming imune em vez de mera amplificação.
Por que o tipo e o momento da radiação importam
Nos diversos modelos, o uso precoce ou em tempo intermediário dos inibidores de checkpoint — aproximadamente coincidindo com o pico dos sinais de perigo induzidos pela radiação — apresentou desempenho consistentemente superior ao tratamento tardio. O trabalho sugere uma regra prática: em cânceres já visíveis ao sistema imune, radiofármacos de baixa dose à base de beta podem ser parceiros ideais para inibidores de checkpoint porque propagam e fortalecem a imunidade existente. Em tumores mais resistentes ao sistema imune, emissores alfa de alto impacto podem ser mais indicados para primar novas respostas de células T e transformar um tumor “frio” em “quente”. Para pacientes, isso significa que nem todos os radiofármacos são intercambiáveis; combinar o isótopo e o cronograma com a personalidade imune do tumor pode tornar a radio‑imunoterapia combinada mais eficaz e mais duradoura.
Citação: Kerr, C.P., Jin, W.J., Liu, P. et al. Priming versus propagating: distinct immune effects of alpha- versus beta-particle emitting radiopharmaceuticals when combined with immune checkpoint inhibition in mice. Nat Commun 17, 2044 (2026). https://doi.org/10.1038/s41467-026-68834-1
Palavras-chave: terapia radiofarmacêutica, alfa vs beta radiação, inibidores de pontos de checagem imunológica, imunoterapia do câncer, microambiente tumoral