Clear Sky Science · pt
Segurança e atividade biológica de um receptor de células T bispecífico direcionado ao Gag do HIV em homens vivendo com HIV: um ensaio em humanos pela primeira vez
Por que este novo estudo sobre HIV é importante
Pessoas vivendo com HIV hoje podem esperar uma expectativa de vida quase normal graças aos coquetéis modernos de medicamentos. Mas esses medicamentos, chamados terapia antirretroviral (TAR), não removem o vírus; apenas o mantêm sob controle. Bolsões ocultos de HIV permanecem no corpo e podem reiniciar a infecção se o tratamento for interrompido. Este estudo testa um novo tipo de terapia imune de precisão — construída a partir de um receptor de células T sintético — que visa treinar o sistema imunológico para localizar esses esconderijos com segurança em pessoas que já estão bem controladas na TAR.
O vírus escondido que não desaparece
Mesmo quando exames de sangue mostram vírus “indetectável”, o HIV permanece como material genético alojado dentro de células de longa vida, principalmente um tipo de glóbulo branco chamado células T CD4. Essas células de reservatório carregam vírus silencioso, porém intacto, que pode despertar novamente, obrigando as pessoas a tomar comprimidos diários pelo resto da vida. Apagar completamente cada célula infectada é extremamente desafiador e só foi alcançado em poucas pessoas que passaram por transplantes de medula óssea arriscados para tratar câncer. Muitos pesquisadores, em vez disso, miram em uma “cura funcional”: reduzir o reservatório o suficiente para que as defesas do próprio corpo consigam manter o HIV sob controle sem medicação constante.
Uma molécula projetada para redirecionar células T
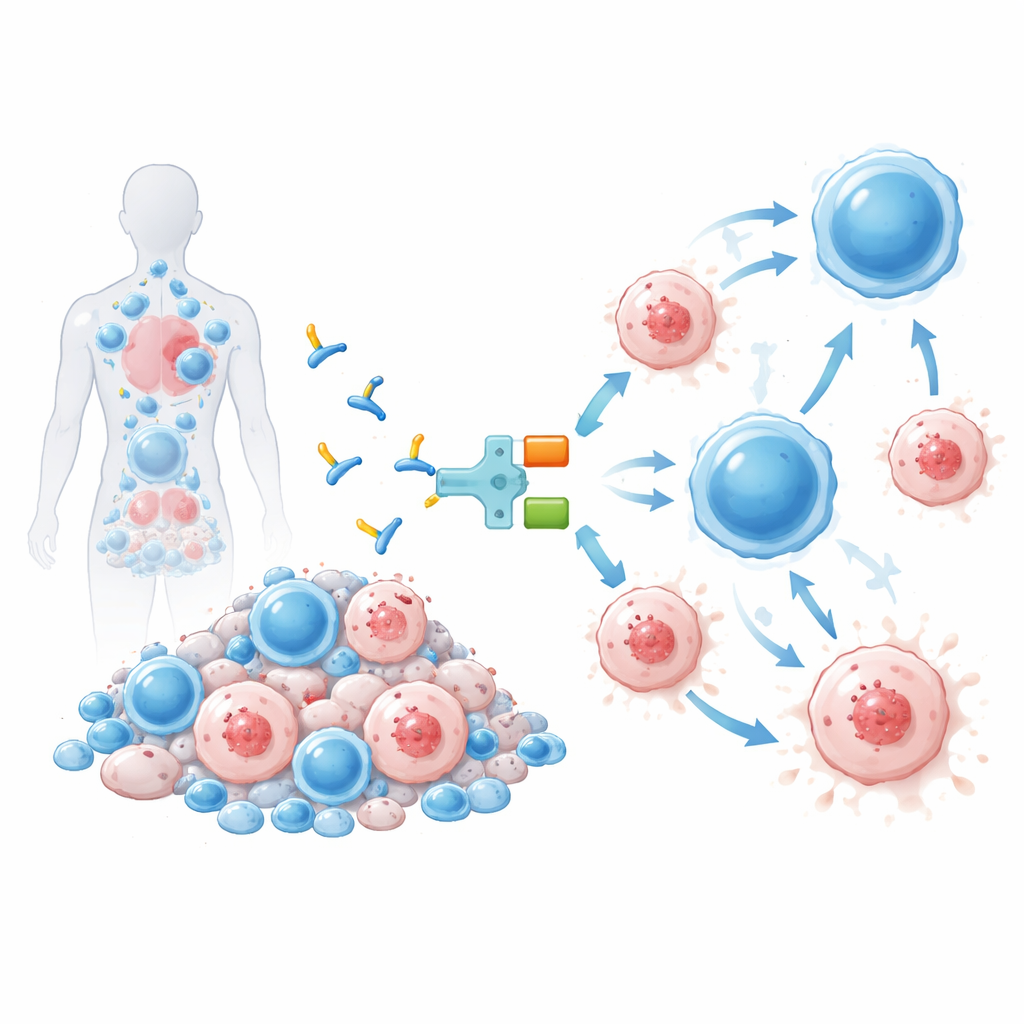
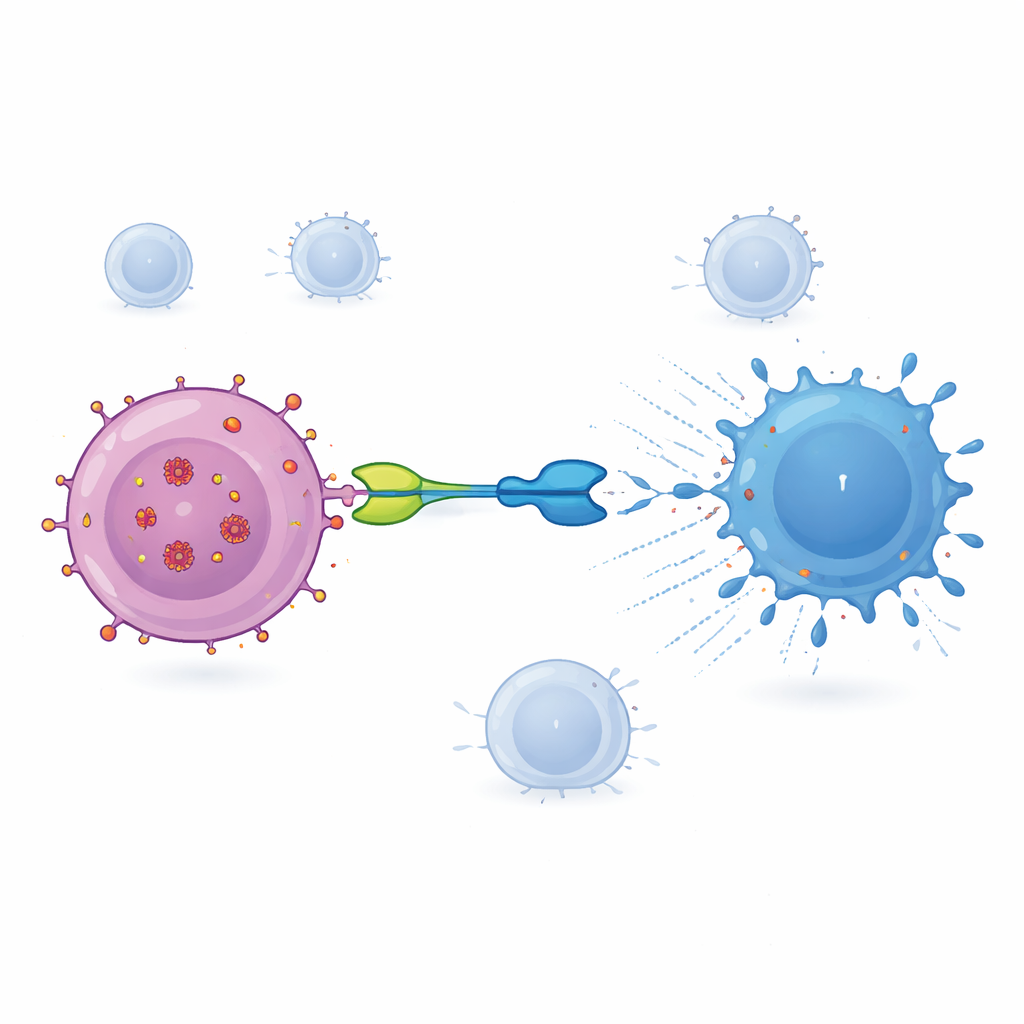
A terapia testada aqui, chamada IMC‑M113V, é uma pequena proteína que funciona como um adaptador molecular entre células infectadas e o sistema imunológico. Uma extremidade do IMC‑M113V é um receptor de células T engenheirado que reconhece um pequeno fragmento do HIV proveniente da proteína Gag exibido na superfície de células infectadas no contexto de um marcador imune comum (HLA‑A*02:01). A outra extremidade liga‑se ao CD3, uma estrutura presente em todas as células T. Quando o IMC‑M113V se liga aos dois lados ao mesmo tempo, ele aproxima células T comuns de uma célula infectada pelo HIV e as ativa para matá‑la. Em testes de laboratório, essa molécula mostrou-se extremamente sensível, detectando apenas algumas cópias do fragmento viral na superfície de uma célula e eliminando efetivamente células infectadas por várias variantes comuns do HIV, enquanto não apresentou ativação significativa contra um painel de células humanas saudáveis.
Primeiro teste em pessoas vivendo com HIV
Para avaliar se essa abordagem é segura em humanos, os pesquisadores conduziram um ensaio em fase inicial com doze homens adultos vivendo com HIV no Reino Unido, Bélgica e Espanha. Todos os participantes apresentavam infecção bem controlada com TAR, contagens de CD4 elevadas e possuíam o tipo de HLA requerido. Cada pessoa recebeu uma dose intravenosa única de IMC‑M113V em um de três níveis de dose baixos e foi então monitorada de perto por um mês. O foco principal nesta fase foi a segurança: procurar efeitos colaterais como febre, inflamação severa ou problemas neurológicos, que podem ocorrer com outros medicamentos potentes que engajam células T usados no tratamento do câncer.
O que os pesquisadores observaram na clínica
Em todas as doses, o IMC‑M113V foi geralmente bem tolerado. Metade dos participantes relatou alguns efeitos colaterais, em sua maioria sintomas leves como fadiga ou irritação da pele, e ninguém desenvolveu problemas graves como síndrome de liberação de citocinas ou neurotoxicidade. Exames de sangue mostraram que os níveis do medicamento subiram e caíram dentro de cerca de um dia, com uma meia‑vida de aproximadamente 15–22 horas. Na dose mais alta (15 microgramas), vários participantes exibiram aumentos temporários em moléculas inflamatórias, especialmente interleucina‑6, e sinais de que suas células T haviam sido ativadas e se tornado mais capazes de produzir proteínas citotóxicas. Essas alterações imunes foram mais fortes em voluntários cujos vírus carregavam variantes de Gag às quais o IMC‑M113V se liga particularmente bem, sugerindo que o medicamento estava de fato engajando seus alvos pretendidos no organismo. No entanto, após uma dose única, não houve redução mensurável no tamanho do reservatório de HIV no sangue, conforme avaliado por RNA viral e DNA viral intacto dentro das células CD4.
O que isso significa para o tratamento futuro do HIV
Para um leitor não especialista, a mensagem principal é que este estudo fornece uma importante prova de conceito inicial: uma molécula imune altamente direcionada que funciona como uma “ponte” pode ser administrada com segurança a pessoas com HIV bem controlado e pode despertar suas células T para reconhecer células que abrigam o vírus. Não curou o HIV nem permitiu que as pessoas interrompessem a TAR, mas esse não era o objetivo deste ensaio inédito em humanos. Os achados apoiam testar doses mais altas e repetidas, possivelmente combinadas com medicamentos que induzam mais células infectadas a se revelarem, e expandir a abordagem para cobrir outros tipos imunes além do HLA‑A*02:01. Se estudos futuros confirmarem que essa estratégia pode reduzir de forma confiável os reservatórios virais sem efeitos colaterais perigosos, ela poderá se tornar parte central de tratamentos combinados voltados ao controle a longo prazo do HIV sem necessidade de medicamentos.
Citação: Vandekerckhove, L., Fox, J., Mora-Peris, B. et al. Safety and biologic activity of a bispecific T cell receptor targeting HIV Gag in males living with HIV: a first-in-human trial. Nat Commun 17, 2207 (2026). https://doi.org/10.1038/s41467-026-68833-2
Palavras-chave: cura do HIV, terapia com células T, reservatório viral, receptor bispecífico, ensaio clínico