Clear Sky Science · pt
Percepções mecanicistas sobre o desdobramento dirigido por PCBP1 de i-motif DNA selecionados no ponto de verificação G1/S
Dobrações de DNA que Funcionam como Semáforos
Dentro de nossas células, o código genético é mais do que uma simples escada reta de DNA. Trechos dele podem se dobrar em formas incomuns que atuam como pequenos interruptores, ajudando a controlar quando as células copiam seu DNA e se dividem. Este estudo foca em uma dessas formas, chamada i-motif, e em uma proteína denominada PCBP1 que pode reconhecer e desdobrar essas estruturas justamente quando a célula se prepara para replicar seu DNA. Compreender essa interação esclarece como as células mantêm a estabilidade do genoma e o que pode dar errado no câncer.
Nós Estranhos de DNA em Regiões Ligadas ao Câncer
A maioria das pessoas aprende que o DNA forma a famosa hélice dupla, mas certos trechos ricos na letra C (citosina) podem se dobrar em um nó de quatro fitas conhecido como i-motif. Essas estruturas tendem a aparecer em regiões de controle de genes que promovem o crescimento celular, como cMYC e BCL2. Durante anos, os cientistas debateram se os i-motifs realmente se formam em células vivas, porque são mais fáceis de observar em condições ácidas em tubo de ensaio do que nas condições quase neutras do interior do corpo. Usando anticorpos especializados que reconhecem i-motifs, trabalhos recentes, incluindo o presente estudo, confirmaram que eles aparecem nos núcleos celulares—e frequentemente se agrupam próximos a genes chave de crescimento e câncer.
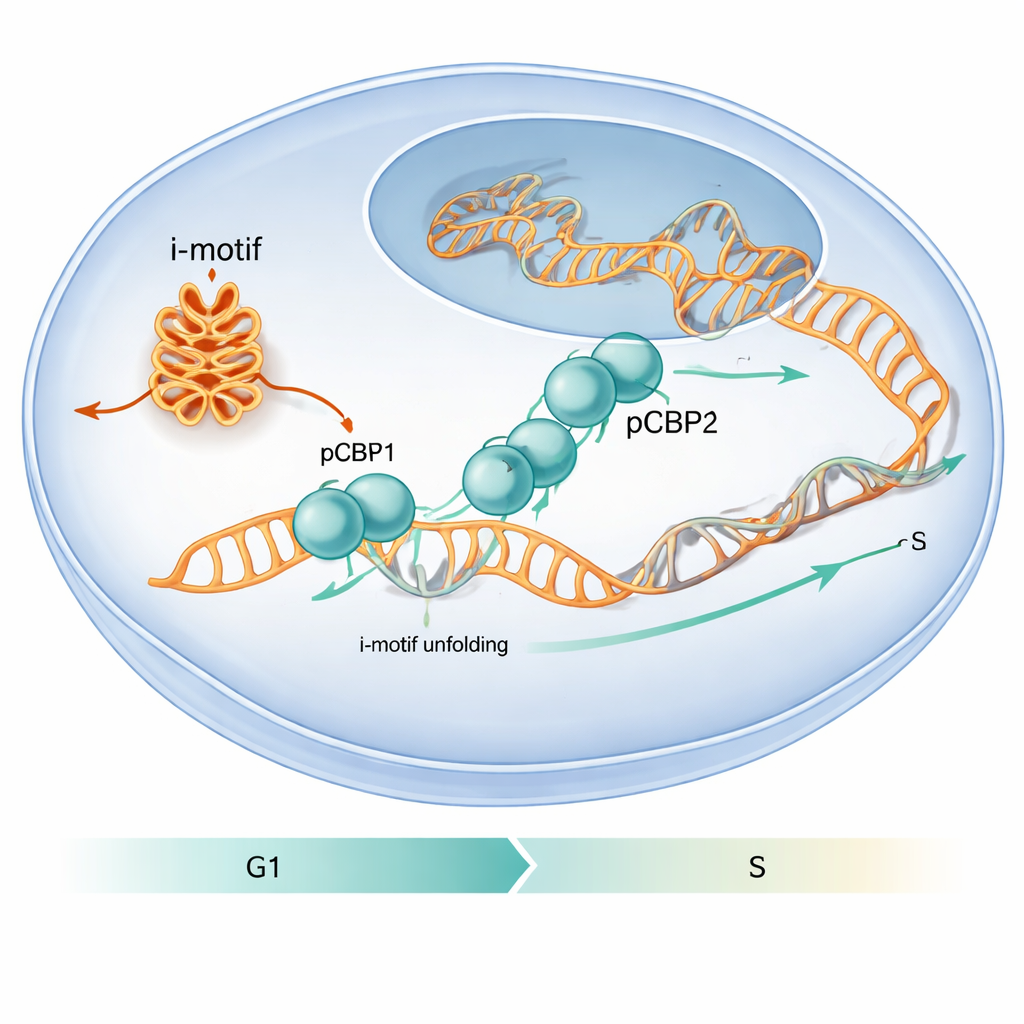
Uma Proteína que Identifica Dobrações de DNA Especiais
Os autores buscaram descobrir como proteínas na célula lidam com essas dobras incomuns de DNA. Eles se concentraram na PCBP1, uma proteína já conhecida por se ligar a trechos ricos em C do DNA e do RNA e por influenciar o ciclo celular. Ao analisar mapas de ligação genômica existentes e realizar experimentos direcionados, descobriram que PCBP1 frequentemente se assenta em regiões ricas em C que podem formar i-motifs, especialmente ao redor de locais de início de genes. Em experimentos celulares usando linhagens humanas de câncer, regiões dos promotores de cMYC, BCL2 e da sequência ligada à insulina ILPR mostraram sinais fortes tanto de i-motif quanto de ocupação por PCBP1, sugerindo que PCBP1 é um guardião dedicado dessas estruturas.
Como PCBP1 Agarra e Desfaz o Nó
Em ensaios de tubo de ensaio, os pesquisadores compararam quão bem PCBP1 se liga a i-motifs dobrados versus a mesma sequência de DNA em forma desdobrada. Ajustaram a acidez para que o DNA permanecesse dobrado ou relaxado, mantendo a proteína estável. PCBP1 sempre preferiu o i-motif dobrado, ligando-se a ele aproximadamente duas vezes mais fortemente do que à mesma sequência quando desdobrada, e apenas fracamente a formas de DNA não relacionadas. Uma vez ligado, PCBP1 pôde promover ativamente o desdobramento, permitindo que a fita do i-motif se emparelhasse com sua parceira complementar. No entanto, nem todos os i-motifs se comportaram da mesma forma: alguns, como a estrutura no promotor de cMYC, foram desdobrados rapidamente, enquanto outros, como os de BCL2, resistiram e se desdobraram apenas lentamente. Características adicionais, como laços em forma de hairpin no DNA e o grau de protonação das citosinas (carregando carga positiva extra) podiam tanto ajudar quanto dificultar a atividade de desenrolamento da PCBP1.
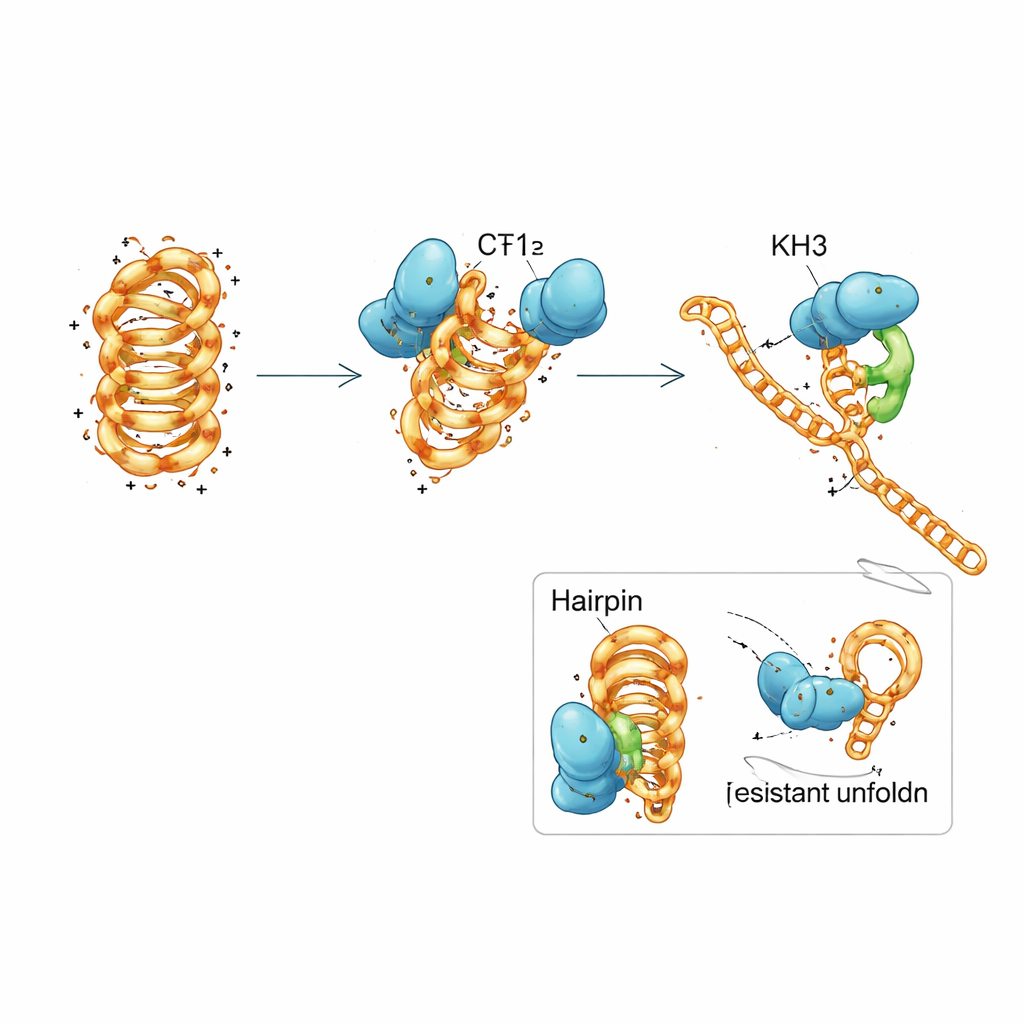
Um Esforço em Equipe Dentro de Uma Única Proteína
A PCBP1 é composta por três módulos repetidos chamados domínios KH, motivos comuns que agarram curtos trechos de ácidos nucleicos. A equipe dissecou a PCBP1 em pedaços e descobriu que nenhum domínio KH isolado podia reproduzir totalmente o comportamento da proteína inteira. Os dois primeiros domínios juntos podiam prender tanto o DNA dobrado quanto o desdobrado e empurrar o i-motif em direção a uma forma menos estável, mas promoviam o desdobramento completo apenas lentamente. O terceiro domínio, isoladamente, quase não se ligava. Quando os três domínios estavam presentes e podiam trabalhar em conjunto, a proteína recuperou sua forte preferência pelos i-motifs dobrados e sua capacidade eficiente de desdobrá-los. Medições biofísicas detalhadas e simulações computacionais sugeriram um mecanismo em etapas: KH1 e KH2 inicialmente se encaixam em regiões flexíveis de laço do i-motif e quebram parcialmente pares de bases selecionados, o que então permite que KH3 se envolva e conduza a estrutura a um estado aberto, pronto para replicação.
Manter o Ciclo Celular no Ritmo
O trabalho também mostra que essa dança molecular importa para o comportamento celular. Quando os pesquisadores reduziram os níveis de PCBP1 em células humanas, mais estruturas de i-motif apareceram em promotores de genes específicos, marcadores de dano ao DNA aumentaram e as células pararam no ponto crítico G1/S—o momento logo antes do início da replicação do DNA. Em condições normais, a presença de PCBP1 nas regiões formadoras de i-motif atinge pico ao redor desse ponto de verificação, diminuindo depois que a fase S começa e os i-motifs são resolvidos. Esse timing sugere que PCBP1 atua como um zelador: liga-se e desdobra i-motifs particulares no momento certo para que a replicação do DNA possa prosseguir sem problemas e o genoma permaneça intacto. Para um leitor leigo, a mensagem é que dobras incomuns do DNA podem funcionar como bloqueios temporários, e a PCBP1 é uma das ferramentas especializadas que a célula usa para removê-los, ajudando a prevenir erros que, de outra forma, poderiam contribuir para o câncer.
Citação: Sengupta, P., Gillet, N., Obi, I. et al. Mechanistic insights into PCBP1-driven unfolding of selected i-motif DNA at G1/S checkpoint. Nat Commun 17, 1149 (2026). https://doi.org/10.1038/s41467-026-68822-5
Palavras-chave: DNA i-motif, proteína PCBP1, ponto de verificação do ciclo celular, estabilidade do genoma, estrutura secundária do DNA