Clear Sky Science · pt
Transcritômica de célula única guiada quimicamente revela remodelamento do esqueleto mediado por sulfotransferase na biossíntese de securinina
Por que a química de um arbusto importa
Alcaloides securinígenos são moléculas potentes encontradas em um pequeno arbusto ornamental, Flueggea suffruticosa, estudado há muito tempo por seu potencial no tratamento de câncer e doenças neurológicas. Ainda assim, até agora, ninguém sabia realmente como essa planta sintetiza essas estruturas intrincadas. Este estudo combina leituras gênicas de célula única modernas com experimentos químicos engenhosos para revelar, passo a passo, como a planta monta e remodela essas moléculas — e descobre um papel surpreendente para um tipo comum de enzima ao longo do caminho. 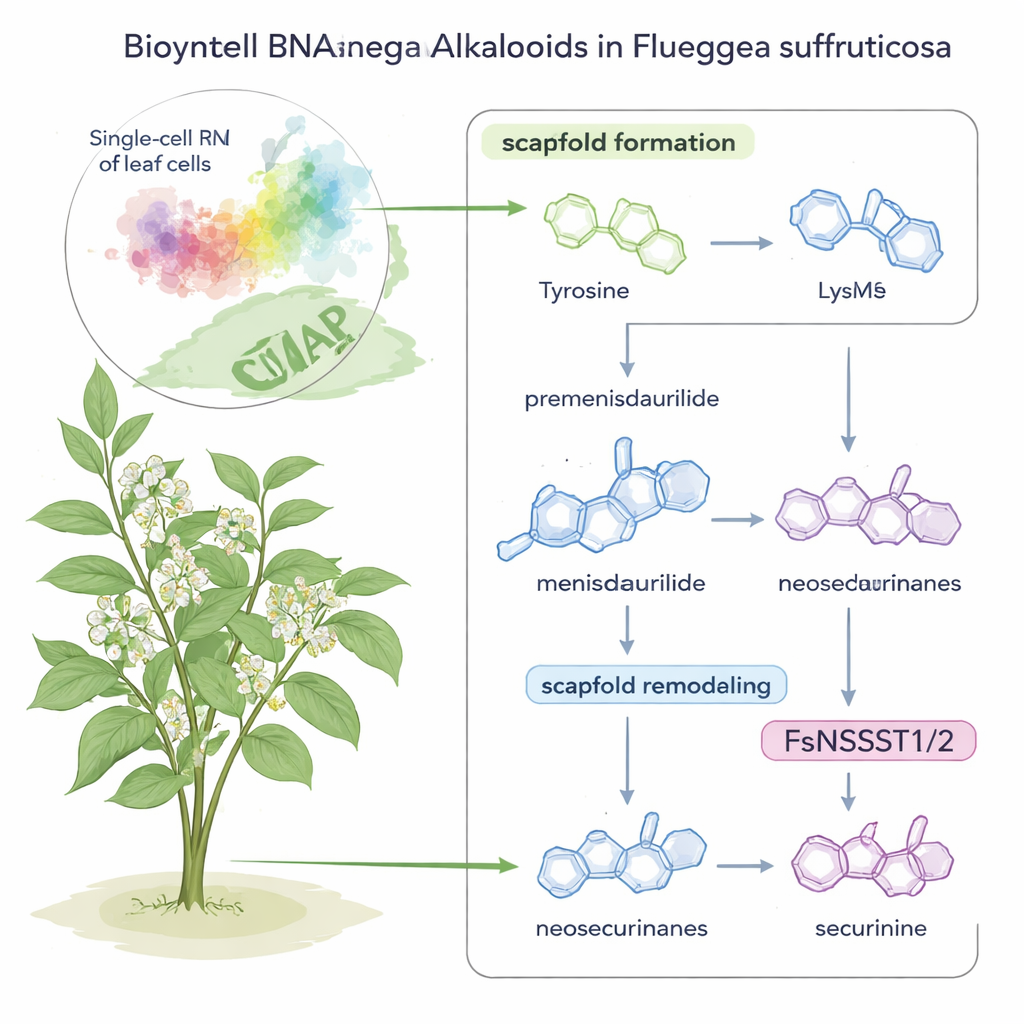
Tijolos de construção a partir de aminoácidos cotidianos
A história começa com dois nutrientes familiares: os aminoácidos tirosina e lisina. Em F. suffruticosa, a tirosina é transformada em uma molécula incomum em forma de anel chamada premenisdaurilida, que é então reduzida a menisdaurilida por uma enzima recém-descoberta que os autores denominaram FsMS (de “menisdaurilide synthase”). Em paralelo, a lisina é convertida em um pequeno anel contendo nitrogênio chamado 1-piperideína por outra enzima, FsPS, descoberta em trabalhos anteriores. Quando menisdaurilida e 1-piperideína se encontram em condições levemente básicas, aquosas, elas se fundem espontaneamente para formar alcaloides “neosecurinana” — estruturas intermediárias no caminho para os compostos medicinais finais.
Assistindo à química acontecer em tempo real
Para provar que essas etapas propostas não são apenas teóricas, a equipe sintetizou versões dos intermediários suspeitos marcadas com átomos de carbono pesados. Alimentar esses compostos rotulados a extratos da planta permitiu aos cientistas rastrear exatamente onde os átomos foram incorporados. Eles observaram menisdaurilida rotulada convertida em neosecurinanas rotuladas, e estas nas já conhecidas alarcoes allosecurinina e securinina, confirmando que esses intermediários realmente fazem parte da via natural. Importante, algumas das reações chave de formação de anel ocorreram mesmo em extratos fervidos, mostrando que partes da rota podem proceder sem enzimas, impulsionadas simplesmente pela química intrínseca das moléculas.
Dando zoom nas células certas
Saber que moléculas aparecem onde aparece é apenas metade do quebra-cabeça; identificar os genes que controlam cada etapa exige saber quais células estão realizando o trabalho. Os pesquisadores sequenciaram RNA de milhares de células individuais retiradas de folhas de F. suffruticosa, agrupando-as em tipos celulares distintos com base em padrões de atividade gênica. Um grupo, associado aos vasos da folha, destacou-se: expressou fortemente os genes conhecidos da via e muitas enzimas ligadas ao metabolismo da tirosina, lisina e enxofre. Ao examinar quais genes variavam em sincronia com as enzimas da via dentro desse grupo, a equipe localizou FsMS e duas sulfotransferases, FsNSST1 e FsNSST2, como candidatas principais para as etapas faltantes. 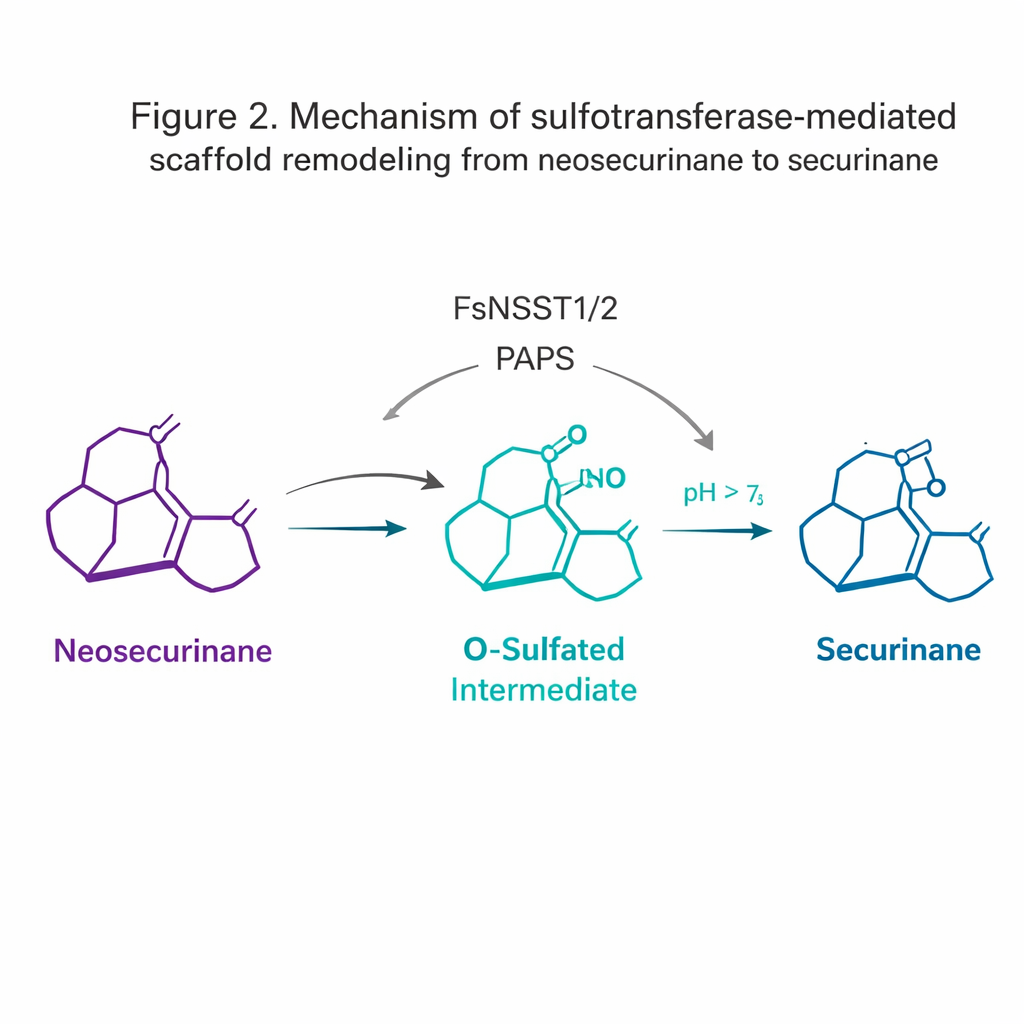
Uma enzima que remodela o esqueleto molecular
A descoberta mais surpreendente veio das sulfotransferases. Normalmente, sulfotransferases adicionam um grupo sulfato às moléculas para melhorar sua solubilidade ou marcá-las para degradação. Aqui, FsNSST1 e FsNSST2 atuam em vez disso como gatilhos: elas ligam um sulfato ao esqueleto neosecurinana, transformando-o temporariamente em um intermediário “O-sulfatado” de alta energia. Essa forma ativada então sofre uma migração espontânea 1,2-amina — um pequeno rearranjo em que um átomo de nitrogênio se desloca — convertendo a estrutura bicicíclica [2.2.2] “neosecurinana” no arcabouço [3.2.1] “securinana”. Esse passo sutil de remodelamento é o que gera o núcleo tetracíclico distinto dos alcaloides biologicamente ativos.
Por que essa via importa
Para um não-especialista, a mensagem principal é que a planta sintetiza os alcaloides securinígenos em duas fases principais: primeiro, constrói um sistema preliminar de anéis a partir de aminoácidos comuns; depois, remodela quimicamente esse esqueleto em uma forma mais complexa usando um “gatilho” sulfato. Ao combinar perfilagem gênica célula a célula com química isotópica marcada, os autores mapeiam essa rota em detalhe e revelam que sulfotransferases — enzimas encontradas em todas as formas de vida — podem fazer mais do que apenas decorar moléculas; elas podem iniciar rearranjos completos da sua forma. Compreender essa via não só esclarece como uma classe promissora de moléculas semelhantes a fármacos é produzida na natureza, mas também abre a porta para engenharia de plantas ou microrganismos para produzir novos medicamentos inspirados nas securininas.
Citação: Choung, S., Kang, G., Kim, T. et al. Chemically guided single-cell transcriptomics reveals sulfotransferase-mediated scaffold remodeling in securinine biosynthesis. Nat Commun 17, 1954 (2026). https://doi.org/10.1038/s41467-026-68816-3
Palavras-chave: alcaloides vegetais, biossíntese, transcritômica de célula única, sulfotransferase, química de produtos naturais