Clear Sky Science · pt
O panorama funcional do splicing alternativo no comprometimento da linhagem hematopoiética
Como pequenas edições nos genes moldam o nosso sangue
Cada segundo, seu corpo produz milhões de novas células sanguíneas. Por trás desse milagre silencioso existe um sistema molecular de edição que pode recortar e colar trechos das mensagens genéticas de maneiras diferentes, gerando versões levemente distintas da mesma proteína. Este estudo investiga como esse processo de edição, chamado splicing alternativo, ajuda a orientar células-tronco imaturas para se tornarem eritrócitos, leucócitos ou outros tipos de células sanguíneas — e o que acontece quando um único trecho editado está ausente.
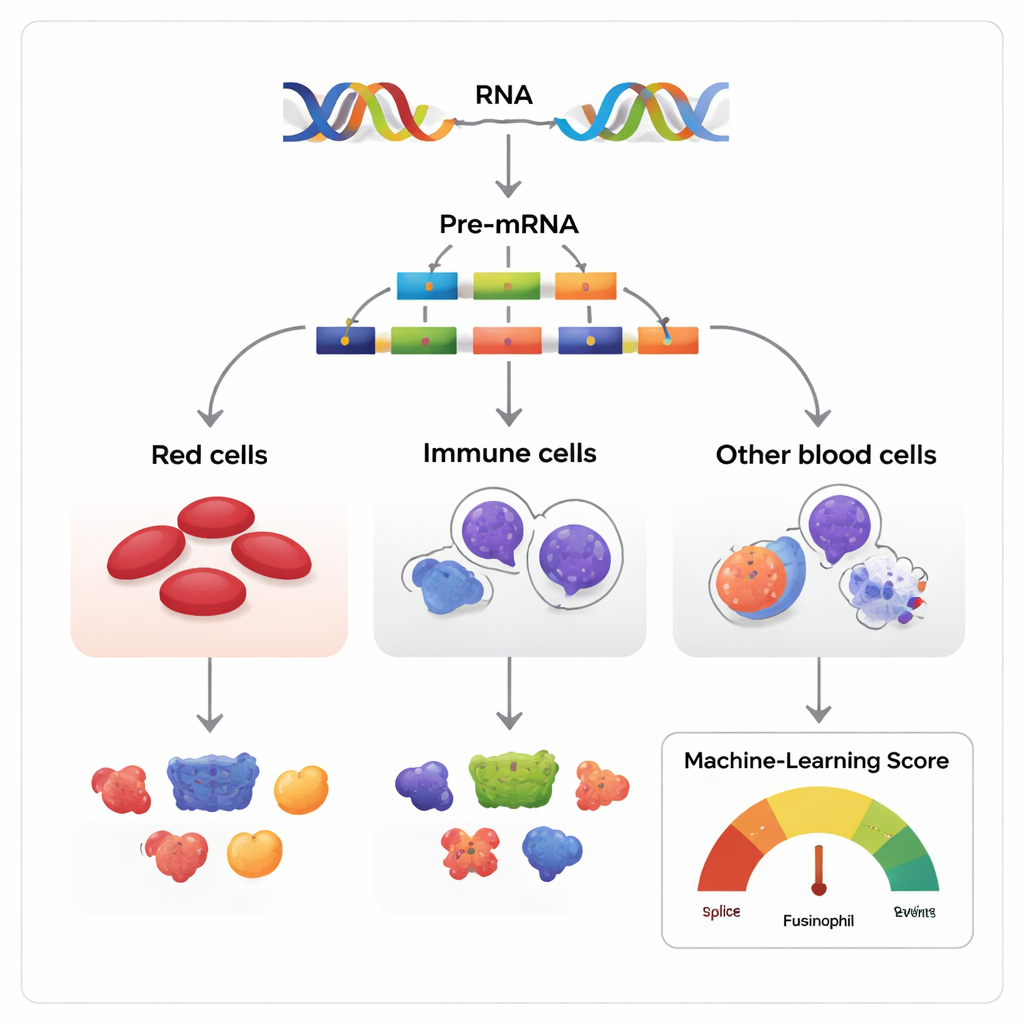
Muitas versões a partir do mesmo roteiro genético
Genes costumam ser descritos como plantas, mas na prática são mais parecidos com roteiros que podem ser reorganizados. Quando um gene é lido, a cópia inicial de RNA contém segmentos chamados éxons que podem ser mantidos ou pulados antes que a mensagem final seja transformada em proteína. Os autores investigaram esse processo, conhecido como skipping de éxons, nos tecidos formadores de sangue de humanos, camundongos e vários outros vertebrados. Eles reuniram mais de 270 conjuntos de dados de RNA que, em conjunto, acompanham células-tronco e progenitoras hematopoiéticas enquanto amadurecem em três famílias principais: células eritroides produtoras de glóbulos vermelhos, células mieloides combatentes de infecção e células linfoides produtoras de anticorpos.
Classificando quais mudanças no splicing realmente importam
Como a maioria dos genes com múltiplos éxons pode ser empalmada de várias maneiras, o desafio central é distinguir variações inofensivas daquelas que realmente influenciam o destino celular. Os pesquisadores construíram um modelo de aprendizado de máquina, chamado Functional AS Score (FAScore), para enfrentar esse problema. Para cada evento de skipping de éxon, o modelo considera 19 informações, como o quanto seu uso muda durante o desenvolvimento celular, quão conservada é a sequência ao redor entre espécies, se altera domínios proteicos conhecidos e se contém sítios para modificações químicas da proteína. O algoritmo, treinado usando uma estratégia positive–unlabeled e um classificador random forest, gera uma pontuação entre 0 e 1 indicando a probabilidade de um dado evento de splicing ter impacto funcional.
Encontrando chaves conservadas e específicas de linhagem
Aplicando o FAScore a dezenas de milhares de eventos de skipping de éxons, a equipe os classificou em grupos prováveis funcionais, não funcionais ou incertos. Eventos previstos como funcionais foram mais frequentemente encontrados em regiões proteicas importantes para interações, em sequências conservadas evolutivamente e em segmentos que hospedam marcas químicas como fosforilação ou SUMOilação. Muitos desses eventos também foram ativos apenas em linhagens sanguíneas específicas ou durante a hematopoiese fetal, sugerindo que atuam como interruptores afinados em janelas de desenvolvimento particulares. O estudo mostrou ainda que alguns dos eventos de splicing mais antigos — aqueles compartilhados entre vertebrados ao longo de centenas de milhões de anos — são especialmente propensos a ser funcionais, espelhando como genes mais antigos tendem a carregar funções biológicas centrais.
Prova experimental: ajustando resultados de células sanguíneas
Para testar as previsões do modelo, os autores escolheram vários éxons com alta pontuação em genes ativos em diferentes linhagens sanguíneas e deletaram esses éxons em células-tronco e progenitoras sanguíneas de camundongo usando CRISPR. Os resultados corresponderam às expectativas do modelo: remover certos éxons nos genes KLF6 e SSBP3 prejudicou a formação de colônias mieloides sem afetar a produção de eritrócitos, enquanto deletar éxons em EPB41L1 e TBC1D23 alterou a formação de colônias eritroides. Em particular, pular o éxon 15 de TBC1D23 reduziu a produção de precursores de glóbulos vermelhos em camundongos e zebrafish, levando a menos glóbulos vermelhos circulantes e níveis mais baixos de hemoglobina, ao mesmo tempo em que poupou em grande parte os leucócitos.
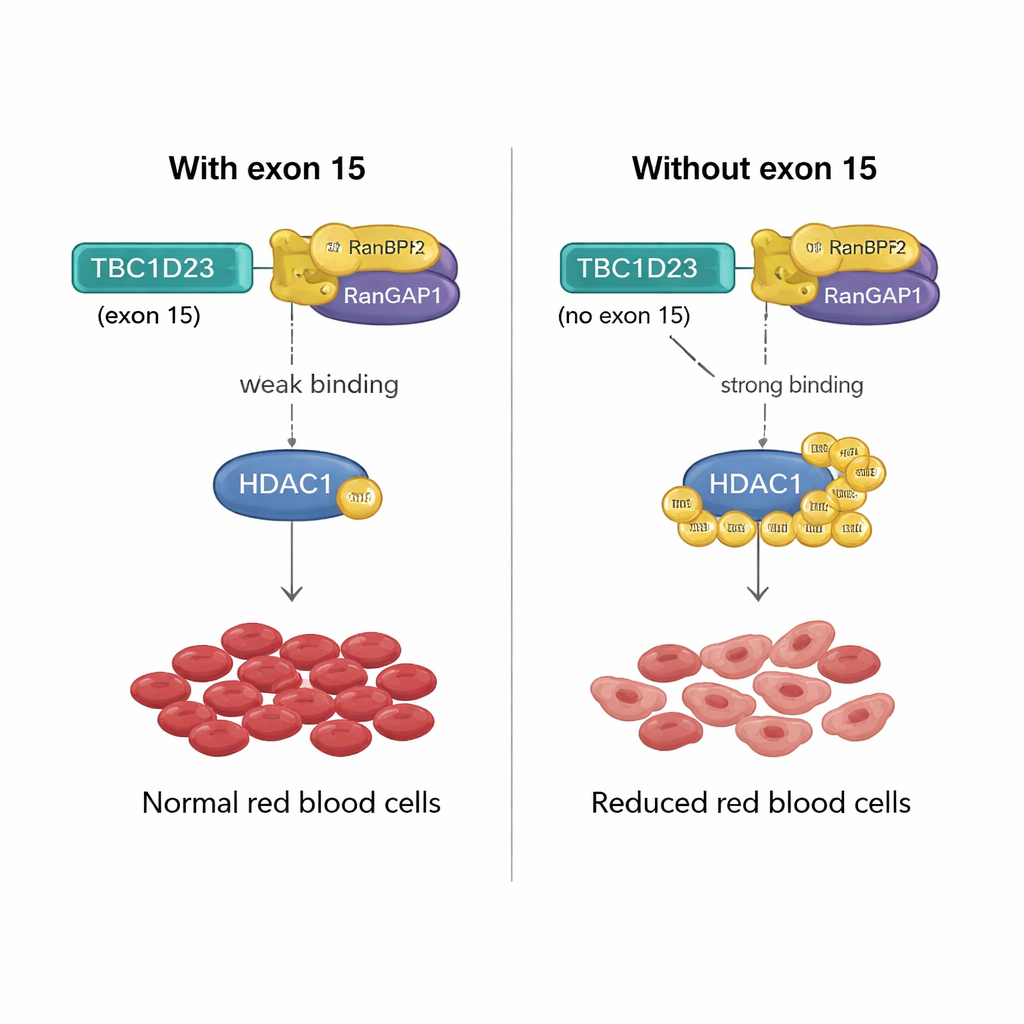
Uma alavanca molecular para a produção de glóbulos vermelhos
Como um trecho de 15 aminoácidos codificado pelo éxon 15 de TBC1D23 pode ter um efeito tão grande? A equipe descobriu que incluir esse éxon enfraquece a ligação de TBC1D23 a um par proteico chamado RANBP2/RANGAP1, que colabora para anexar marcas SUMO em outras proteínas. Sem o éxon 15, TBC1D23 liga-se mais fortemente a esse par, aumentando a SUMOilação de uma enzima-chave, HDAC1. Essa maior marcação altera a atividade de muitos fatores de transcrição — reguladores mestres da expressão gênica — desajustando os programas gênicos necessários para a maturação adequada dos glóbulos vermelhos. Quando os pesquisadores engenheiraram uma versão de HDAC1 que não pode ser SUMO-markada em duas posições cruciais, isso resgatou a formação de eritrócitos em células sem o éxon 15 de TBC1D23, confirmando que essa modificação química é o passo crítico.
Por que isso importa para a saúde e terapias futuras
Para um não especialista, a mensagem deste trabalho é que nem todas as mudanças genéticas são equivalentes: às vezes, a diferença entre sangue saudável e anemia está em se um pequeno segmento de um gene é mantido ou pulado na mensagem final. Ao combinar dados de RNA em grande escala com um sistema de pontuação sofisticado, o estudo fornece um roteiro para identificar quais variantes de splicing têm mais probabilidade de influenciar como células-tronco escolhem seus destinos. Essa abordagem não só aprofunda nossa compreensão de como as células sanguíneas são formadas em saúde e doença, como também oferece uma estratégia geral para localizar eventos de splicing importantes em outros órgãos, potencialmente guiando futuras terapias gênicas e tratamentos de precisão.
Citação: Hu, X., Wang, J., Chen, L. et al. The functional landscape of alternative splicing in hematopoietic lineage commitment. Nat Commun 17, 2047 (2026). https://doi.org/10.1038/s41467-026-68811-8
Palavras-chave: splicing alternativo, hematopoiese, aprendizado de máquina, glóbulos vermelhos, regulação gênica