Clear Sky Science · pt
Base estrutural da regulação transcricional pelo regulador da divisão celular MraZ em Mycoplasma genitalium
Como uma bactéria minúscula controla quando se divide
Toda célula viva precisa decidir quando se dividir em duas, e essa decisão pode significar a diferença entre crescimento saudável e uma infecção descontrolada. Este estudo examina uma das bactérias mais simples conhecidas, Mycoplasma genitalium, para revelar em detalhe atômico como uma única proteína, chamada MraZ, se prende ao DNA e liga ou desliga genes-chave da divisão celular. Ao entender esse sistema de controle minimalista, os cientistas esperam descobrir regras gerais do crescimento bacteriano que um dia possam inspirar novos tipos de antibióticos ou “células mínimas” sintéticas.
Uma célula reduzida com grandes lições
Mycoplasma genitalium é famosa por seu genoma diminuto: uma fração do DNA encontrado em bactérias comuns como E. coli. Esse tamanho reduzido a torna um modelo poderoso para identificar quais genes e sistemas de controle são realmente essenciais para a vida. Muitas bactérias mantêm seus genes de divisão celular e de parede celular agrupados em um bloco chamado de cluster dcw. Em micoplasmas sem parede, a maioria desses genes desapareceu, mas um punhado permanece, incluindo mraZ na dianteira do cluster. MraZ atua como um controlador de tráfego, regulando a atividade de genes vizinhos que, por sua vez, influenciam como e quando a célula se divide.
Um padrão de DNA repetido como um interruptor de controle
Logo a montante do gene mraZ, os pesquisadores encontraram um trecho de DNA altamente conservado que funciona como uma estação de acoplamento para a proteína MraZ. Essa região contém quatro segmentos curtos repetidos, ou “caixas”, que apresentam sequência quase idêntica em muitas espécies bacterianas. Ao mutar cuidadosamente uma, duas ou mais dessas caixas e então medir quão firmemente o MraZ ainda conseguia se prender ao DNA, a equipe demonstrou que a proteína se liga de forma cooperativa: cada caixa ajuda a fortalecer a ligação global. Experimentos com repórteres usando um marcador fluorescente confirmaram que quanto mais essas caixas eram perturbadas, menos eficazmente o MraZ conseguia reprimir a atividade gênica, destacando sua importância como um painel de controle finamente ajustado. 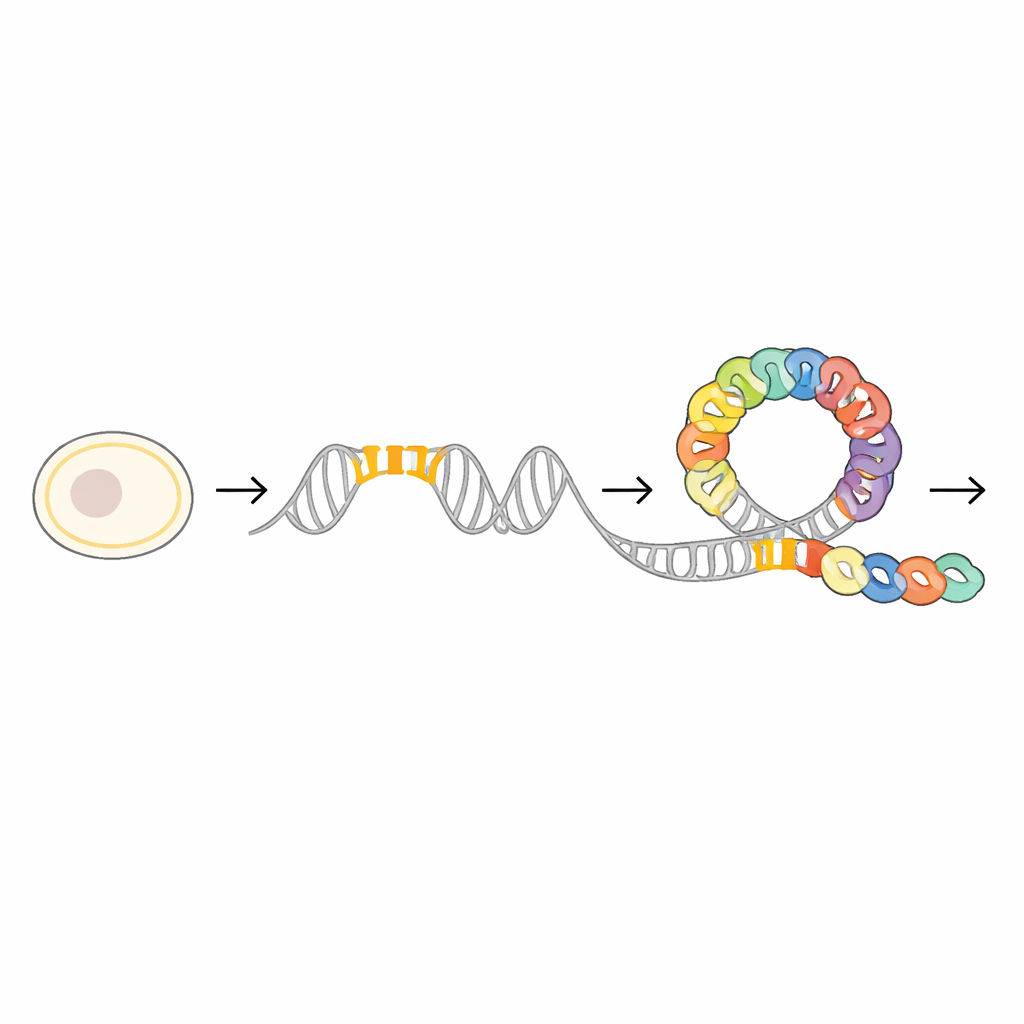
Uma proteína em forma de anel que se abre para envolver o DNA
Para ver como esse painel de controle funciona em nível atômico, os cientistas usaram crio-microscopia eletrônica e cristalografia de raios X para resolver várias estruturas tridimensionais do MraZ sozinho e ligado ao DNA. Sozinhas, as moléculas de MraZ juntam-se em montagens em forma de anel compostas por oito ou nove subunidades idênticas. Esses anéis têm uma superfície distintiva “em forma de berço” formada por uma pequena estrutura de folha-beta, diferente das hélices espirais frequentemente observadas em proteínas ligadoras de DNA. Quando o MraZ encontra seu segmento de DNA com quatro caixas, o anel não se limita a repousar sobre a hélice; em vez disso, ele se flexiona e se rearranja de modo que quatro de suas subunidades se alinham ao longo do DNA, cada uma acomodando uma caixa no sulco maior.
Pontos de contato-chave que leem o código do DNA
As estruturas em alta resolução revelaram que cada subunidade que contata o DNA usa três cadeias laterais carregadas positivamente — pontos específicos na superfície da proteína — para ler a sequência do DNA. Esses “dedos” químicos alcançam o sulco da dupla hélice e formam ligações de hidrogênio precisas com pares de bases particulares nas caixas conservadas. Quando os pesquisadores modificaram qualquer um desses três resíduos, o MraZ perdeu em grande parte a capacidade de se ligar ao DNA e de silenciar o gene repórter de teste. Contatos adicionais com a espinha dorsal do DNA ajudam a estabilizar o complexo, mas são menos específicos em termos de sequência. Em conjunto, essas descobertas mostram como o MraZ combina uma cabeça leitora altamente especializada com um corpo flexível de múltiplas subunidades para reconhecer sua região-alvo. 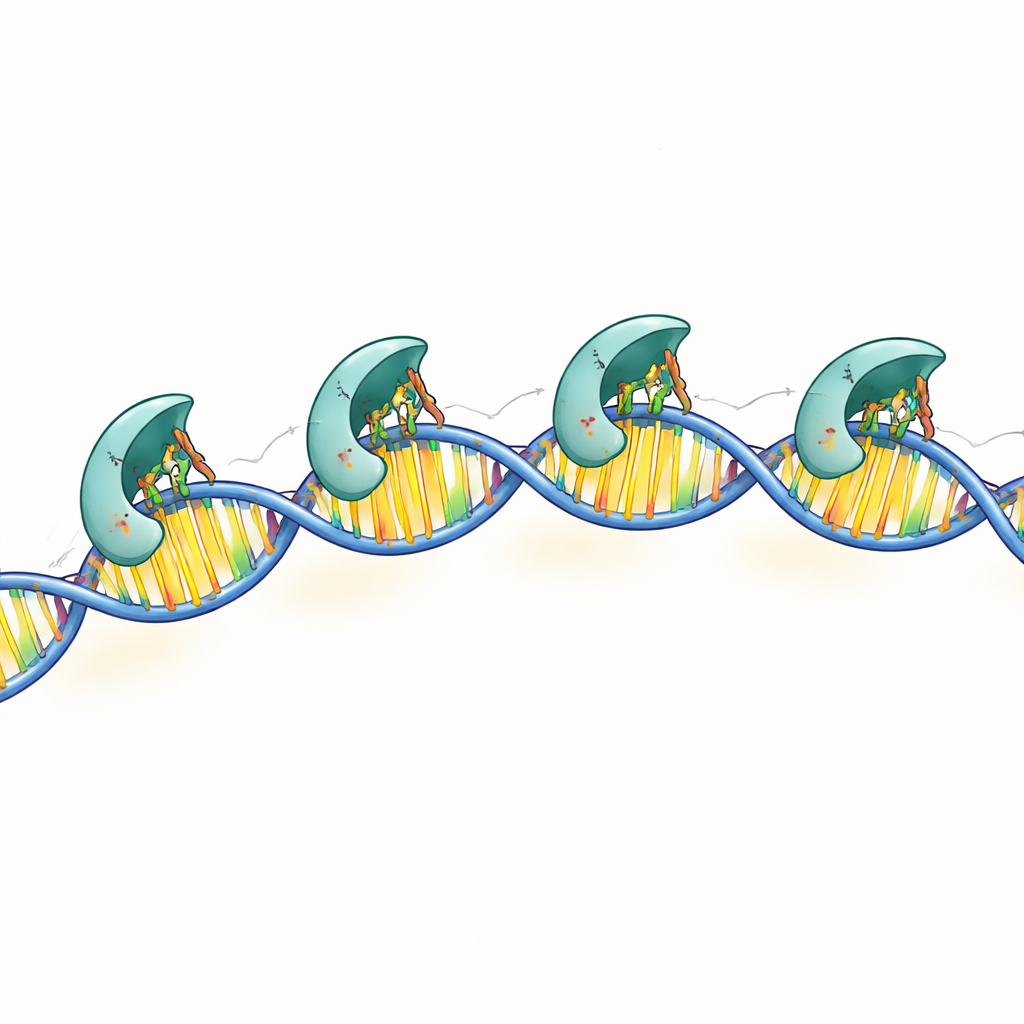
Oligômeros que ajustam a força do controle
Como o MraZ forma anéis e outras formas multiunidade, a equipe investigou se esse agrupamento é necessário para a ligação ao DNA ou apenas a ajusta finamente. Ao criar uma versão do MraZ que não podia mais se montar em anéis, descobriram que a proteína ainda se ligava à sequência de DNA das quatro caixas, porém com afinidade mais fraca. Essa forma monomérica teve dificuldade especialmente quando o espaçamento entre as caixas era alterado, sugerindo que o oligômero completo ajuda a ligar e alinhar caixas distantes, elevando a concentração local de motivos de ligação ao longo do DNA. Os autores propõem um modelo dinâmico no qual o MraZ alterna entre um anel fechado e uma forma aberta engajada ao DNA, usando seu estado de montagem como um botão para ajustar quão fortemente apreende o promotor.
O que isso significa para bactérias e além
Em termos simples, este trabalho explica como uma pequena proteína em uma bactéria mínima reconhece um padrão repetido no DNA e o usa como um interruptor mestre para genes de divisão celular. A combinação de uma cabeça leitora em forma de berço e um corpo anelar flexível permite que o MraZ reconheça seu alvo com alta precisão mantendo-se adaptável a diferentes arranjos de DNA. Como proteínas e motivos de DNA semelhantes aparecem em muitas bactérias, o mecanismo aqui descoberto provavelmente é uma estratégia compartilhada para coordenar crescimento e divisão. Insights desse sistema simplificado podem ajudar pesquisadores a projetar circuitos genéticos enxutos em células sintéticas e, a longo prazo, contribuir para novas formas de interromper o crescimento bacteriano em doenças.
Citação: Sánchez-Alba, L., Varejão, N., Durand, A. et al. Structural basis for transcriptional regulation by the cell division regulator MraZ in Mycoplasma genitalium. Nat Commun 17, 2132 (2026). https://doi.org/10.1038/s41467-026-68809-2
Palavras-chave: divisão celular bacteriana, interação DNA–proteína, regulação transcricional, crio-microscopia eletrônica, Mycoplasma genitalium