Clear Sky Science · pt
Trajetórias celulares e transcricionais da especificação do destino neural em anêmonas-do-mar revelam dois modos de neurogênese adulta
Como uma criatura marinha simples continua produzindo novas células cerebrais
A maioria dos animais, incluindo os humanos, gera a maior parte de seus neurônios cedo na vida e depois praticamente para. Ainda assim, algumas criaturas aparentemente simples, como as anêmonas-do-mar, continuam a acrescentar novas células nervosas ao longo da vida adulta. Este estudo investiga como a anêmona-estrelar (Nematostella vectensis) renova e remodela constantemente seu sistema nervoso difuso, revelando estratégias que podem ecoar soluções antigas para o crescimento e reparo de cérebros.
Um corpo em crescimento precisa de uma rede nervosa em crescimento
As anêmonas-do-mar não têm um cérebro; em vez disso, possuem uma rede nervosa emaranhada espalhada pela parede corporal. À medida que esses animais crescem ou encolhem dependendo da disponibilidade de alimento, sua rede nervosa deve aumentar ou diminuir para acompanhar. Usando uma proteína fluorescente sensível à luz como registro temporal, os autores marcaram neurônios existentes em adultos juvenis e então acompanharam o surgimento de células recém-nascidas na semana seguinte. Encontraram abundância de novos neurônios dispersos ao longo do eixo corporal, não restritos a uma zona de crescimento especial. Essas células recém-formadas apareceram tanto na extremidade voltada para a boca quanto na oposta do animal, mostrando que a neurogênese adulta é espacialmente difundida e contínua.
Rastreando as origens das novas células nervosas
Para descobrir de onde vêm essas novas células, os pesquisadores combinaram imagens ao vivo com sequenciamento de RNA de célula única, uma técnica que lê quais genes estão ativos em milhares de células individuais. Eles se concentraram em células que carregam “repórteres” fluorescentes controlados por três genes-chave: FoxL2, SoxC e Elav. FoxL2 marca um amplo reservatório de células progenitoras multipotentes em divisão; SoxC é ativado brevemente quando as células começam a se especializar; e Elav é fortemente ativo em neurônios peptidérgicos, que se comunicam principalmente por pequenos peptídeos sinalizadores. A equipe mostrou que uma população de progenitores FoxL2-positivos e Piwi1-positivos comporta-se como células-tronco: eles se autorrenovam enquanto geram continuamente descendentes diversos, incluindo neurônios, células urticantes chamadas cnidócitos e células secretoras. SoxC e Elav, em contraste, acendem-se apenas quando as células deixam esse reservatório de progenitores e se comprometem com destinos neurais particulares.
Dois caminhos diferentes para neurônios adultos
Ao alinhar o tempo dos repórteres com a assinatura de expressão gênica de cada célula, o estudo revelou duas rotas distintas para células neurais maduras. Neurônios peptidérgicos seguem um caminho direto: surgem de progenitores que já apresentam um perfil molecular “comprometido com peptidérgicos” e então se diferenciam rapidamente em uma variedade de subtipos neuronais. Novos membros de cada subtipo aparecem em proporção à frequência daquele subtipo já existente, sugerindo que o sistema mantém uma mistura balanceada de tipos neuronais em vez de favorecer certos tipos. Nessa linhagem, não há uma série clara de estações intermediárias; em vez disso, subtipos neuronais intimamente relacionados emergem em paralelo a partir de progenitores igualmente predispostos. 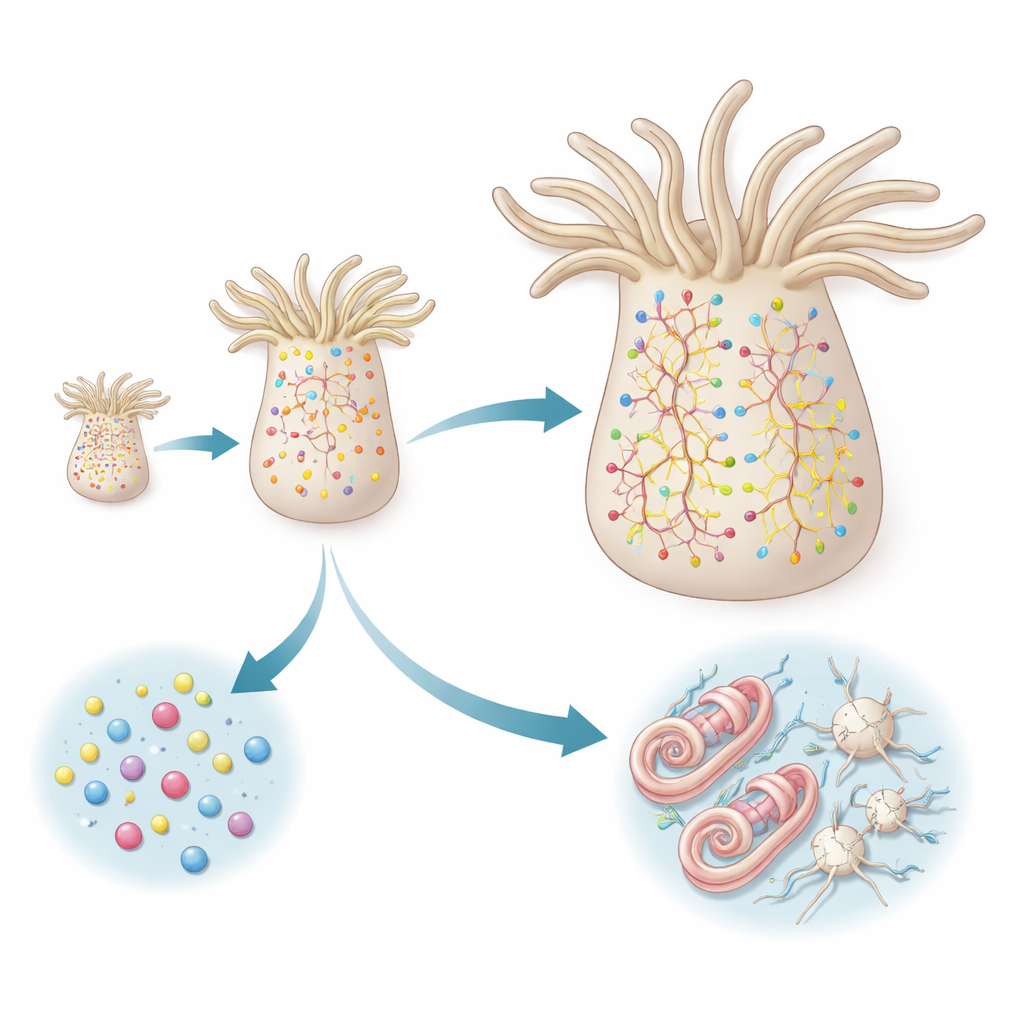
O caso especial das células urticantes
Os cnidócitos, as células urticantes exclusivas dos cnidários, seguem uma rota mais faseada. Eles primeiro passam por uma fase de “construção de cápsula”, durante a qual constroem seus orgânulos pressurizados característicos que podem disparar um arpão microscópico. Essa etapa depende de um conjunto específico de genes regulatórios e proteínas estruturais que estão em grande parte ausentes em outros tipos celulares. Só depois que esse programa intermediário é concluído os cnidócitos ligam um segundo programa, mais convencional, de natureza neural, adicionando canais iônicos e outros componentes necessários para a sinalização elétrica. Dados genéticos de mutantes que ficam estagnados na fase inicial reforçam esse modelo em duas fases: bloquear a transição impede o aparecimento das características neurais tardias. 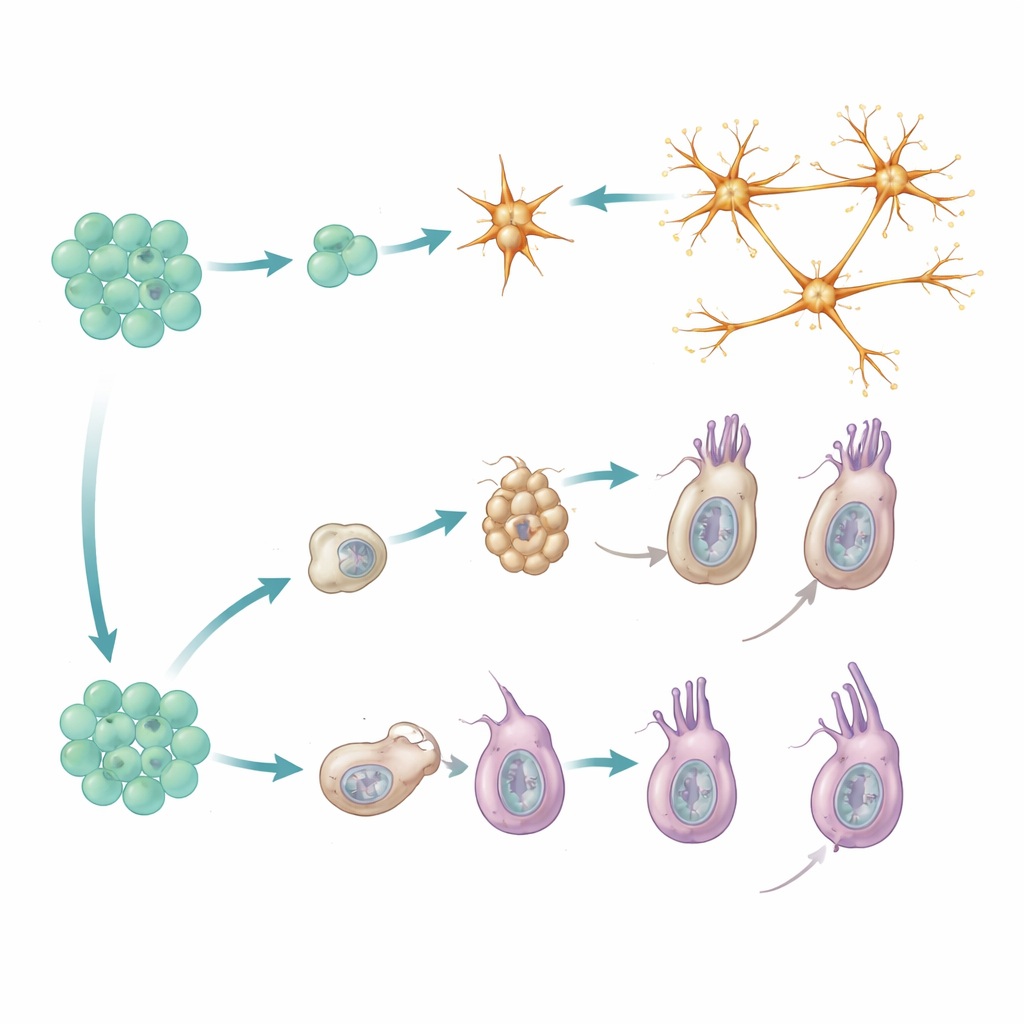
Regras compartilhadas e raízes antigas
Apesar de suas rotas diferentes, neurônios peptidérgicos e cnidócitos dependem de famílias sobrepostas de genes regulatórios para consolidar suas identidades. Características neurais amplas estão associadas a fatores de transcrição bHLH e bZIP, enquanto a identidade fina de cada subtipo neuronal é especificada por combinações únicas de genes homeobox e de dedos de zinco — um “código” que lembra como os tipos neuronais são definidos em animais mais complexos, incluindo vermes e vertebrados. Os autores argumentam que essas estratégias modulares — progenitores com comportamento semelhante ao de células-tronco, atividade transitória de SoxC durante o comprometimento e códigos homeobox que definem subtipos — podem representar princípios profundamente conservados da neurogênese. Em anêmonas-do-mar, elas sustentam a renovação ao longo da vida e a escalagem da rede nervosa; em outros animais, mecanismos relacionados podem subjazê-la tanto à neurogênese adulta limitada quanto às notáveis habilidades regenerativas vistas em algumas linhagens.
Citação: Plessier, F., Marlow, H. Cellular and transcriptional trajectories of neural fate specification in sea anemone uncover two modes of adult neurogenesis. Nat Commun 17, 2611 (2026). https://doi.org/10.1038/s41467-026-68802-9
Palavras-chave: neurogênese adulta, anêmona-do-mar, células progenitoras neurais, cnidócitos, transcriptômica de célula única