Clear Sky Science · pt
Entrega de coacervados peptídicos para formar centros de interação estáveis em células
Construindo Novas “Estações de Trabalho” Dentro das Células
Nossas células estão repletas de pequenos locais de trabalho onde tarefas importantes—como produção de energia ou respostas ao estresse—acontecem. Com o tempo, ou em doenças, essas estações naturais podem falhar. Este estudo explora uma maneira de acrescentar novos “centros de interação” em células vivas usando gotículas simples, feitas em laboratório, compostas por peptídeos curtos. Esses centros sintéticos podem captar proteínas específicas, concentrá‑las e até ajudar a degradá‑las, sugerindo novas estratégias para futuras terapias e engenharia celular.
Por Que as Células Precisam de Espaços de Trabalho Personalizados
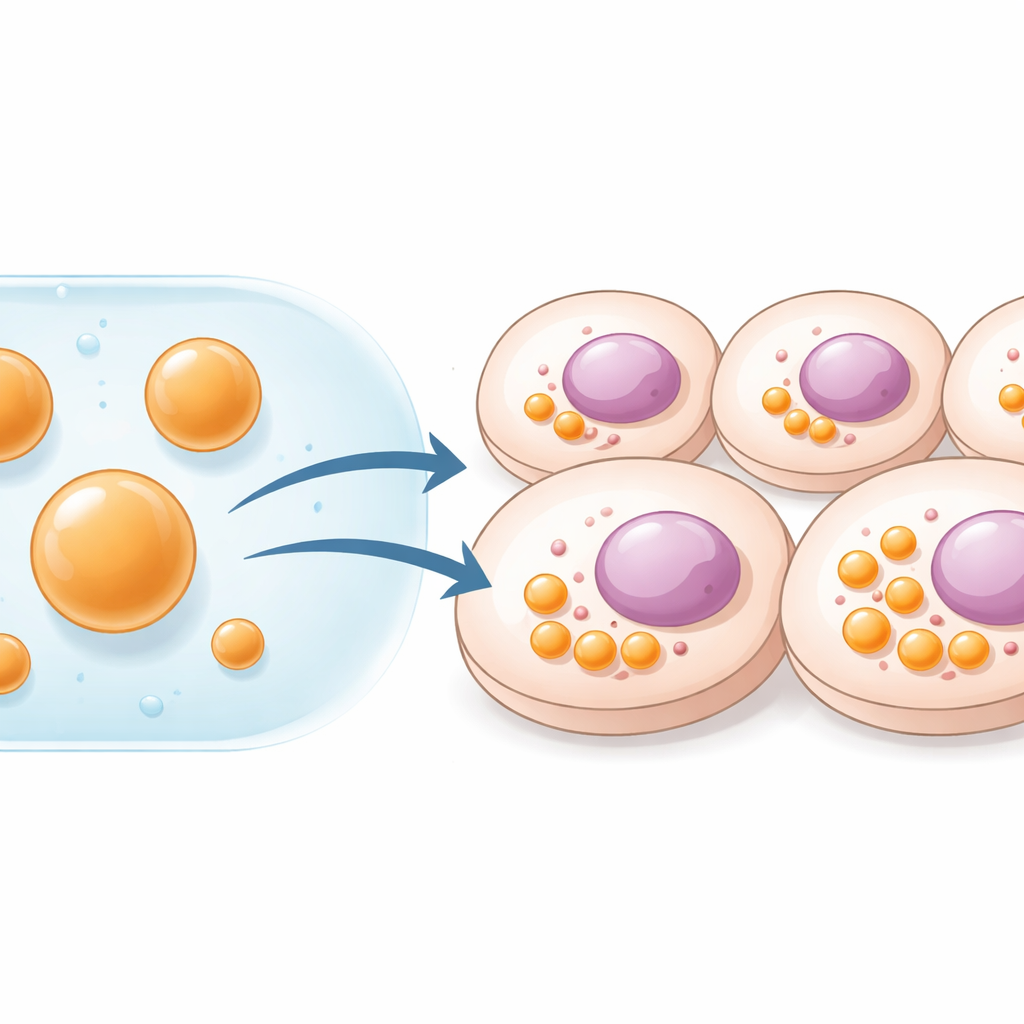
As células mantêm a ordem separando diferentes tarefas em compartimentos distintos. Alguns são envoltos por membranas, como as mitocôndrias; outros são estruturas mais “moles”, semelhantes a gotículas, que se formam quando certas proteínas e RNAs se agrupam. Essas gotículas fluidas, ou condensados, atuam como centros de reação que aceleram ou silenciam vias bioquímicas específicas. Pesquisadores já tinham projetado tais compartimentos forçando as células a produzir proteínas de andaime especiais a partir de genes introduzidos. Embora potente, esse método exige entrega de DNA e limita quanto material a célula pode sintetizar. Os autores deste estudo buscaram contornar o DNA por completo e, em vez disso, construir compartimentos prontos fora da célula, para então entregá‑los diretamente como gotículas estáveis de tamanho micrométrico.
Gotículas Peptídicas que Formam Centros Estáveis
A equipe trabalhou com peptídeos curtos e desordenados conhecidos como HBpep e uma variante redox‑responsiva, HBpep‑SA. Em condições levemente ácidas esses peptídeos permanecem dissolvidos, mas quando o pH é ajustado para níveis próximos aos fisiológicos—ou quando a temperatura é reduzida—eles se separan em fases, formando gotículas macias e tipo gel com cerca de 1–5 micrômetros de diâmetro. Ao ajustar a concentração de peptídeo, os pesquisadores puderam controlar tanto o tamanho quanto o número das gotículas. Usando técnicas de fluorescência, mostraram que as moléculas peptídicas dentro dessas gotículas se movem lentamente, indicando um estado gelatinoso suficientemente robusto para resistir à diluição e manuseio. Quando adicionadas a culturas de células humanas cancerígenas, células de melanoma de camundongo e células imunes humanas primárias, as gotículas foram captadas eficientemente e se acumularam no citoplasma. Gotículas maiores, em particular, permaneceram intactas por pelo menos cinco dias, atuando efetivamente como organelas sintéticas de longa duração dentro de células vivas.
Carregando e Direcionando os Centros
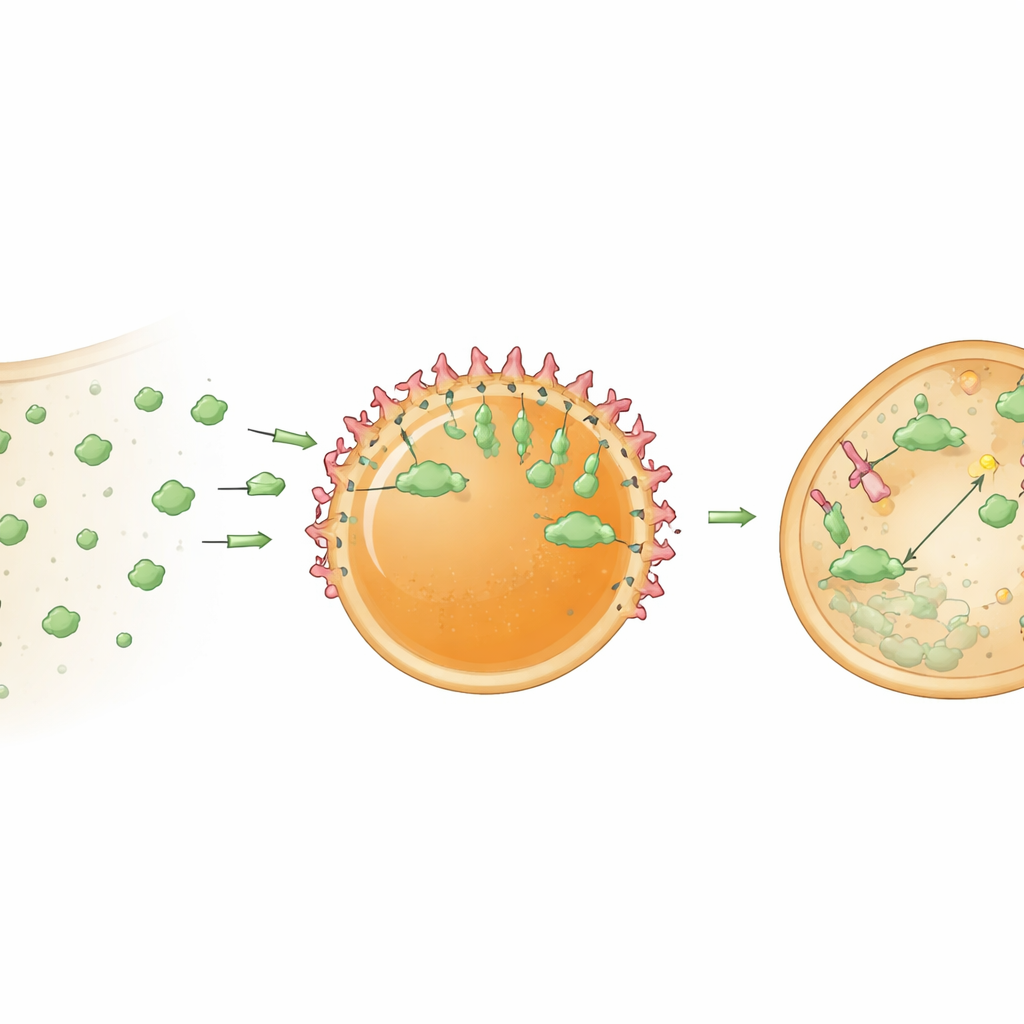
Para que esses centros fossem úteis, eles precisavam reter e organizar proteínas‑carga. Os pesquisadores primeiro melhoraram o carregamento anexando uma pequena etiqueta derivada de HBpep a uma proteína modelo, a GFP. Essa etiqueta incentivou a GFP a se particionar fortemente nas gotículas e, de forma interessante, a se concentrar perto de suas superfícies, criando uma organização núcleo‑casca. Em seguida, incorporaram nanocorpos—proteínas compactas semelhantes a anticorpos que se ligam fortemente a alvos escolhidos—dentro das gotículas. Um nanocorpo que se liga à GFP permitiu que os centros capturassem seletivamente a GFP tanto em tubos de ensaio quanto dentro de células. Como o gel peptídico é relativamente denso, inicialmente a maior parte da GFP capturada se acumulou na superfície das gotículas. Mas quando a estrutura interna foi parcialmente afrouxada, seja alterando condições redox ou ajudando as gotículas a escapar das membranas endossomais circundantes, a GFP também começou a penetrar o interior. Em células, coadjuvantes químicos que promovem a fuga endossomal aumentaram muito a fração de centros que recrutaram com sucesso seus alvos.
Transformando Centros em Trituradores de Proteínas
Os autores então atualizaram esses centros de armadilhas passivas para centros de processamento ativos. Eles carregaram as gotículas com um bioPROTAC—uma proteína de fusão que combina um nanocorpo de ligação ao alvo com parte de um adaptador enzimático que sinaliza proteínas para destruição pela maquinaria de descarte da célula. Quando essas gotículas “degradossomo” foram entregues em células que expressavam GFP de forma estável, os níveis de GFP citosólica caíram cerca de 78% dentro de um dia. Centros‑controle contendo apenas o nanocorpo sequestraram GFP, mas não reduziram apreciavelmente seu nível global, confirmando que a forte diminuição resultou da degradação direcionada em vez de simples captura. Os achados sugerem que agrupar bioPROTACs dentro de um microambiente concentrado os torna muito mais potentes do que quando estão dispersos livremente no citoplasma.
O Que Isso Pode Significar para Terapias Futuras
Em termos simples, este trabalho mostra que cientistas podem fabricar gotículas à base de peptídeos em um tubo de ensaio, preenchê‑las com ferramentas proteicas customizadas e então entregá‑las em células vivas onde se comportam como novas organelas duradouras. Esses centros sintéticos podem atrair seletivamente proteínas naturais e, quando equipados com maquinário de degradação, podem remover ativamente alvos escolhidos da célula. Como essa plataforma evita alterar os genes da célula e é modular no que pode transportar, ela abre um caminho para terapias que restauram ou reescrevem o comportamento celular—como eliminar proteínas nocivas ou reconfigurar sinalizações defeituosas—simplesmente instalando novas “estações de trabalho” programáveis em nossas células.
Citação: Tu, W., Theisen, R.Q., Jin, P. et al. Delivery of peptide coacervates to form stable interaction hubs in cells. Nat Commun 17, 2250 (2026). https://doi.org/10.1038/s41467-026-68793-7
Palavras-chave: organelas sintéticas, coacervados peptídicos, entrega intracelular, degradação de proteínas, engenharia celular