Clear Sky Science · pt
O trans-corte do CRISPR-Cas9 é impedido por um R-loop flanqueado, um espaçador alongado e um domínio HNH inativo
Por que pequenos cortes no DNA importam
O CRISPR-Cas9 é famoso como um bisturi molecular que pode cortar DNA em locais escolhidos, mas essa ferramenta tem um segundo comportamento, menos reconhecido: uma vez ativada, ela também pode roer outros fragmentos de material genético por perto. Entender quando esse corte “colateral” é ligado ou desligado é crucial para criar terapias de edição genética mais seguras e testes diagnósticos mais sensíveis. Este estudo dissecou as características físicas do complexo Cas9–DNA–RNA que determinam se o Cas9 faz silenciosamente seu corte pretendido ou também começa a mastigar fitas simples de DNA soltas.
Como as tesouras CRISPR são ativadas
Para agir, o Cas9 se liga a um pequeno trecho de RNA guia que o direciona a uma sequência de DNA correspondente no genoma. Quando o Cas9 encontra seu alvo, o RNA guia pareia com uma das fitas de DNA, forçando as duas fitas a se separarem e criando uma região híbrida DNA–RNA chamada R-loop. Em seu papel clássico, o Cas9 então corta ambas as fitas de DNA naquele ponto. Mas trabalhos recentes mostraram que, uma vez ativado dessa forma, o domínio de corte RuvC do Cas9 também pode fatiar DNA simples não relacionado, como trechos de pol(T), em outras partes da solução. Os autores investigaram: quais características geométricas e estruturais do DNA alvo e do RNA guia tornam essa atividade colateral forte, fraca ou ausente?
Alvos curtos versus longos: dando espaço para o Cas9 se mover
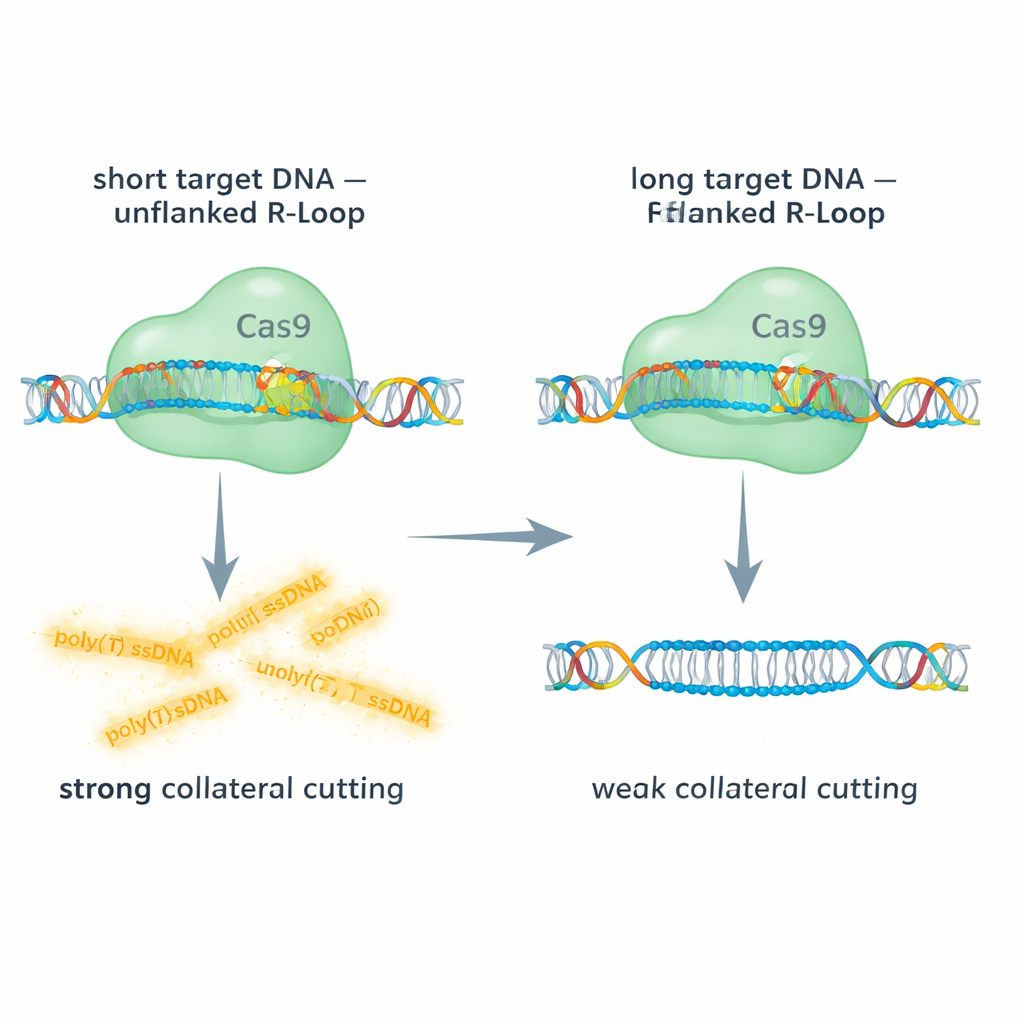
A equipe comparou o Cas9 agindo sobre alvos de DNA de dupla fita curtos e longos, usando leituras fluorescentes para acompanhar tanto o corte no alvo quanto o corte colateral de uma sonda de DNA de fita simples. Com alvos de DNA curtos, o R-loop na extremidade 5′ do RNA guia é “não flanqueado” — não há DNA de dupla fita extra além da região híbrida. Nessas condições, o Cas9 mostrou atividade colateral robusta sobre DNA de fita simples. Em contraste, quando usaram segmentos de DNA mais longos que deixavam DNA de dupla fita extra flanqueando o R-loop, o corte colateral caiu dramaticamente, às vezes em cerca de 90%, embora o corte principal no alvo ainda ocorresse. Alvos de DNA de fita simples longos, que removem o R-loop por completo, restauraram em grande parte a atividade colateral. Essas comparações revelam que uma “tampa” de dupla fita ao lado do R-loop endurece o complexo e impede fisicamente o acesso ou a flexibilidade necessários para que o domínio RuvC do Cas9 corte outras fitas.
Ajustes finos com comprimento do guia e mismatches
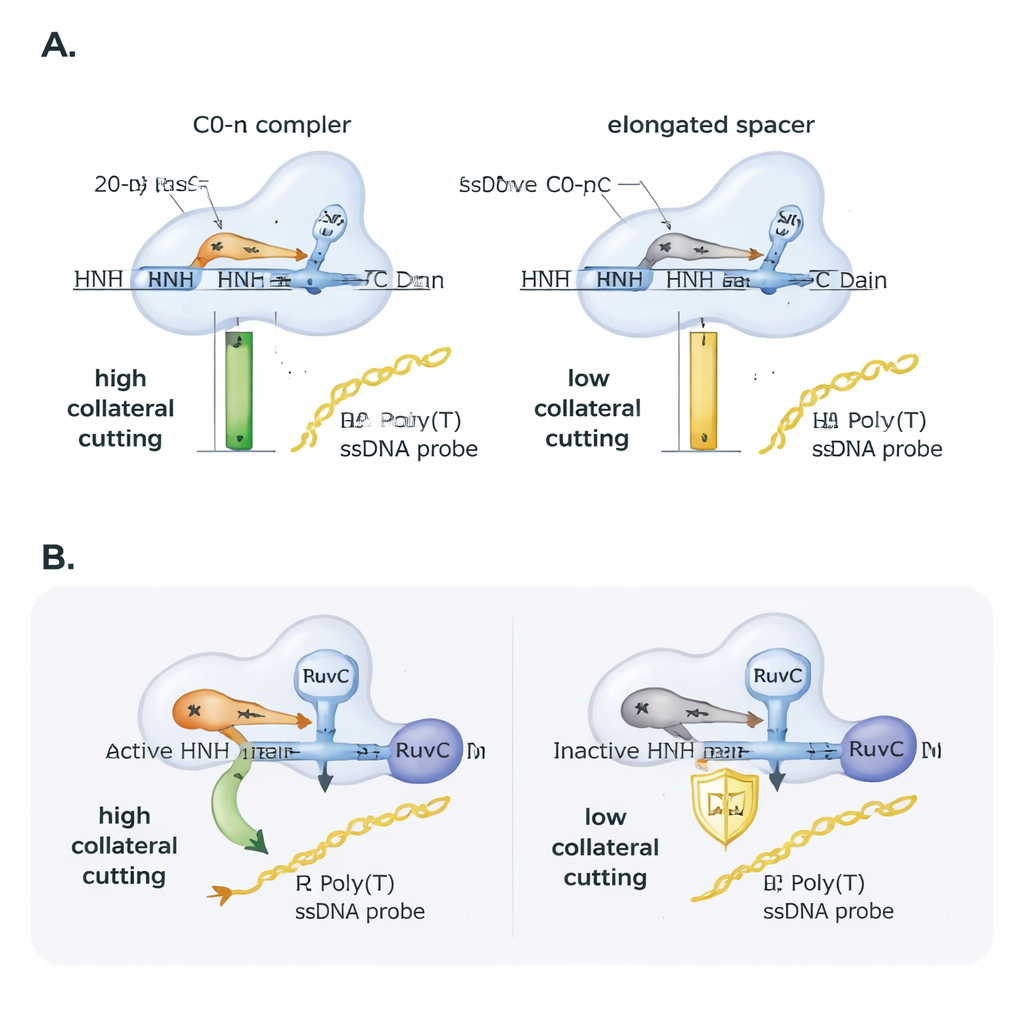
Os pesquisadores então exploraram como o próprio RNA guia regula esse comportamento. Eles introduziram pequenos mismatches entre o guia e o DNA alvo e monitoraram quão bem o Cas9 ainda cortava. O corte principal no alvo tolerou muitos mismatches de base única, mas o corte colateral foi mais frágil e dependente da posição exata do mismatch, ressaltando sua sensibilidade. Em seguida, alongaram sistematicamente o espaçador do RNA guia além dos habituais 20 nucleotídeos. Mesmo que o Cas9 ainda conseguisse reconhecer e cortar o DNA alvo, a atividade colateral caiu quase linearmente conforme o espaçador aumentava: acrescentar apenas duas bases extras reduziu a atividade colateral aproximadamente pela metade, e quatro bases extras a reduziram ainda mais. Em testes práticos usando material genético do SARS-CoV-2, somente amplicons de DNA organizados para produzir um R-loop não flanqueado com um guia de comprimento padrão deram um sinal colateral forte, destacando como o desenho de primers e guias pode fazer ou desfazer ensaios de detecção baseados em CRISPR.
Um domínio auxiliar essencial nos bastidores
O Cas9 possui dois domínios de corte, RuvC e HNH. Trabalhos anteriores ligaram o corte colateral diretamente ao RuvC, mas este estudo mostra que o HNH ainda importa. Quando os autores usaram uma variante de Cas9 com o domínio HNH inativo, a atividade colateral despencou, embora a ligação ao alvo e o comportamento de nicking permanecessem. Curiosamente, se forneceram ao Cas9 um alvo de DNA que já estava nickado em uma fita, a versão com HNH inativo recuperou a atividade colateral semelhante à da enzima normal. Isso sugere que o papel do HNH é em parte mecânico: ao cortar ou afrouxar a fita alvo, ele ajuda a proteína a adotar uma conformação que expõe o RuvC ao DNA de fita simples próximo. Análises estruturais de modelos 3D existentes apoiaram essa visão, mostrando que R-loops não flanqueados e guias de comprimento padrão permitem que a extremidade 5′ do RNA “tape” contra o Cas9 e posicionem favoravelmente as regiões catalíticas, enquanto R-loops flanqueados e guias alongados compactam mais a proteína e provavelmente protegem o sítio RuvC de fitas soltas.
O que isso significa para ferramentas futuras
Para não especialistas, a mensagem principal é que o comportamento do Cas9 não é tudo ou nada: detalhes geométricos minúsculos — quanto o DNA se estende, quão longo é o guia e se um domínio auxiliar pode completar seu corte — decidem se a enzima se atém à sua função principal ou também destrói fitas simples por perto. Alvos curtos que deixam o R-loop não flanqueado, guias padrão de 20 bases e um domínio HNH ativo promovem conjuntamente corte colateral forte; DNA flanqueador longo, guias alongados ou um domínio HNH inativo o suprimem. Esses insights dão aos pesquisadores um controle mais preciso sobre o Cas9, ajudando-os a projetar sistemas de edição genética mais seguros que evitem danos colaterais indesejados, ou ensaios diagnósticos mais potentes que aproveitem deliberadamente essa atividade colateral para detectar quantidades ínfimas de material viral ou genético.
Citação: Montagud-Martínez, R., Ruiz, R., Baldanta, S. et al. CRISPR-Cas9 trans-cleavage is hindered by a flanked R-loop, an elongated spacer, and an inactive HNH domain. Nat Commun 17, 1998 (2026). https://doi.org/10.1038/s41467-026-68789-3
Palavras-chave: CRISPR-Cas9, corte colateral, R-loop, espaciador de RNA guia, diagnósticos de ácidos nucleicos