Clear Sky Science · pt
NatA participa de complexos multifatoriais na saída do túnel polipeptídico ribossômico
Como as células ajustam novas proteínas à medida que nascem
Cada segundo, suas células fabricam milhares de novas proteínas em pequenas máquinas chamadas ribossomos. À medida que cada cadeia proteica emerge, ela precisa ser aparada, etiquetada e dobrada corretamente; caso contrário, pode se comportar de forma inadequada e contribuir para doenças. Este estudo examina um dos sistemas de marcação chave, uma modificação chamada acetilação N-terminal, e mostra como um complexo enzimático central, NatA, trabalha em conjunto com vários parceiros justamente onde as novas proteínas saem do ribossomo. Compreender essa coreografia ajuda a explicar como as células mantêm suas fábricas de proteínas funcionando sem problemas.
A pequena marca química que importa
A maioria das proteínas começa a vida com o mesmo primeiro bloco construtor, o aminoácido metionina. Frequentemente, essa metionina inicial é removida e substituída por uma pequena marca química chamada grupo acetila. Essa marca, adicionada à ponta da proteína (seu N-terminal), pode influenciar quanto tempo a proteína sobrevive, para onde ela vai na célula e como ela funciona. Dois tipos principais de enzimas ficam na saída do túnel do ribossomo para gerenciar essa primeira transformação: as metionina aminopeptidases (MAPs), que cortam a metionina inicial, e as N-acetiltransferases (NATs), que adicionam a acetila. Entre as NATs, NatA é o cavalo de trabalho nas células humanas, potencialmente modificando quase 40% de todas as proteínas. Como muitas proteínas são produzidas ao mesmo tempo, a célula precisa organizar essas enzimas para que o corte e a marcação ocorram rapidamente e na ordem certa.
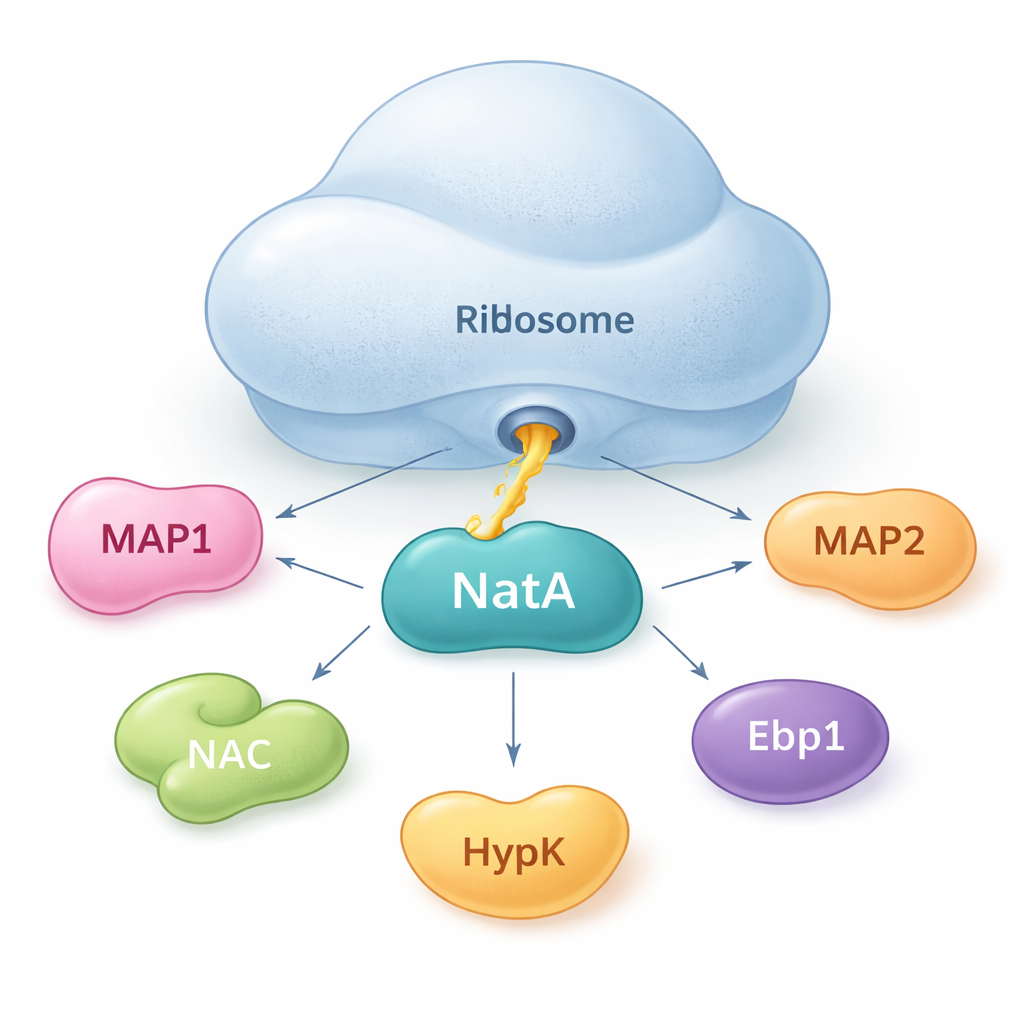
NatA como um ponto de encontro para ajudantes proteicos
Os autores mostram que NatA não age sozinho. Em vez disso, ele se comporta como um hub que reúne múltiplas proteínas auxiliares, tanto sobre o ribossomo quanto soltas no citosol. Usando medições sensíveis de ligação em solução, descobriram que NatA pode formar complexos estáveis com MAP1, o complexo associado à polipeptídeo nascente (NAC), a proteína regulatória HypK e outra enzima, Naa50, mesmo sem o ribossomo presente. O NAC pode conectar NatA ao MAP1, permitindo que as etapas de corte e acetilação fiquem ligadas em um único conjunto. Entretanto, HypK, que normalmente reduz a atividade de NatA, pode impedir a ligação do NAC. Isso sugere que as células podem alternar NatA entre um estado mais ativo, ligado ao NAC, e um estado restringido, ligado ao HypK, dependendo de suas necessidades.
Um segundo ponto de ancoragem bem na saída do túnel
Ao usar criomicroscopia eletrônica, uma técnica que imagina grandes moléculas em detalhe quase atômico, os pesquisadores descobriram que NatA pode se ligar ao ribossomo em duas posições distintas. Um sítio, já conhecido, fica um pouco afastado da saída do túnel. O sítio recém-descoberto, “proximizado”, posiciona o núcleo catalítico de NatA muito próximo de onde a cadeia proteica em crescimento emerge, encurtando a distância que a cadeia precisa percorrer para ser modificada. De forma intrigante, ambas as posições podem estar ocupadas ao mesmo tempo, o que significa que dois complexos NatA podem sentar no mesmo ribossomo. A cópia mais distante atua como uma plataforma e âncora, enquanto a cópia proximal está idealmente posicionada para marcar novas proteínas. As duas moléculas de NatA também se tocam, indicando que NatA pode coordenar suas próprias duplicatas em equipes multi-enzimáticas.
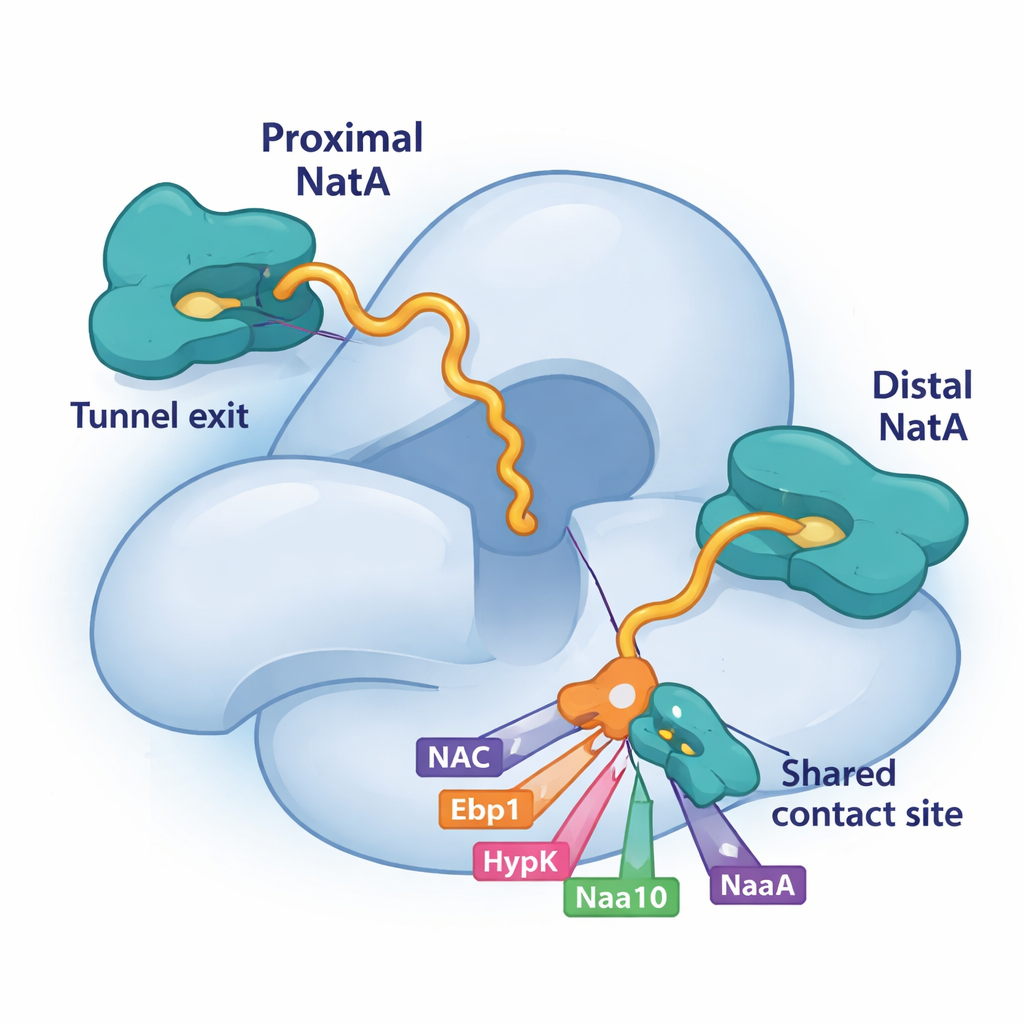
Competição por um ponto de atracagem compartilhado em NatA
Uma peça-chave desse quebra-cabeça é um pequeno sulco na subunidade grande de NatA, Naa15. O estudo mostra que quatro fatores associados ao ribossomo—NAC, HypK, Ebp1 e até um segmento da cauda da própria subunidade catalítica de NatA, Naa10—usam hélices curtas para se fixar exatamente no mesmo trecho de Naa15. Por dependerem desse ponto de atracagem compartilhado, eles têm de competir pelo acesso. Quando HypK ocupa o sítio, ele não apenas silencia a atividade de NatA, como também impede que NatA se associe ao NAC ou forme dímeros NatA–NatA. Quando NAC, a pseudo-enzima Ebp1 ou o Naa10 proximal se ligam ali em vez disso, eles podem remodelar a posição ou as conexões de NatA no ribossomo. Essa ligação competitiva dá à célula uma maneira flexível de escolher quais parceiros se montam ao redor de NatA a cada momento.
Uma pseudo-enzima como controlador de tráfego
A proteína Ebp1 é especialmente intrigante. Ela se assemelha a uma das enzimas que removem a metionina, mas carece de atividade catalítica; é uma “pseudo-enzima”. Trabalhos anteriores mostraram que Ebp1 pode sentar-se no ribossomo perto da saída do túnel e prender um longo segmento de RNA. Neste estudo, os autores constatam que, quando NatA se une ao ribossomo, Ebp1 muda de posição, libera o RNA e, em vez disso, usa sua própria hélice para ocupar o mesmo sítio de ligação em Naa15 que NAC e HypK utilizam. Esse rearranjo sugere que Ebp1 pode agir como um marcador temporário ou organizador: ela pode moldar o ambiente local de RNA e depois passar o controle para enzimas ativas como as MAPs e NatA, sem realizar diretamente a química ela mesma.
Por que esse controle de multidão molecular importa
Para um não-especialista, os detalhes de hélices e sítios de ligação podem soar abstratos, mas a mensagem é simples: as células executam um sistema de controle de qualidade multietapa e muito coreografado bem onde as proteínas nascem. NatA fica no centro desse sistema, capaz de recrutar ou liberar diferentes parceiros dependendo de quais fatores ganham acesso a uma mancha de acoplamento crucial e qual sítio ribossômico NatA ocupa. Essa rede flexível ajuda a garantir que o corte e a acetilação ocorram com o tempo e a ordem corretos para milhares de proteínas diferentes. Como erros no processamento N-terminal estão ligados a distúrbios do desenvolvimento, neurodegeneração e câncer, mapear como NatA e seus parceiros se montam fornece aos pesquisadores um roteiro mais claro de como o processamento precoce de proteínas é controlado — e como ele pode ser alvo quando sai do trilho.
Citação: Klein, M., Wild, K., McTiernan, N. et al. NatA engages in multi-factor complexes at the ribosomal polypeptide tunnel exit. Nat Commun 17, 884 (2026). https://doi.org/10.1038/s41467-026-68787-5
Palavras-chave: controle de qualidade de proteínas, acetilação N-terminal, saída do túnel ribossômico, complexo NatA, modificação co-traducional