Clear Sky Science · pt
A fucosiltransferase vegetal FUT11 distorce o aceptor de açúcar para catalisar via um mecanismo intermediário oxocarbenium transitório
Como as plantas ajustam finamente os açúcares em suas proteínas
Proteínas em nossas células, e nas plantas, frequentemente são decoradas com cadeias complexas de açúcares que funcionam como códigos de barras, orientando como essas proteínas se dobram, quanto tempo persistem e com quais parceiros podem interagir. Este estudo foca em uma enzima vegetal chamada FUT11 que adiciona um açúcar minúsculo, a fucose, a essas cadeias. Ao descobrir exatamente como a FUT11 atua em nível atômico, os autores revelam um truque surpreendente: a enzima dobra brevemente seu parceiro açucarado fora de forma para impulsionar um passo químico difícil. Compreender esse processo importa não só para a biologia fundamental, mas também para projetar medicamentos produzidos em plantas que evitem desencadear reações imunes indesejadas em humanos.
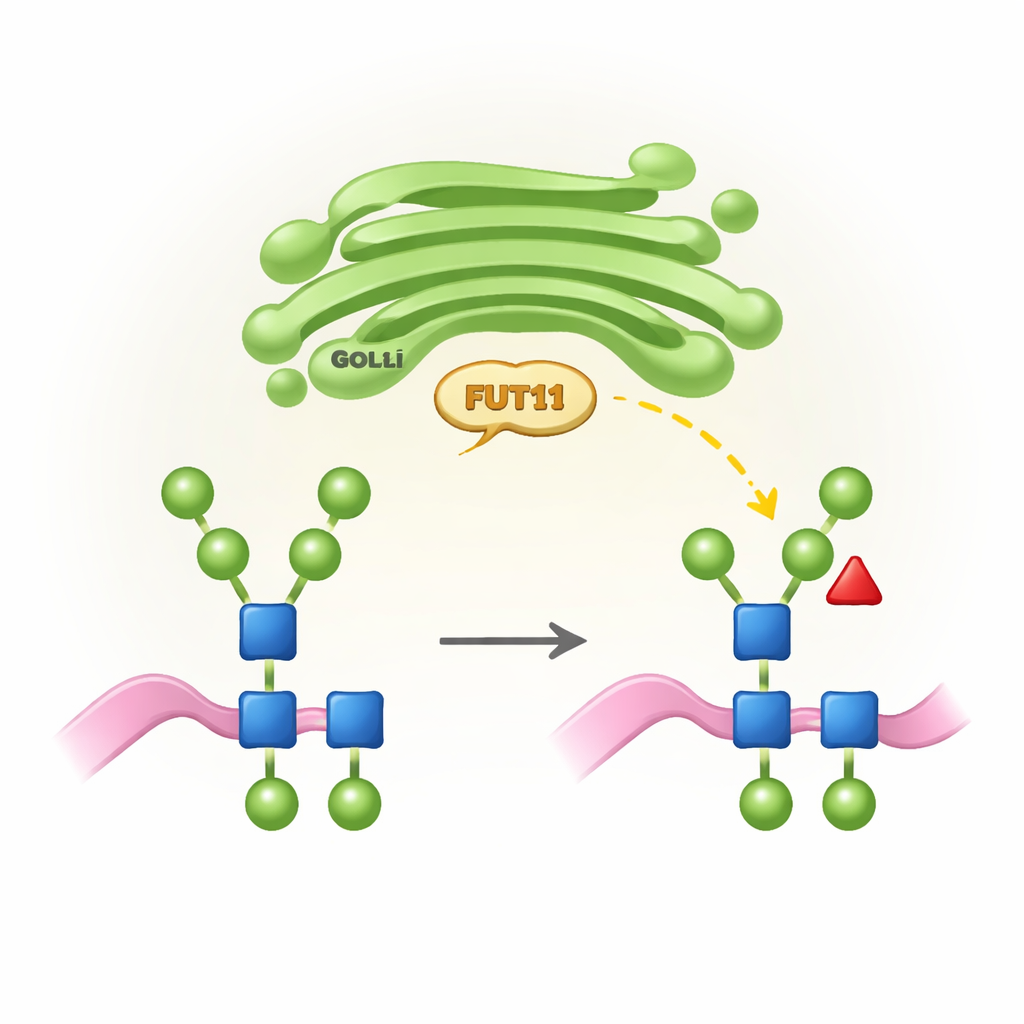
Marcas de açúcar específicas das plantas e por que importam
Todos os organismos superiores usam um processo chamado N-glicosilação para ligar cadeias de açúcares (N-glicanos) a pontos específicos nas proteínas. Em animais, essas cadeias são remodeladas no aparelho de Golgi da célula em estruturas elaboradas que frequentemente terminam com ácidos siálicos e carregam uma fucose central em uma posição específica. As plantas, no entanto, seguem uma “regra de projeto” diferente: seus N-glicanos tipicamente não têm ácido siálico, mas carregam uma fucose central em outra posição (chamada b1,3) além de uma xilose extra. Essas características específicas das plantas são essenciais para o crescimento e a fertilidade normais, mas podem ser vistas como estranhas pelo sistema imunológico humano. FUT11 é uma das enzimas vegetais chave que instala essa fucose central, e sua atividade molda tanto o desenvolvimento vegetal quanto a forma como proteínas terapêuticas produzidas em plantas serão percebidas em nossos corpos.
Mapeando onde a FUT11 pode atuar em ramificações complexas de açúcar
Para entender o que a FUT11 reconhece, os pesquisadores testaram a enzima em um microarranjo de 144 estruturas diferentes de N-glicanos. Eles descobriram que a FUT11 é bastante seletiva quanto a um ramo da árvore de açúcar — o chamado braço b1,3 — que deve portar um bloco construtor particular (uma N-acetilglucosamina terminal, ou GlcNAc) para que a reação prossiga. Ao mesmo tempo, a FUT11 tolera outras decorações: ela ainda funciona quando a manose central carrega uma xilose exclusiva de plantas, e mesmo quando outra fucose já foi adicionada na posição típica de mamíferos no núcleo. O ramo oposto (b1,6) está em grande parte exposto ao solvente e faz apenas contatos fracos com a enzima, o que explica por que a FUT11 pode lidar com uma ampla variedade de modificações ali. Essas preferências de ligação ajudam a explicar por que as plantas produzem um conjunto característico de estruturas de N-glicanos e mostram como a FUT11 poderia ser utilizada ou evitada ao engenheirar células vegetais para biotecnologia.
Um desenho estrutural único para capturar e posicionar açúcares
Usando cristalografia de raios X, a equipe resolveu a estrutura tridimensional da FUT11 ligada ao seu doador de açúcar (GDP-fucose) e a um aceptor de N-glicano. A enzima tem uma arquitetura de duas lobulações do tipo “GT-B”: uma lóbulos acolhe o GDP-fucose, enquanto um lóbulos de aceptor incomumente elaborado, incluindo um subdomínio N-terminal específico de plantas, envolve o N-glicano. Esse subdomínio extra, ligado ao resto da enzima por pontes dissulfeto, ancora a parte central do glicano e ajuda a apresentar a unidade reativa GlcNAc em direção ao doador. Mutar aminoácidos-chave confirmou seus papéis: alterar um único glutamato (Glu158) eliminou a atividade, enquanto modificar duas residências próximas enfraqueceu muito a fucosilação em células humanas reengenheiradas. Esses resultados conectam instantâneos estruturais à função celular real, mostrando exatamente quais partes da proteína são indispensáveis para a ligação e catálise.
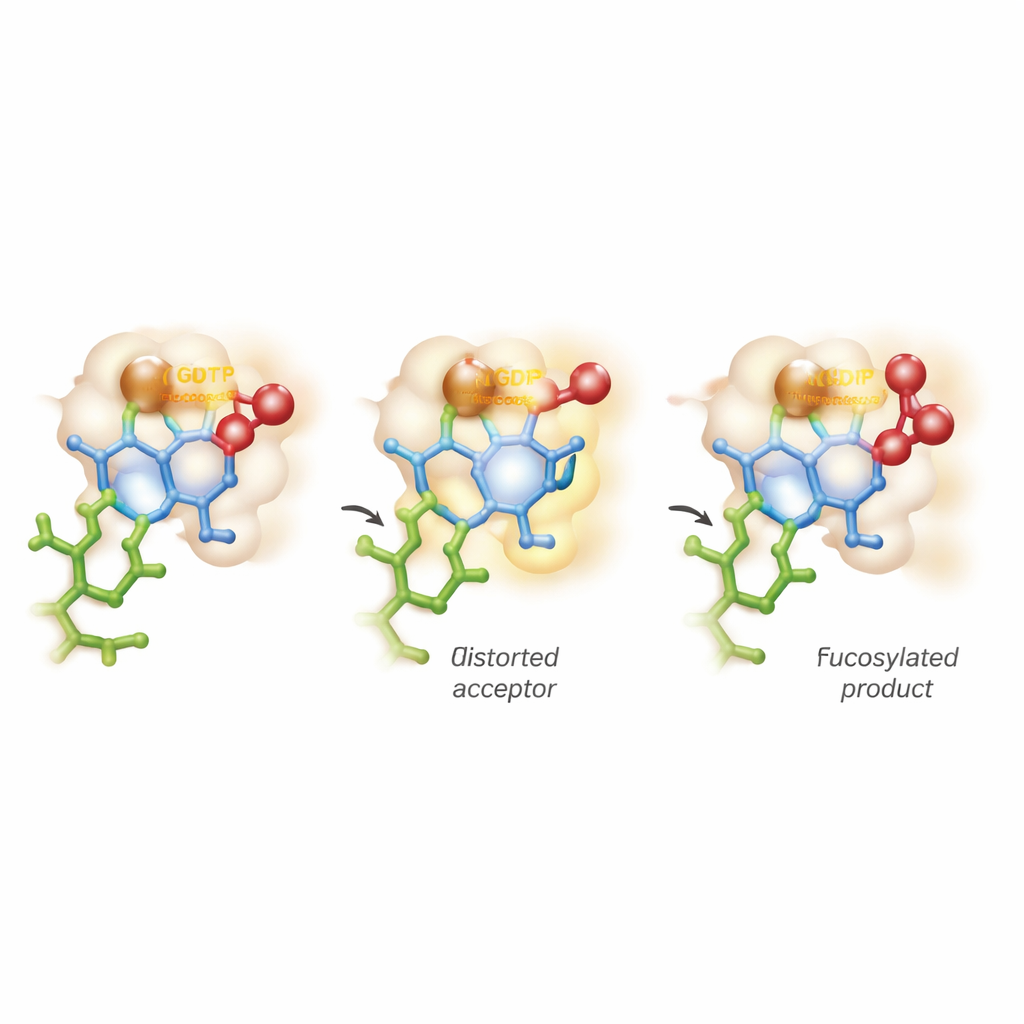
Dobrando o açúcar e caminhando na linha entre dois caminhos de reação
A percepção mais marcante vem de simulações computacionais avançadas que combinam mecânica quântica e dinâmica molecular. Visões tradicionais assumem que o açúcar aceptor mantém sua forma estável, em cadeira, enquanto a enzima simplesmente ativa o doador. Aqui, a FUT11 se comporta de forma mais agressiva: interações mediadas por Glu158 distorcem temporariamente o anel interno de GlcNAc para uma forma menos confortável e pregueada. Nessa postura tensionada, o grupo hidroxila crítico fica perfeitamente alinhado para atacar o doador de fucose. Os cálculos revelam que, à medida que a ligação química com o GDP se rompe, surge um estado de curta duração e carga positiva, parecido com um oxocarbenium, no açúcar, antes que a nova ligação ao aceptor esteja totalmente formada. Isso significa que a reação não se encaixa de forma limpa nas categorias SN1 ou SN2 dos livros didáticos, mas prossegue ao longo de um contínuo, de forma assíncrona e quase em etapas.
Flexibilidade oculta e ecos evolutivos
Ao comparar a FUT11 com uma enzima humana relacionada, FUT9, os autores encontraram que a enzima vegetal também pode, embora fracamente, modificar um tipo diferente de motivo açucarado (LacNAc) para formar uma estrutura conhecida como Lewis X. Essa atividade lateral provavelmente não é biologicamente importante nas plantas, onde Lewis X não é normalmente observado, mas ressalta como andaimes proteicos semelhantes podem ser reaproveitados ao longo da evolução para atuar em contextos açucarados distintos. O estudo sugere que a FUT11 e suas parentes compartilham uma estrutura modular para reconhecer N-glicanos, com ajustes sutis que deslocam a especificidade entre núcleos vegetais e antenas animais.
Por que esse truque de dobragem importa para ciência e medicina
Em conjunto, o trabalho mostra que a FUT11 faz mais do que simplesmente aproximar dois parceiros açucarados: ela ativamente dobra o açúcar aceptor em uma pose reativa e canaliza a química através de um intermediário carregado efêmero. Para um leitor leigo, isso significa que o açúcar na proteína não é um sítio de ancoragem rígido, mas um participante flexível que a enzima molda conforme necessário. Essa nova visão de “catálise conformacional” ajuda a explicar como as enzimas alcançam rapidez e seletividade e oferece um roteiro para redesenhar vias de glicosilação. Em termos práticos, saber exatamente como a FUT11 reconhece e modifica N-glicanos vegetais pode guiar a engenharia de plantas cultivadas e de sistemas de produção baseados em plantas para minimizar padrões de açúcar que disparam o sistema imunológico humano, ou para criar glicoproteínas customizadas com propriedades biológicas sob medida.
Citação: Taleb, V., Sanz-Martínez, I., Serna, S. et al. Plant fucosyltransferase FUT11 distorts the sugar acceptor to catalyze via a transient oxocarbenium intermediate mechanism. Nat Commun 17, 1960 (2026). https://doi.org/10.1038/s41467-026-68786-6
Palavras-chave: glicosilação vegetal, fucosiltransferase FUT11, N-glicanos, mecanismo enzimático, glicoengenharia