Clear Sky Science · pt
Base estrutural e implicações patológicas do complexo central dimérico OS9-SEL1L-HRD1 da ERAD
A equipe de limpeza celular sob o microscópio
Dentro de cada uma de nossas células, uma fábrica movimentada converte instruções genéticas em proteínas funcionais. Como em qualquer fábrica, ocorrem erros. Quando proteínas se dobram de forma errada, podem entupir o sistema e contribuir para doenças. Este estudo investiga uma das principais máquinas de controle de qualidade da célula — o complexo SEL1L‑HRD1 — para revelar sua estrutura 3D detalhada e mostrar como pequenas mudanças genéticas podem romper essa maquinaria e potencialmente levar a enfermidades humanas.
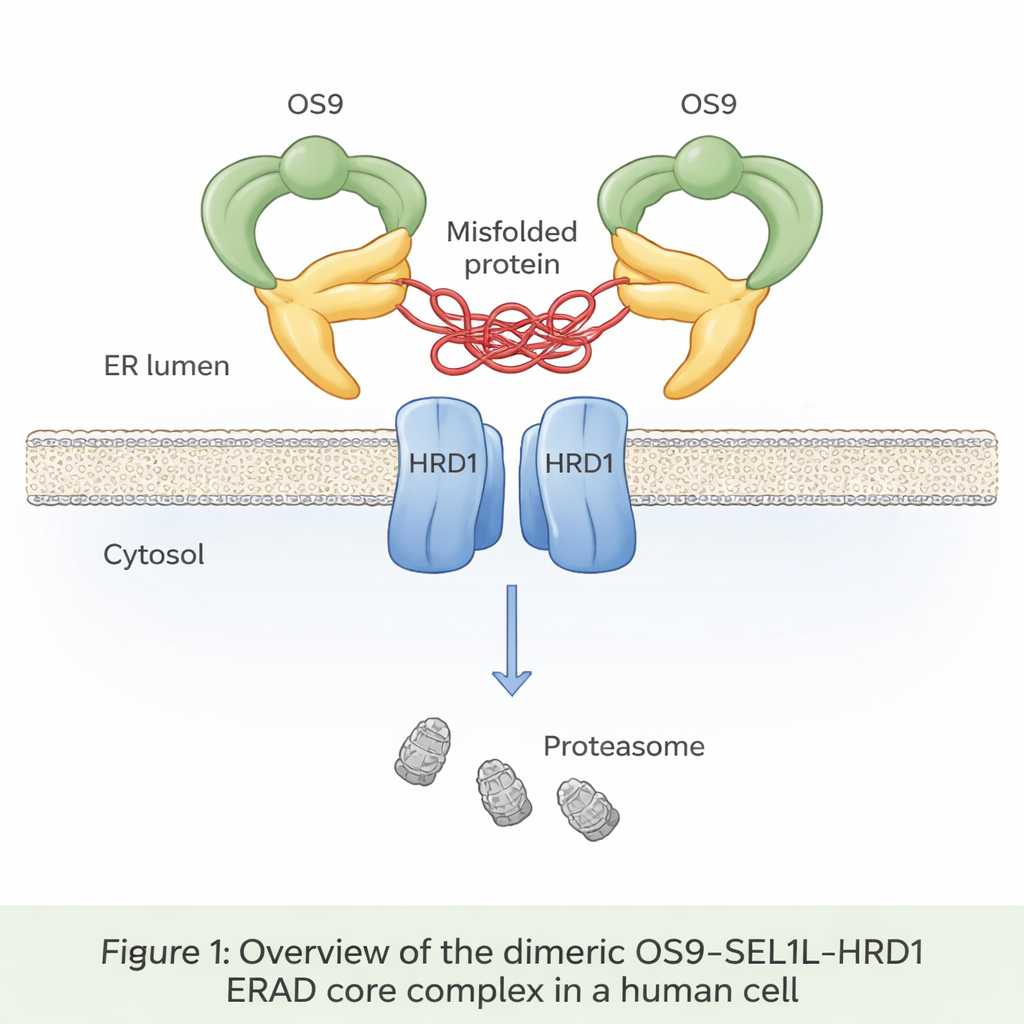
Uma correia transportadora oculta na célula
Até um terço de todas as proteínas recém-sintetizadas entra em um compartimento chamado retículo endoplasmático, ou RE, onde são dobradas e verificadas. Proteínas mal dobradas normalmente são reconhecidas, retiradas do RE e destruídas em um processo conhecido como degradação associada ao RE (ER‑associated degradation, ERAD). No cerne de uma via importante da ERAD está um trio de proteínas: OS9, SEL1L e HRD1. O OS9 atua como sensor de proteínas defeituosas marcadas por açúcares; SEL1L serve de andaime; e HRD1 etiqueta proteínas condenadas com pequenas bandeiras de ubiquitina que as marcam para destruição pelas unidades de descarte da célula, os proteassomos. Até agora, porém, ninguém havia visto em detalhe atômico como essas três peças se encaixam em células humanas.
Revelando a forma da máquina central
Os autores usaram criomicroscopia eletrônica, uma técnica que imagina moléculas congeladas rapidamente em resolução quase atômica, para visualizar o complexo OS9‑SEL1L‑HRD1 purificado de células humanas. Descobriram que ele forma um dímero — basicamente duas cópias idênticas unidas — em vez de permanecer como unidades isoladas. Do lado do lúmen do RE (o interior do RE), duas moléculas de OS9 e duas de SEL1L se montam em um anel semelhante a uma pinça de caranguejo com uma abertura central que parece projetada para agarrar proteínas mal dobradas. Na própria membrana, duas moléculas de HRD1 emparelham-se para formar um canal compartilhado. Esse arranjo posiciona a “pinça” diretamente acima da porta do HRD1, criando um caminho contínuo para que proteínas mal dobradas se movam do lúmen do RE, através da membrana, em direção à degradação no citosol.
Como pequenas mudanças quebram um grande sistema
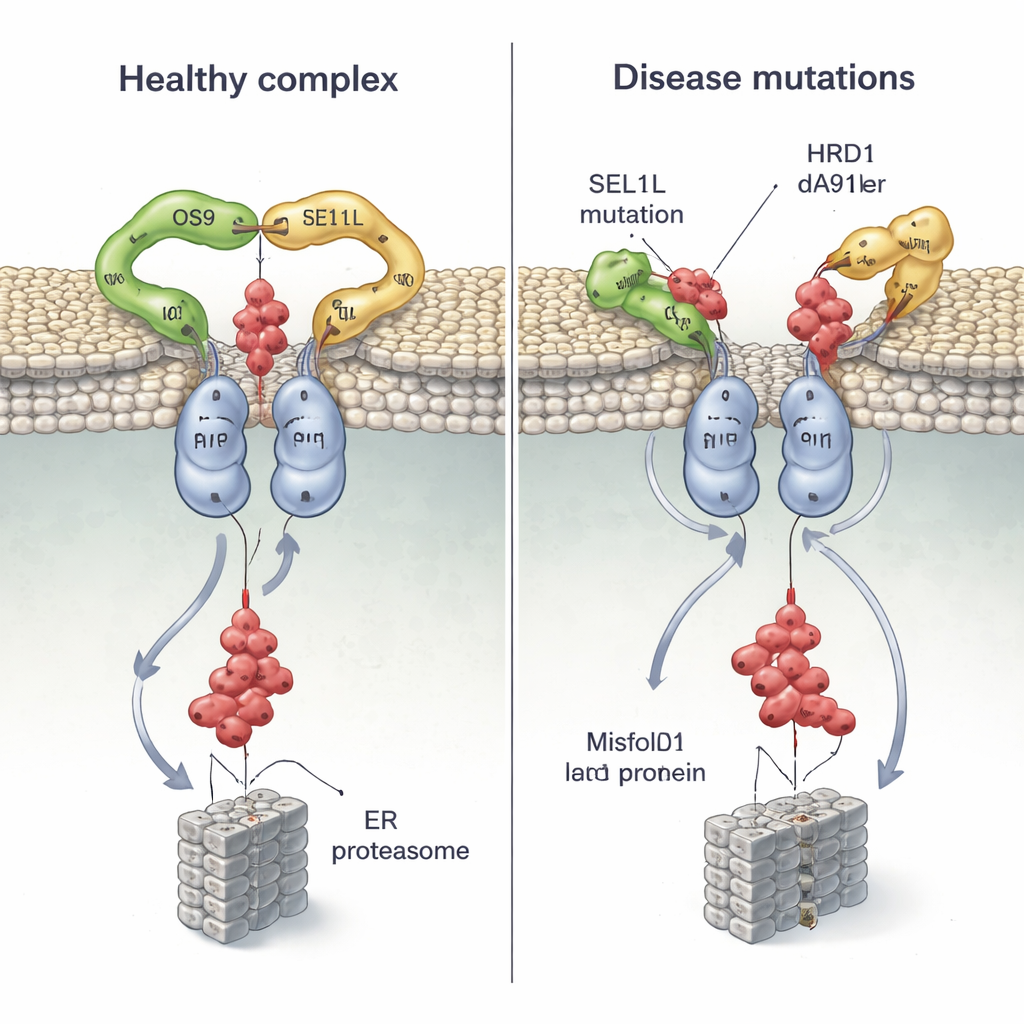
Como mutações em SEL1L e HRD1 foram encontradas em pacientes com distúrbios neurodesenvolvimentais graves e outras doenças, a equipe mapeou várias variantes associadas a doenças em sua estrutura e testou como elas se comportam em células. Duas mutações em SEL1L, G585D e S658P, situam‑se exatamente nos pontos de contato com OS9 e HRD1, respectivamente. Em experimentos celulares, G585D quase aboliu a capacidade de SEL1L de se ligar ao OS9, enquanto S658P enfraqueceu muito sua interação com HRD1; a combinação de ambas as mutações basicamente quebrou o complexo central, sem afetar outros parceiros. Como resultado, as células tiveram dificuldade para marcar e eliminar um precursor hormonal mal dobrado, permitindo que proteínas defeituosas permanecessem.
Uma mutação de doença no canal da membrana
A estrutura também mostra que o segmento transmembrana 3 do HRD1 é a interface chave onde duas moléculas de HRD1 se encontram para formar o canal. Os pesquisadores introduziram “alças” de cisteína em posições específicas e usaram entrecruzamento químico para confirmar que essas regiões entram em contato próximo em células vivas, provando que o HRD1 realmente dimeriza in vivo. Quando eles desestabilizaram um único resíduo altamente conservado (T93) nessa interface, o dímero se desfez e a atividade da ERAD entrou em colapso, mesmo que o complexo ainda se montasse com OS9 e SEL1L. Em seguida, examinaram uma variante de paciente recém‑descoberta, HRD1 A91D, encontrada em uma criança com problemas cardíacos e pulmonares. Essa alteração, também na interface de dímero, reduziu a dimerização do HRD1 em cerca de metade e prejudicou severamente a eliminação de proteínas mal dobradas, novamente sem perturbar a interação global com os parceiros.
Uma nova visão do controle de qualidade de proteínas e da doença
Ao combinar biologia estrutural com testes em células, este trabalho mostra que o complexo OS9‑SEL1L‑HRD1 opera como uma máquina pareada e dimérica: um captador em forma de pinça ligado a um canal compartilhado que encaminha proteínas defeituosas para fora do RE. Mutações que afrouxam a pegada da pinça ou desestabilizam o par de HRD1 não apenas reduzem a eficiência — podem efetivamente entupir o sistema, permitindo que proteínas danificadas se acumulem e contribuam para doenças humanas. Para não especialistas, a mensagem chave é que mesmo mudanças de uma única letra em nosso DNA podem deformar sutilmente a forma de máquinas celulares essenciais, com consequências de grande alcance para o desenvolvimento cerebral, a imunidade e a função dos órgãos.
Citação: Lin, L.L., Maldosevic, E., Zhou, L.E. et al. Structural basis and pathological implications of the dimeric OS9-SEL1L-HRD1 ERAD Core Complex. Nat Commun 17, 2064 (2026). https://doi.org/10.1038/s41467-026-68777-7
Palavras-chave: controle de qualidade de proteínas, retículo endoplasmático, ERAD, complexo SEL1L-HRD1, desdobramento incorreto de proteínas