Clear Sky Science · pt
Perfilagem de deleção de éxons em célula única revela eventos de splicing que moldam a expressão gênica e a dinâmica do estado celular
Como pequenas edições no RNA podem mudar o comportamento celular
Nossas células estão constantemente lendo e emendando instruções de RNA para decidir quais proteínas produzir e como responder ao estresse, crescer ou se dividir. Este estudo mostra que alterar pedaços muito pequenos dessas mensagens de RNA — segmentos únicos chamados éxons — pode remodelar fortemente a atividade gênica e até alterar como as células transitam pelo ciclo celular. O trabalho apresenta uma ferramenta poderosa que permite aos cientistas examinar muitas dessas escolhas de RNA em paralelo, célula a célula, abrindo novas maneiras de entender doenças e descobrir alvos terapêuticos.
Cortando palavras selecionadas do roteiro genético
Os genes são escritos como longos trechos de DNA, mas as células não os leem de ponta a ponta. Em vez disso, cortam e colam blocos menores, chamados éxons, para montar uma mensagem de RNA. Ao escolher quais éxons manter, as células podem gerar múltiplas versões de proteína a partir de um único gene, de modo parecido com produzir diferentes edições de um filme a partir do mesmo material bruto. Muitas doenças, incluindo câncer e autismo, estão associadas a erros nesse processo, e ainda não sabemos para a maioria das escolhas de éxons qual é sua função real. Os autores se propuseram a mudar isso ao construir um sistema em grande escala que pode remover éxons específicos de muitos genes e então observar, em milhares de células individuais ao mesmo tempo, como essas edições afetam a rede interna da célula.
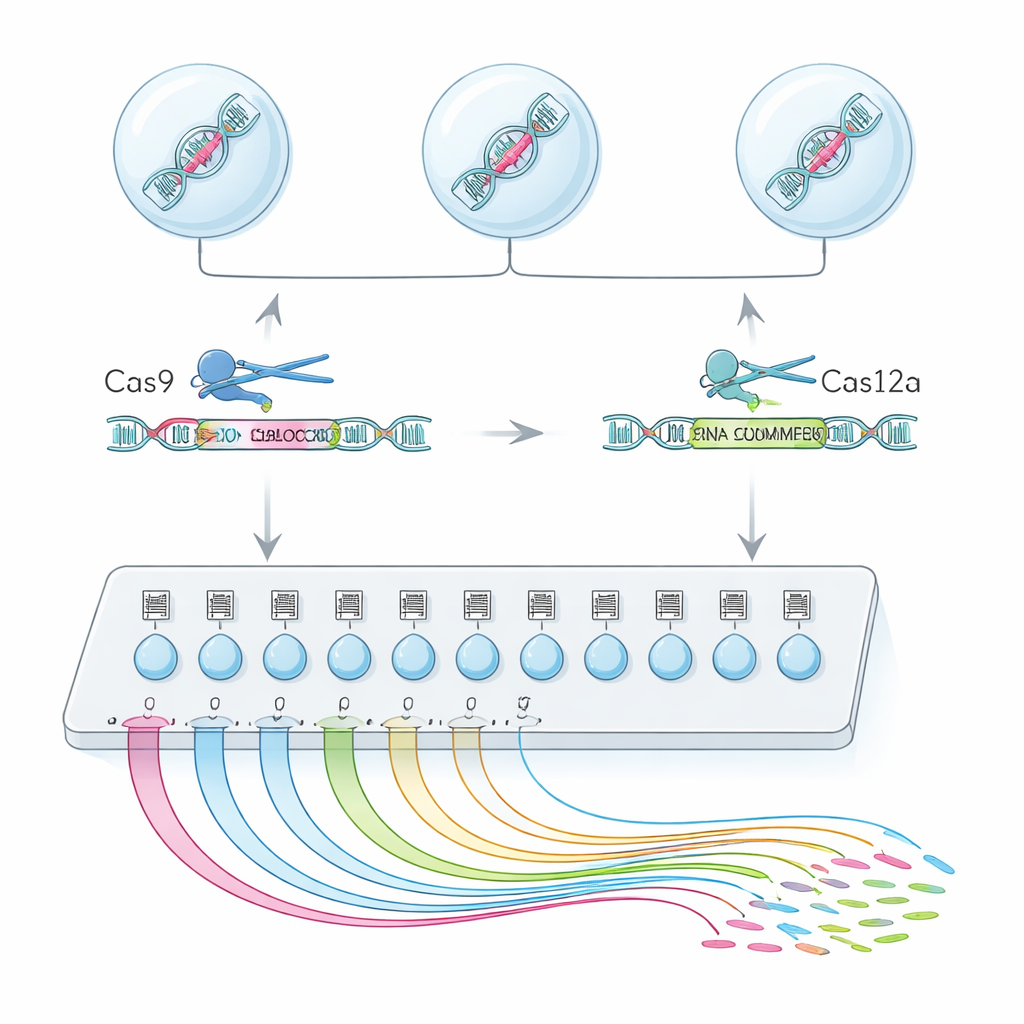
Um "mecanismo de busca" em célula única para a função de éxons
Para conseguir isso, a equipe combinou duas enzimas de edição do genoma, Cas9 e Cas12a, em uma plataforma híbrida chamada CHyMErA. Cada enzima é guiada até o DNA por curtas “endereços” de RNA. Ao direcionar as duas enzimas para cortar logo antes e logo depois de um éxon escolhido, elas podem deletar com precisão esse segmento mantendo o resto do gene intacto. O novo método, scCHyMErA-Seq, vincula esse corte preciso à tecnologia de sequenciamento de RNA de célula única. O RNA de cada célula é capturado em uma gotícula junto com um código de barras e os RNA-guia que especificam qual éxon foi removido. O sequenciamento então revela, para dezenas de milhares de células, tanto a edição recebida por cada célula quanto o padrão detalhado de genes que foram ativados ou silenciados.
Engenharia da ferramenta para ver as duas lâminas da tesoura
Um desafio central foi detectar de forma confiável os RNA-guia da Cas12a ao lado dos da Cas9 no mesmo experimento de célula única. Projetos iniciais ou não capturavam os RNA-guia da Cas12a ou prejudicavam a eficiência de edição. Os pesquisadores resolveram isso redesenhando cuidadosamente a sequência do cabo (handle) da Cas12a para remover trechos que interrompiam prematuramente a transcrição, e adicionando um pequeno elemento estabilizador de RNA e uma etapa de amplificação direcionada. Esses ajustes aumentaram a capacidade de ver ambos os guias em cerca de 90% das células, preservando forte deleção de éxons. Com essa configuração otimizada, os autores triaram 224 éxons alternativos em 161 genes de células humanas, perfilando mais de 200.000 células únicas de alta qualidade.
Descobrindo éxons que controlam programas gênicos e o ciclo celular
Quando a equipe comparou a atividade gênica de células editadas com controles, quase metade dos éxons testados provocou mudanças substanciais em centenas de outros genes. Éxons de genes envolvidos em processamento de RNA e transcrição tendiam a se agrupar, produzindo assinaturas de expressão semelhantes e revelando vias biológicas compartilhadas, como montagem de ribossomos ou degradação de RNA. Em alguns casos, deletar um único éxon teve um efeito claro e interpretável: remover um éxon nos genes TAF5 ou LSM11 atrapalhou o processamento adequado de RNAs histônicos, levando a um acúmulo incomum de mensagens de histona poliadeniladas. O conjunto de dados também destacou dezenas de éxons cuja perda alterou a proporção de células encontradas em diferentes estágios do ciclo celular, vinculando eventos específicos de splicing diretamente a decisões sobre quando uma célula pausa, replica seu DNA ou se prepara para dividir.
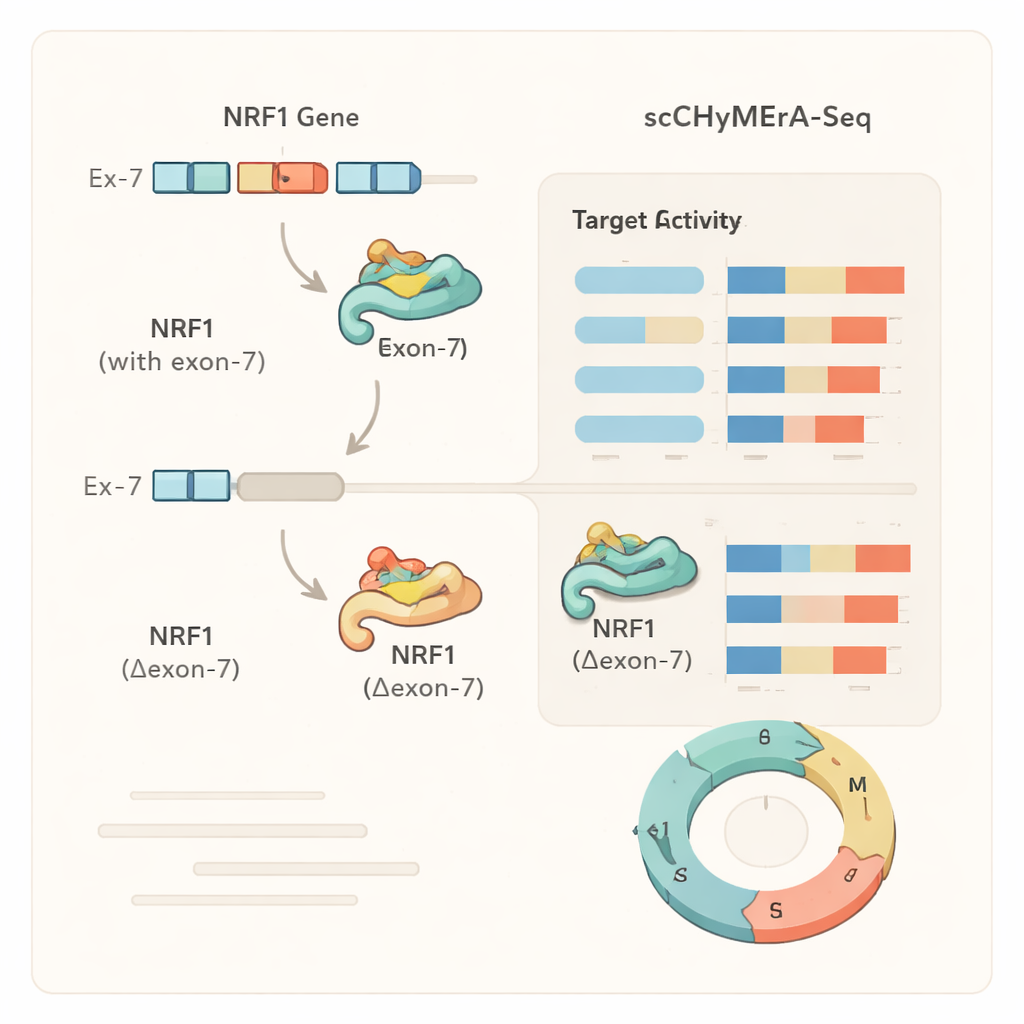
Um estudo de caso: um éxon que regula um mestre controlador
Um exemplo marcante foi o éxon 7 do gene NRF1, um fator de transcrição que controla muitos genes envolvidos na produção de energia celular. Esse éxon se sobrepõe parcialmente à região de ligação ao DNA do NRF1. Quando o éxon 7 foi deletado, centenas de genes controlados pelo NRF1 mudaram sua atividade, e experimentos detalhados mostraram que a proteína NRF1 encurtada tinha muito menos capacidade de se ligar aos promotores-alvo no genoma. Os autores também identificaram um regulador específico de splicing, SRSF3, que promove a inclusão desse éxon, revelando uma cadeia que vai de um fator de splicing, passando por uma escolha de éxon em NRF1, até mudanças amplas em programas gênicos e no metabolismo celular. Análises semelhantes mostraram que, para alguns genes, a deleção do éxon imitou a deleção completa do gene, enquanto para outros produziu uma mudança mais refinada e dependente do estado, sugerindo que éxons alternativos podem modular sutilmente o comportamento da proteína em vez de simplesmente ligá-la ou desligá-la.
Por que isso importa para a saúde e terapias futuras
Para um leitor não especialista, a mensagem principal é que as células dependem da inclusão ou exclusão de segmentos de RNA muito curtos para ajustar como os genes funcionam, e que esses ajustes finos podem alterar traços importantes, como a forma como as células se dividem ou respondem ao estresse. A plataforma scCHyMErA-Seq atua como um teste laboratorial de alta produtividade para essas escolhas de splicing, identificando quais éxons têm impacto funcional real e como eles remodelam estados celulares. Como muitos cânceres e transtornos neurológicos envolvem éxons mal emendados ou fatores de transcrição alterados, essa abordagem pode ajudar a priorizar quais variantes de splicing direcionar com futuros medicamentos ou terapias baseadas em RNA, e fornecer um roteiro para entender como pequenas edições no roteiro genético se propagam em grandes mudanças no comportamento celular.
Citação: Kumari, B., Damodaran, A.P., Guiblet, W.M. et al. Single-cell exon deletion profiling reveals splicing events that shape gene expression and cell state dynamics. Nat Commun 17, 1218 (2026). https://doi.org/10.1038/s41467-026-68774-w
Palavras-chave: splicing alternativo, sequenciamento de RNA de célula única, triagem CRISPR, regulação gênica, ciclo celular